Nano Res.│南开大学刘阳课题组:杯芳烃集成纳米递送体系用于抗癌药物的肿瘤靶向递送和追踪
本篇文章版权为刘阳课题组所有,未经授权禁止转载。
背景介绍
纳米递送体系近年来在临床上得到了非常广泛的研究,可以有效提高药物的有效应和安全性。然而,大多数纳米递送体系的载药方式依赖于物理吸附或包埋,缺乏准确的负载机制,从而导致纳米载体在制备和递送过程中可能造成药物泄漏等问题。为了解决这些问题,科学家们提出将药物直接修饰到纳米递送体系上的共价策略,然而复杂的化学合成和纯化过程限制了它们的普遍应用。大环分子的快速发展为克服传统纳米递送体系的局限性提供了可能,大环分子与药物之间的强键合可以有效地避免药物在血液循环以及正常组织中泄漏。然而大环化合物作为没有靶向能力的小分子,无法通过高通透性和滞留效应(EPR)在肿瘤内富集,从而限制了它们在抗肿瘤中的应用。
成果简介 刘阳课题组集成纳米递送体系和超分子大环主体的优势,构建了一种杯芳烃基纳米递送体系(CanD),用于抗癌药物的靶向递送和体内追踪。CanD由接枝在PHEMA上的磺化偶氮杯芳烃(PHEMA-SAC4A)与接枝在PEG上的罗丹明B(PEG-RhB)自组装而成。SAC4A是一种具有乏氧响应性的超分子大环主体,在常氧条件下与RhB和一系列抗癌药物表现出了很强的结合力,在乏氧条件下结合力下降。这使得CanD可以有效负载药物并在血液循环和正常组织中维持结构稳定性;到达肿瘤乏氧微环境后,CanD解离并释放药物。由于SAC4A的还原同时导致了CanD的解离和药物释放,因此药物释放的同时,RhB的荧光也得到了有效的恢复,因此,RhB的荧光可以用于指示药物的释放情况和体内分布。此外,SAC4A的乏氧响应性还赋予CanD肿瘤靶向能力,从而提高药物在肿瘤内的富集量,并增强其抗肿瘤效果。由于SAC4A可以负载多种抗癌药物,因而CanD可能成为用于递送抗癌药物及体内示踪的潜在通用平台,为研究抗癌药物的疗效提供新的策略。 图文导读 作者简介 刘阳,南开大学化学学院研究员,博士生导师。2011年毕业于南开大学化学学院高分子化学与物理专业,获博士学位。2016年毕业于美国加州大学洛杉矶分校(UCLA)化学工程与分子生物学工程系,获博士学位。从事高分子合成,大分子自组装,药物载体设计与药物输送,纳米医药,癌症免疫疗法等方面的研究。近年来在Nature Nanotechnology、Angewandte Chemie International Edition、Advanced Materials、Nano Letters、Small、Nano Research等期刊发表论文60多篇。 文章信息 L. Xu, J. Chai, Y. Wang, et al. Calixarene-integrated nano-drug delivery system for tumor-targeted delivery and tracking of anti-cancer drugs in vivo. Nano Research. https://doi.org/10.1007/s12274-022-4332-4. 识别二维码或点击左下角“阅读原文”可访问全文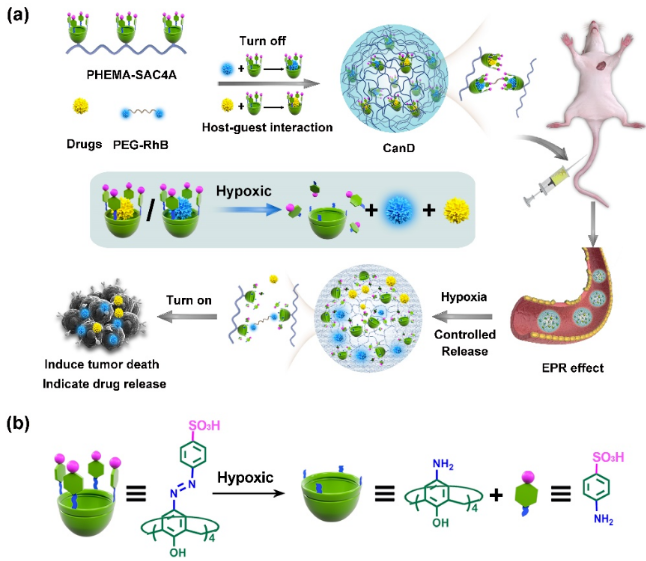


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号