乏氧激活糖代谢共价标记助力肿瘤发生精准诊疗
2019年诺贝尔生理学与医学奖授予对人体细胞感知并适应氧气供应的分子机制研究。众所周知,乏氧应激会影响生理病理的多个方面,例如心肌梗死、中风、外周血管疾病、肺病以及癌症等。特别是乏氧与肿瘤发生、发展及转移之间的紧密关联。因此,了解乏氧变化在肿瘤发生病理过程中的作用对于精准诊疗至关重要,这需要可靠的技术手段来特异性地区分乏氧细胞或组织,并能够将其与生理环境中动态且复杂的疾病状态相关联。目前,已有多种乏氧检测探针被广泛报道,其设计策略主要依赖于对乏氧生物标志物的特异性响应,包括对氧分子的化学或酶促反应。然而,这些类型的乏氧探针分子在实际应用当中,会面临不受限的分子扩散和对环境响应的较低特异性等问题,在动态分析乏氧病理发展以及实时精准治疗方面存在局限。
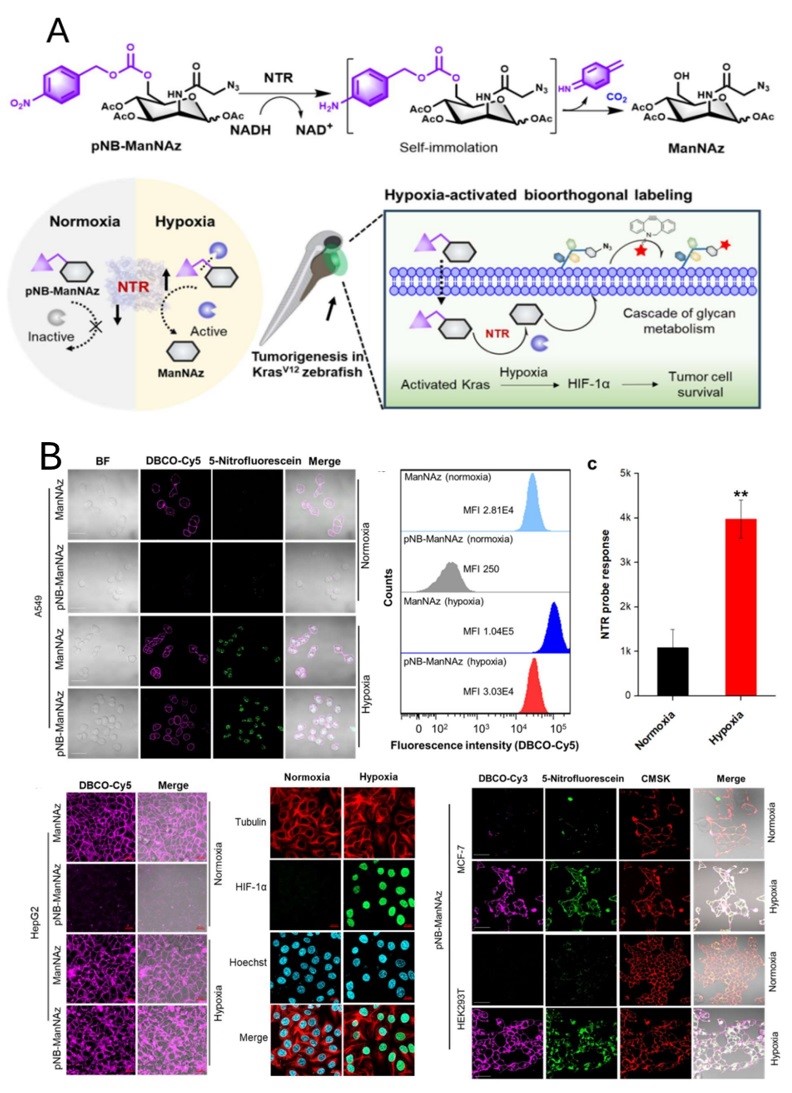
图1. A. 乏氧激活糖代谢共价标记探针响应机制及肿瘤生成的乏氧标记应用示意图;B. 糖代谢共价标记探针对乏氧细胞的标记效果。
为解决这一科学问题,新加坡南洋理工大学邢本刚教授(点击查看介绍)课题组联合北京理工大学王志敏(点击查看介绍)课题组借鉴近年来广泛报道的代谢糖工程(MGE)和生物正交标记技术,开发出一种基于硝基还原酶(NTR)激活的糖代谢标记探针(pNB-ManNAz),可用于肿瘤发生病理乏氧细胞的精准识别和干预。其中,代谢糖工程使用具有叠氮基序的非天然糖,如N-叠氮乙酰甘露糖胺 (Ac4ManNAz),其代谢途径与天然己糖 N-乙酰甘露糖胺相似。可通过一系列酶促转化最终产生胞苷单磷酸-唾液酸 (CMP-Neu5Ac),经高尔基体中的后续翻译后修饰最终代谢加工的产生聚糖与细胞表面糖蛋白结合。通常,上述代谢偶联的生物正交功能基团可以作为化学锚,使各种报告分子能够通过点击反应共价结合到细胞膜上,从而可克服上述提到的探针分子自由扩散等问题。鉴于此,作者们所设计的糖代谢标记探针pNB-ManNAz在正常条件下不可被细胞代谢参与蛋白修饰,但在病理或生理乏氧条件下,硝基还原酶可将其经自消除化学转化为可代谢标记的糖分子ManNAz,能够通过生化合成途径整合到细胞表面糖蛋白上,最后结合生物正交化学实现特异性的共价荧光标记(图1A)。这种乏氧相关酶激活的糖代谢标记探针在多种细胞以及斑马鱼活体模型的乏氧识别中表现出广泛的适用性,特别是在动态监测原位肿瘤发生和体内肿瘤靶向光治疗方面展现出良好的性能。
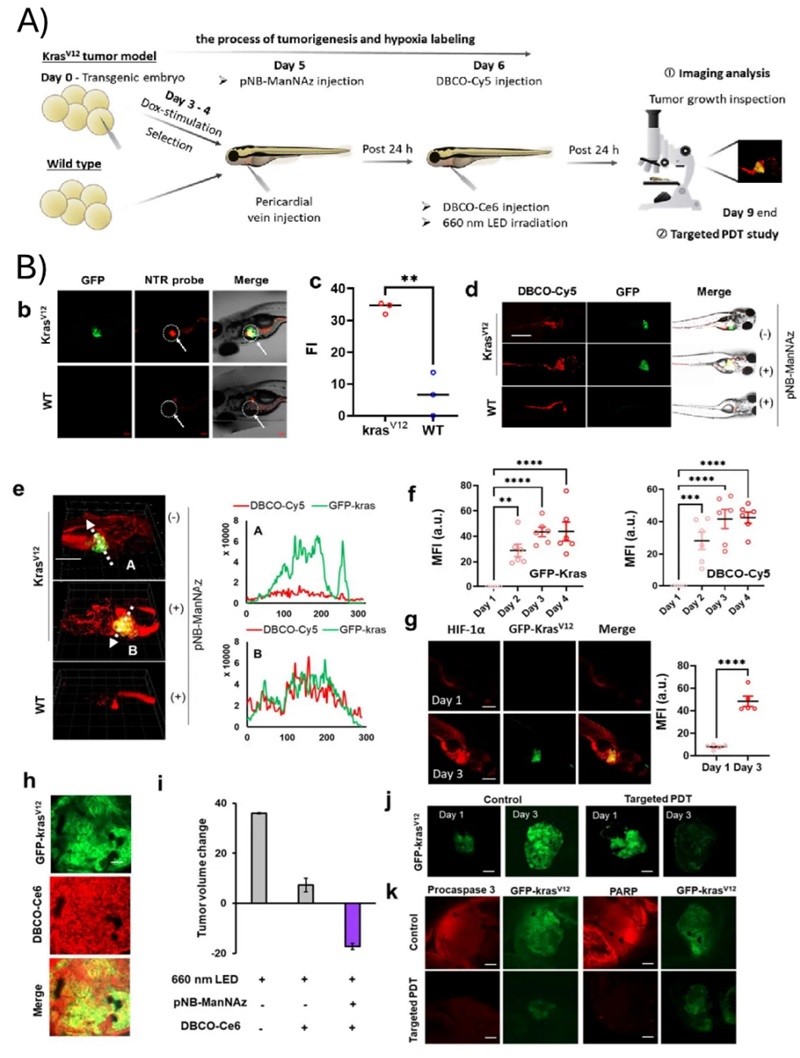
图2. A. KrasV12 突变的斑马鱼模型; B. pNB-ManNAz在携带 KrasV12 突变的斑马鱼中,肿瘤发生过程中低氧肿瘤细胞的体内特异性代谢标记及靶向光动力治疗。
在研究结果方面,作者首先系统性研究了pNB-ManNAz对于硝基还原酶的响应灵敏度和选择性;接着在多种细胞模型上验证了该糖探针分子的乏氧特异性响应共价标记效果,包括A549、HepG2、MCF-7和HEK293T等细胞的正常和乏氧模型(图1B);此外,在斑马鱼生理性乏氧模型中,也表现出显著的乏氧响应性荧光标记能力。截止目前,Kras突变已被证明可导致肿瘤发生,为了评估 pNB-ManNAz 在揭示缺氧调节肿瘤发生的直接证据方面的可行性,作者建立了转基因 KrasV12 突变的肿瘤斑马鱼模型,并使用多西环素(Dox)作为诱导剂(图2A)。为了评估 KrasV12突变肿瘤模型中NTR 的缺氧特异性激活,作者应用了标准的NTR 响应荧光探针来比较野生型(WT)和致瘤斑马鱼之间的低氧酶活性,观察到 NTR 激活的独特荧光响应与 KrasV12-GFP在低氧肝脏肿瘤中共同定位,且3D 荧光成像显示Cy5 与GFP 荧光有良好的重叠,表明缺氧激活的糖探针可用于特异性和准确地监测肿瘤发生(图2B)。此外,KrasV12癌基因激活后,糖代谢标记信号与GFP-Kras 荧光变化以及HIF-1α 的上调相关,证明了缺氧在肿瘤发生过程中的调节作用。随着肿瘤细胞的动态生成和变化,糖探针分子可以高选择性地对新生成的肿瘤细胞进行共价标记,揭示了细胞乏氧在肿瘤生成中的重要作用同时,这种乏氧环境特异性的共价标记策略也实现了对新生成肿瘤的主动靶向的光动力治疗,准确干预了肿瘤病理发生的过程。
总之,该工作报道了一种能够用于肿瘤发生病理乏氧细胞的特异性识别的酶激活糖代谢共价标记工具,对研究肿瘤乏氧相关病理机制及精准治疗提供了新的思路。
相关论文发表于Angewandte Chemie International Edition,论文第一作者是北京理工大学王志敏和新加坡国立大学博士研究生Lau Jun Wei,通讯作者为北京理工大学王志敏副教授和南洋理工大学邢本刚教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Nitroreductase-activatable Metabolic Reporter for Covalent Labeling of Pathological Hypoxic Cells in Tumorigenesis
Zhimin Wang†*, Jun Wei Lau†, Songhan Liu, Ziheng Ren, Zhiyuan Gong, Xiaogang Liu, and Bengang Xing*
Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202411636
邢本刚教授简历

邢本刚,南洋理工大学(NTU),化学、化工和生物技术学院(CCEB)教授。
邢本刚博士近年来主要从事化学生物学,分子探针及标示设计、近红外光控生物调节以及纳米医药等交叉领域方面的研究。迄今为止,邢本刚博士在Sci Adv, Nat Comm, Angew Chem Intl Ed., J Am Chem Soc., Chem Soc Rev.等国际知名学术期刊上发表学术论文160余篇,20余篇国际专利,7本专著等。担任若干学术杂志编辑委员会委员,执行副主编等,并在多个国际学术组织担任职务。
邢本刚
https://www.x-mol.com/university/faculty/4461
团队介绍
https://personal.ntu.edu.sg/bengang/
王志敏
https://www.x-mol.com/university/faculty/376150
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号