Nano Res.[生物]│刘向文课题组:超高载药量ZIF-8纳米封装结构设计合成
本篇文章版权为刘向文所有,未经授权禁止转载。
背景介绍
癌症是导致各国人口死亡的主要原因,在过去的十年里,基于纳米颗粒的药物递送系统在癌症治疗领域引起了越来越多的关注。多种纳米材料被尝试用于药物载体,克服细胞毒性药物在给药过程中的非特异性药物分布问题,提升药物对肿瘤的疗效。然而,大多数纳米药物递送系统的临床应用潜力,会受到载体材料固有细胞毒性和负载药物泄露的限制。因此,如何克服载体材料固有细胞毒性和负载药物的泄漏,成为提高纳米药物递送系统安全性的主要挑战。
成果简介 近日,刘向文课题组基于对ZIF-8胶体颗粒非经典成核途径(X. Liu et al., PNAS., 118, e2008880118, 2021)的深入理解,设计了一种新颖、超高载药量、药物封装的“ZIF-8纳米药物递送系统封装结构”。通过对反应条件的精确控制,实现了在室温、水相、一步反应条件下,无定形ZIF-8表皮对模型药物阿霉素的良好封装,载药量高达90%(即1mgZIF-8封装9mg阿霉素)。对于MOFs来说,这种封装合成工艺是新颖而有启发性的。ZIF-8对药物的封装避免了负载药物泄露的风险,超高载药量则极大程度降低了负载单位剂量药物所需的载体质量,使载体摄入量极大程度低于体内安全极限。因此,设计出的ZIF-8纳米药物递送系统的高载量和药物封装特点,为提高纳米药物递送系统在生物应用中的安全性提出了一种新的策略。 图文导读 图1 超高载药量DOX@ZIF-8合成和其基于酸碱响应性的体内给药示意图 作者简介 刘向文,副研究员,于2013年清华大学化学系获得博士学位,2015-2017年于美国波士顿学院进行博士后研究,2017-2020年于新加坡国立大学进行博士后研究,现任北京市科学技术研究院分析测试研究所先进材料创制及原位表征分析实验室负责人。主要从事金属有机框架材料(MOFs),贵金属及其合金,碳材料等调控合成的探索性研究工作,并且围绕上述材料针对双碳能源以及生物医药等领域开展相关研究,主要包括CO2还原,电解水制氢,异相催化;纳米载药,生物分析,快速检测等。从纳米晶到单原子,围绕其尺寸,组成,形貌以及表面微观结构,研究材料的构效关系;利用先进的液相/气相原位表征技术实现对材料的成核生长以及催化过程进行全生命周期、跨尺度的分析。相关成果发表于PNAS、J. Am. Chem. Soc.、Adv. Mater.、Nano Lett.、等国际知名期刊杂志。承担了多项国家及省部级科研项目,并入选第15批北京项目青年项目。 文章信息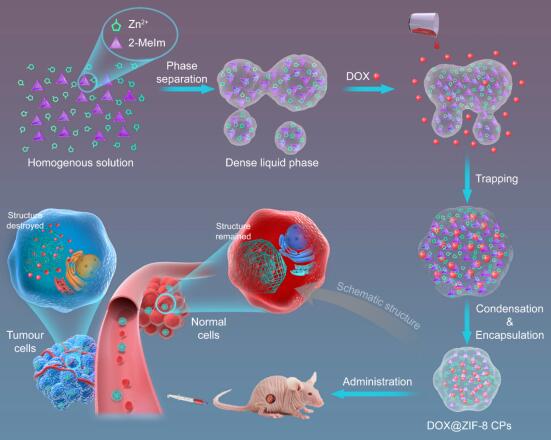

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号