Nano Res.[能源]│电子科技大学王丽平:铜离子迁移诱导CuS相转变与电压衰退
本篇文章版权为王丽平课题组所有,未经授权禁止转载。
背景介绍
转化型正极材料(FeF2、MnO2、FeS2等)具备高理论能量密度和低成本属性,近些年受到的关注正日益增加。其中,CuS材料理论上能实现1015 Wh kg-1和4743 Wh L-1的能量密度,被认为是一种极具前景的转化型材料。该材料最早于1984年被应用于电极活性材料,随后在器件创新、形貌改性、机理研究等角度开展了系列研究,加深了对该材料的认识。关于其充放电反应机理,目前提出了转化-转化型、嵌入-转化型、嵌入-置换型三种反应机理。然而,目前尚未对CuS的结构转变和电压衰退机制达成共识。根据先前的研究,Cu2S、LixCuS(x<0.16)和Li0.83CuS是几种可能的中间产物。不过,这些化合物在解释CuS的电化学行为方面并不充分,因此需要对CuS的中间产物进行进一步研究,确定其结构转变和电压衰退机制。
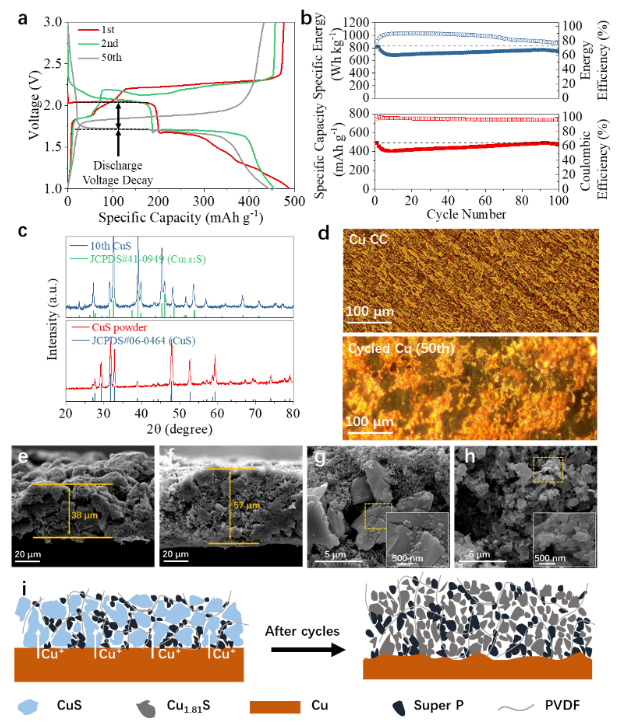
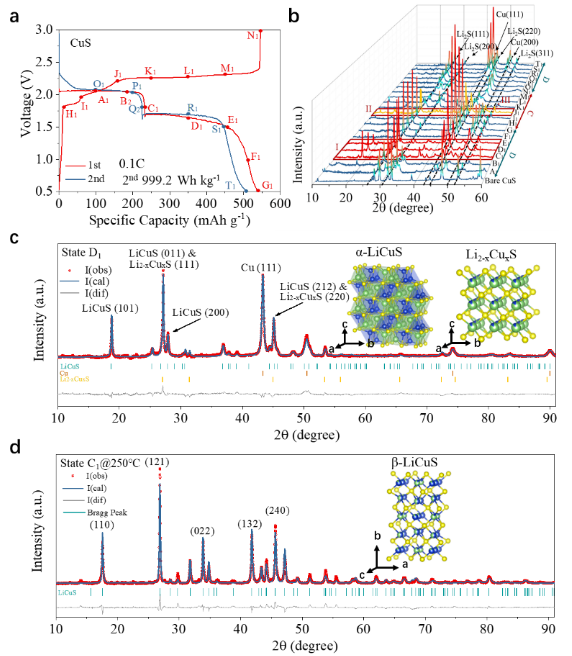
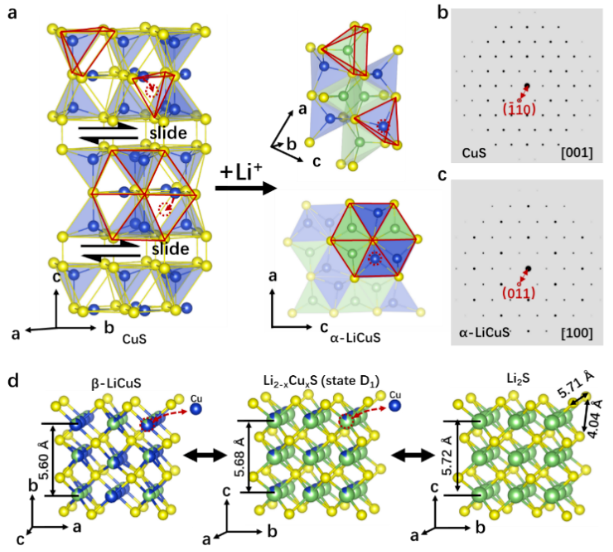
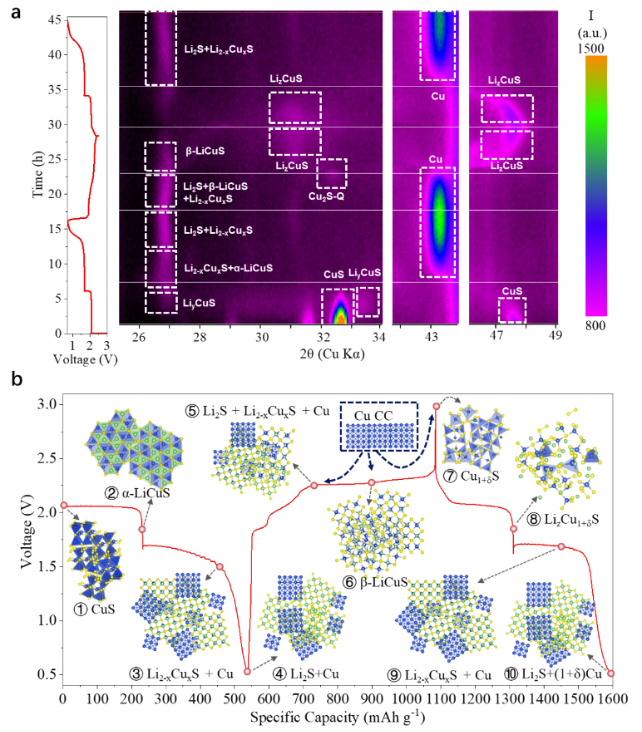
成果简介 电子科技大学王丽平团队利用原位/非原位XRD以及电化学分析,详细解释了CuS材料的反应机理。其中,CuS的电压衰退来源于CuS材料和Cu集流体的自发反应。该过程导致了能量密度损失和活性材料退化(CuS → Cu1.81S)。而CuS的低能量效率被认为是其多种相变导致的,放电过程主要相变涉及为:CuS → α-LiCuS → Li2-xCuxS + Cu → Li2S + Cu;充电过程主要相变为:Li2S + Cu → Li2-xCuxS → β-LiCuS → CuS。其中,α-LiCuS、β-LiCuS和Li2-xCuxS为三种新确定的中间产物。CuS的多重相变的主要驱动力来源于拓扑反应相关的铜离子扩散和重排。基于识别出的多种中间产物,该工作给出了CuS的新反应路径。这项工作强调了了解过渡金属扩散对理解相变和转换型材料电化学行为的重要性。 图文导读 CuS采用Cu和S粉末固相烧结而成,根据充放电测试显示,该材料在0.5C下490 mAh g-1的初始放电容量(1C = 560 mA g-1,图1(a)),100次循环后没有明显的容量衰减(图1(b))。但可以注意到,CuS的高电位放电平台在循环中逐渐退化消失(2.05 → 1.71 V),从第2个循环到第50个循环,该电压降导致11.0%的能量密度损失。这种电压降可以在许多著作中找到,但鲜有讨论。随后进行的XRD测试表明,该电位衰退过程伴随着不可逆相变(CuS→ Cu1.81S,图1(c)),这可能是导致能量密度损失的罪魁祸首。显然,该不可逆相变需要Cu集流体提供额外的Cu,即Cu集流体中的铜原子扩散到CuS阴极中,并生成Cu1.81S。通过光学显微镜镜检,确实观察到了Cu集流体腐蚀的现象,原本光滑的表面循环50次后变得粗糙(1(d))。此外,CuS正极层的体积膨胀也可以视为吸收Cu原子后的附带效应(图1(e-f))。不仅如此,该过程还降低了CuS颗粒的粒径(~5 μm→ ~500 nm,图1(g-h)),产生了更松散的结构。图1(i)给出了CuS退化过程的图示说明。根据热力学计算,若以Cu2S为典型产物,CuS和Cu之间可以实现自发反应: 这也是一些文献开发Cu离子电池的基础(基于Cu2+/Cu+与Cu/Cu+氧化还原电对)。鉴于活性物质与Cu集流体的反应,多种转换型材料比如FeF3、CuF2等可能不适合采用Cu集流体。 为了揭示CuS反应过程中的中间产物,该工作对CuS进行了非原位XRD测试(图2(a-b))。根据XRD曲线,鉴别出了三种未曾明确的中间产物,分别为α-LiCuS(物质I),β-LiCuS(物质II)和Li2-xCuxS(物质III)。图2(c)展示了α-LiCuS的Rietveld精修结果,α-LiCuS属于Pnma空间群,具有CuMgP型结构,其晶胞参数为a = 6.38709 Å,b = 3.75934 Å,c = 7.02002 Å,α = β = γ = 90°。α-LiCuS由[LiS5]棱锥和[CuS4]四面体组成,通过S顶点共享而连接。β-LiCuS属于Ibam空间群(图2(d)),其晶胞参数为a = 5.61822Å,b = 12.057Å,c =5.9784Å,α = β = γ = 90°。β-LiCuS由三种基本结构组成:[Li0.85Cu0.15S4]四面体、[Li0.5Cu0.5S4]四面体和二维[Li0.15Cu0.85S2]棒。其中Cu/Li位点混排水平受锂含量和温度的影响。Li2-xCuxS的结构与Li2S相同(空间群),该物质可以看成是Cu和Li2S的固溶体,Cu的含量与充放电深度相关,所以其晶胞参数是Cu含量x的函数,当其完全放电时,即为Li2S。例如,在D1状态时,Li2-xCuxS晶胞参数为a = b = c = 5.6774 Å,Li2S的晶胞参数为a = 5.7190 Å。两者的仅相差0.7%。进一步对比发现,本文所涉及的几种产物,α-LiCuS、β-LiCuS、Li2-xCuxS和Li2S在27°附近的衍射峰高度重合,这可能是先前工作将这四种物质均认为是Li2S的原因。 接下来,该工作进一步研究了多重相变发生的内在驱动力。根据观察,CuS的相变产物和其母相多具备高度的结构相关性,如CuSα-LiCuS以及β-LiCuSLi2-xCuxSLi2S。这里,图3(a)展示了从CuS到α-LiCuS的变化过程。这种转变涉及Cu+和Li+的扩散和重排,而S原子以最小的位移保持了CuS的骨架稳定。具体的,Cu原子将自己从CuS的[CuS3]三角平面中重新定位到α-LiCuS的[CuS4]四面体中。这种扩散行为可归结于Cu+的高扩散系数(10-7-10-9 cm2 s-1)以及Cu+和Li+相似半径的(0.77 vs. 0.76Å)。整个变化过程[S5]四棱锥和[S6]环在相变期间几乎保持不变。CuS([001]方向)和α-LiCuS([100]方向)的模拟电子衍射图也显示了它们的结构一致性(图3(b-c))。这种母相和生成相之间的平滑相变通常被称为“拓扑反应”,这种反应有利于反应动力学。图3(d)展示了另一个基于铜离子迁移相关的拓扑相变反应。在放电过程中,β-LiCuS中高度混排的Cu和Li原子逐渐析出单质Cu,从而生成Li2-xCuxS;进一步放电,Li2-xCuxS完全析出Cu,从而生成Li2S。注意到,β-LiCuS的(100)面和Li2-xCuxS的(010)面之间的晶格失配仅为1.4%,从而令拓扑相变得以容易发生。注意到,Cu的析出和金属化过程均会涉及到Cu原子的扩散,而先前的文献也表明Cu迁移可以快速进行并使得Cu金属高度结晶化,这与该工作结果一致。更重要的是,这种Cu的析出-金属化过程是可逆的(Cu0→ Cu+),Cu可以再次溶解到晶格之中并由Li2S生成Li2-xCuxS。在该反应期间,Cu集流体表面上的Cu也可以被氧化成Cu+从而扩散到活性材料中,这便解释了宏观的Cu集流体腐蚀和CuS退化(CuS → Cu1.81S)。 根据上述研究结果,再结合原位XRD测试,该工作重新梳理了CuS的反应路径。放电时,Li可以占据[S5]四棱锥和S-S空位层的空位,而一些铜原子迁移到[S4]四面体的中心,在放电早期形成非化学计量比LiyCuS(y < 0.36)化合物(图4(a))。然后,非化学计量比LiyCuS在进一步嵌锂后转变为α-LiCuS。随后,α-LiCuS转化为Li2-xCuxS,再是Li2S。首次放电反应如下: 在首次充电中,初始产物为Li2-xCuxS,然后转变为β-LiCuS。紧接着,β-LiCuS在充电过程中部分转化为Cu2S(Chalcocite-Q)。特别值得注意的是,剩余的β-LiCuS、Li2-xCuxS和Cu2S在进一步脱锂后转化为另一种Li-Cu-S固溶体(LizCuS,z < 1)。根据XRD图谱,该中间体与LiyCuS不同。这种差异可能是由于初始CuS和循环CuS的结晶度和缺陷量不同造成的。LizCuS到CuS的变化是一个连续的转变,这一点可以通过在47.5°附近峰的逐渐位移来证明(图4(a))。注意,充电过程包含Cu的氧化,不仅是CuS层中的Cu,也包括Cu集流体中的Cu。因此,最终产品是有缺陷的CuS(Cu1+δS,δ < 1),额外的Cu来源于Cu集流体。因此,首次充电过程的电化学反应可以写为: 为了简要说明CuS的反应机理和退化原理,图4(b)标记了不同状态下的主要产物。综合上述化学方程式可以得出结论,在整个反应过程中,S价保持恒定(S-2)。因此CuS的反应中并无显著的多硫化物的产生,这有利于CuS的循环稳定性。尽管上述反应是在使用Cu集流体时获得的,但由于首次充放电涉及的Cu集流体反应量很少,因此所述的充放电机理仍可以迁移到使用其他集流体的情形(如Al、Ti集流体)。 图4(a)CuS的原位XRD图谱。(b)放电/充电过程中CuS的相变。 作者简介 王丽平研究员简介:王丽平,电子科技大学研究员/博士生导师。中南大学应用化学学士(2006年)、中科院物理研究所凝聚态物理和法国亚眠大学固体材料(双)博士学位(2011年),曾在德国马普胶体与界面研究所、美国布鲁克海文国家实验室从事研究工作。2014年加入电子科技大学,先后副教授、研究员。从事高能量密度锂电池材料和器件研究,主持国家级、企业委托技术开发等项目10余项;在Joule, Advanced Materials, Journal of the American Chemical Society等期刊共发表学术论文100余篇;合作撰写专著一部;在国内国际做邀请报告20余次;申请中国专利29项,获授权17项(转化3项)。获电子科技大学“百人计划”、四川省高层次人才计划和四川省杰出青年科学基金支持。担任Nano Research期刊客座编辑,Energy Material Advances期刊和eScience期刊青年编委。 通讯邮箱:lipingwang@uestc.edu.cn 研究生报考链接:https://yjsjy.uestc.edu.cn/gmis/jcsjgl/dsfc/dsgrjj/11820?yxsh=03。 文章信息 Zou J, Wu Z, Tang R, et al. Copper diffusion related phase change and voltage decay in CuS cathode. Nano Research, 2023, https://doi.org/10.1007/s12274-023-5627-9. 识别二维码或点击左下角“阅读原文”可访问全文
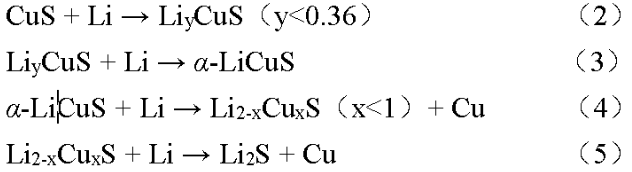
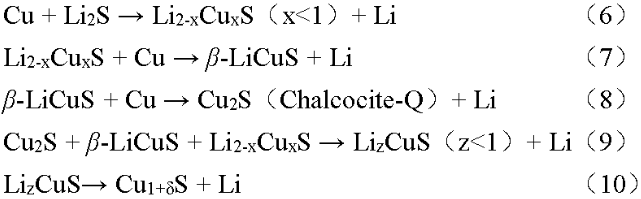


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
























































 京公网安备 11010802027423号
京公网安备 11010802027423号