原核细胞内的无膜“细胞器”:基于蛋白质相分离的生物合成酶区室化
原核细胞相比真核细胞,大都结构简单。比如因为缺乏细胞器,大肠杆菌常常被比作一个“茶包”:所有的酶、mRNA等生物分子无序分散在细胞膜所包裹的细胞液中,改造大肠杆菌作为细胞工厂生产生物活性分子时候也是如此。代谢工程学家通常缺乏有效的手段来调控生物酶的细胞内时空分布,异源表达的生物酶一般认为将无序分散在细胞液中。
香港中文大学夏江教授(点击查看介绍)相信调控酶的相对位置和空间分布,将会对生物合成起到四两拨千斤的功效。他们通过多酶组装来改变酶的空间位置,发现将多个酶组装在一起这一简单操作可以大大提升生物催化的效率,提高最终产物(以萜类作为模型)的产率。比如膜定位组装(Nat. Commun. 2019),共价组装酶复合物(ACS Nano 2019)和以类病毒颗粒作为模板组装(Bioconjugate Chem. 2021)等多酶自组装都实现了提升细胞内生物合成的产率。然而这些组装方式只是机械地将多个酶结合到一起,并没有能够有效模拟天然多酶复合物的动态性:既能和外界环境快速交流,又保持相对的结构独立性。
若论到动态又独立的区隔方式,其中的翘楚非无膜细胞器莫属。液-液相分离(Liquid-liquid phase separation, LLPS)是细胞内很多重要生命过程的关键驱动机制,细胞常常通过LLPS富集相关的生物分子,形成无膜的亚细胞结构。这些分子团聚体并非固态沉淀,而是高度聚集的(一般团聚体内部蛋白浓度大概是外部浓度的几十至上百倍)、动态的(团聚体可以融合也可以分裂)、流动的(团聚体作为独立的结构单位可以在细胞内流动)。这一奇特的现象在高分子物理领域和蛋白质结晶领域颇为常见,最近在细胞生物学中被广泛报道,但在合成生物学领域仍然少有涉及。
有鉴于此,该团队设想能否在大肠杆菌内部通过LLPS产生新的“人造细胞器”,并且通过把多个酶组装其中来实现具有催化功能的“人造细胞器”呢?于是该团队遵循从简单到复杂,从胞外到胞内的原则做了如下尝试。
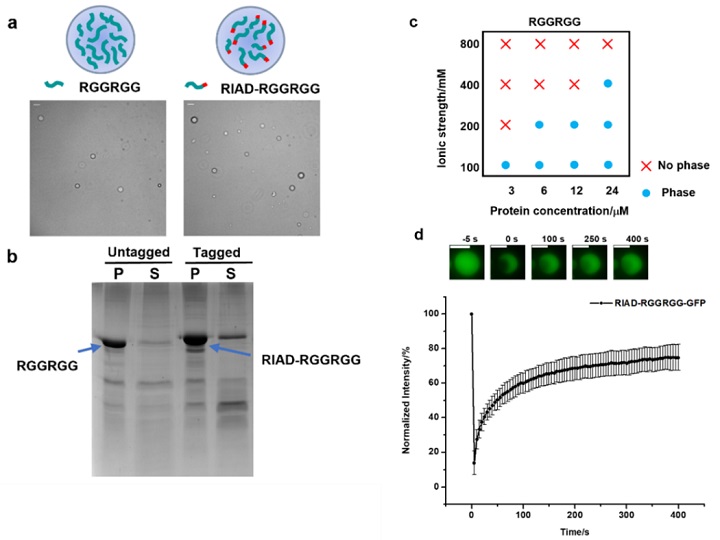
作者首先通过体外重构融合相分离形成蛋白RGGRGG,激光共聚焦显微镜和SDS-PAGE显示了液液相分离的形成,相图反应了盐浓度和蛋白浓度对LLPS形成的影响,光漂白后的荧光恢复实验展示了相分离的液体性质。并且证明了融合一个相互作用多肽RIAD并没有改变RGGRGG蛋白相分离的性质。这一个工作是后续工作的最基础的准备。
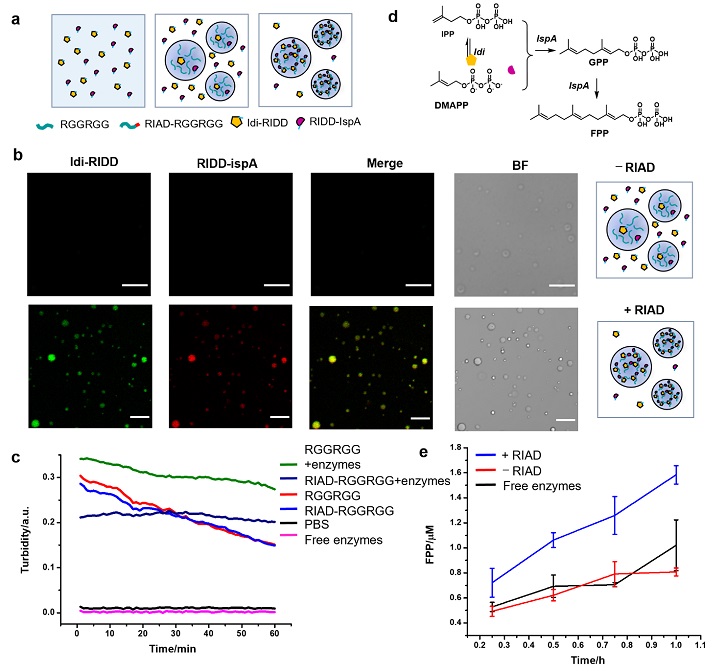
接着,作者尝试将生物催化酶组装进入相分离团聚体。作者选取了法尼烯生物催化过程中的两个关键酶Idi和IspA,发现通过多肽相互作用把酶招募进团聚体中,FPP的产率由0.82-1.02 μM/h提升到了1.58 μM/h。
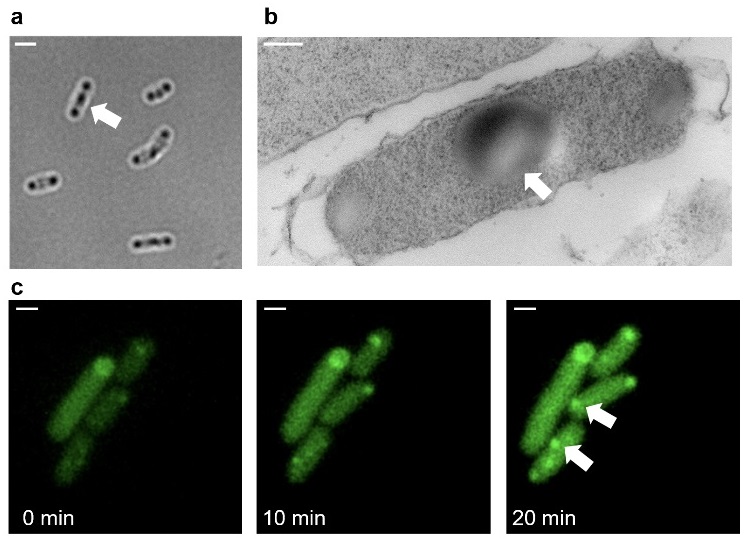
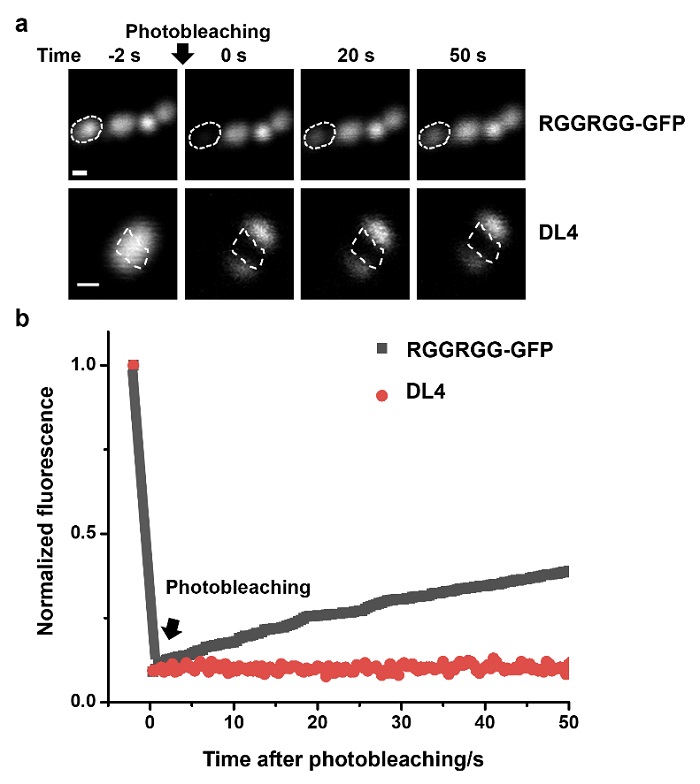
受此激励,作者开始在大肠杆菌细胞内构建无膜细胞器。出乎意料,过表达RGGRGG蛋白后,在细菌中形成在普通光学显微镜下都可以观察到的蛋白质团聚体,在电镜下清晰可见。这些蛋白质团聚体证实并非固体沉淀。在经过双光子激发显微镜荧光淬灭后,通过LLPS形成的团聚体仍具有荧光恢复的能力。
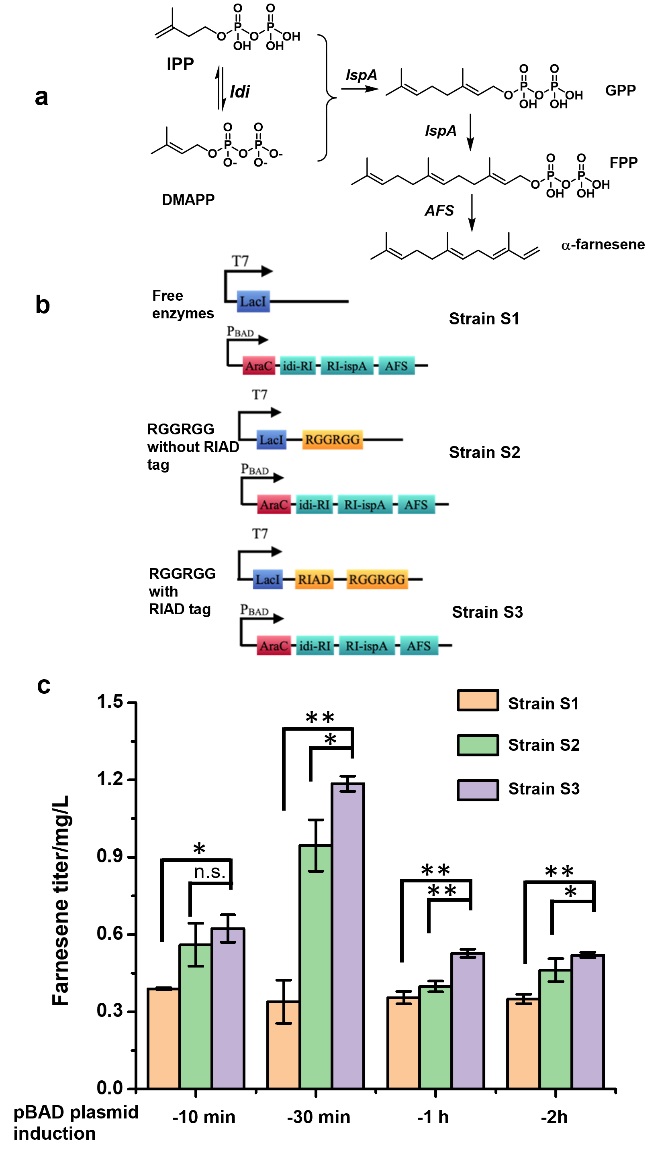
最后作者把Idi、IspA和AFS三个酶组装到蛋白团聚体中,构建了多个法尼烯生产菌株。比较完全没有蛋白团聚体的菌株和具有团聚体但没有组装机制的菌株,通过多肽相互作用组装酶的团聚体菌株具有最高的法尼烯产率。这一结果最终证明调节酶的空间位置(并没有改变单个酶的活性)可以促进级联的生物催化反应的效率,从而获得更高产的菌株。
本工作共同一作为香港中文大学化学系博士生王越和刘敏。香港中文大学生命科学学院姜里文教授、香港科技大学电子与计算机工程系瞿佳男教授、香港中文大学生物医学工程系周仁杰教授提供了显微镜、电镜方面的帮助。本工作得到科技部重点专项2018YFA0903204和研究资助局课题14304921的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Phase-Separated Multienzyme Compartmentalization for Terpene Biosynthesis in a Prokaryote
Yue Wang, Min Liu, Qixin Wei, Wanjie Wu, Yanping He, Jiayang Gao, Renjie Zhou, Liwen Jiang, Jianan Qu, Jiang Xia
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202203909
导师介绍
夏江
https://www.x-mol.com/university/faculty/53892
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号