含血红素L-酪氨酸羟化酶的芳香烃C-H和C-F键裂解机理
在自然界中,二羟基苯丙氨酸(多巴)通常由非血红素含铁酶催化合成。近年来,含血红素的L-酪氨酸羟化酶(TyrH)作为一类新型的多巴生成酶被逐渐报道。该类酶在抗菌抗癌类天然产物的生物合成途径中,利用血红素催化过氧化氢,从而实现酪氨酸的氧化。
近来的研究表明TyrH在同一底物的催化中可表现出双重活性:当3-氟代酪氨酸作为反应底物时,TyrH不仅得以如预想那样裂解C-H键生成氟代多巴,还可以裂解化学惰性很强的C-F键生成氟离子和多巴 (ACS Catal., 2019, 9, 4764–4776)。同一酶对同一底物进行两种截然不同的催化反应是十分有趣的现象,然而这背后的化学原理却并非显而易见。从蛋白一级结构和催化反应产物和上看,TyrH与其他芳香烃羟化酶或C-F键裂解酶非常的不同。因此,从分子层面解释该现象显得非常必要和有意义。
近日,德州大学圣安东尼奥分校的Feradical(Aimin Liu,刘爱民)(点击查看介绍)课题组通过光谱学、基因突变和X-射线晶体学等方法对该现象进行了研究,提出了两种对应的机理来解释C-H键和C-F键的断裂原理。相关成果已于Journal of the American Chemical Society 发表,刘爱民教授和其博士研究生王一帆分别为论文通讯作者和第一作者。
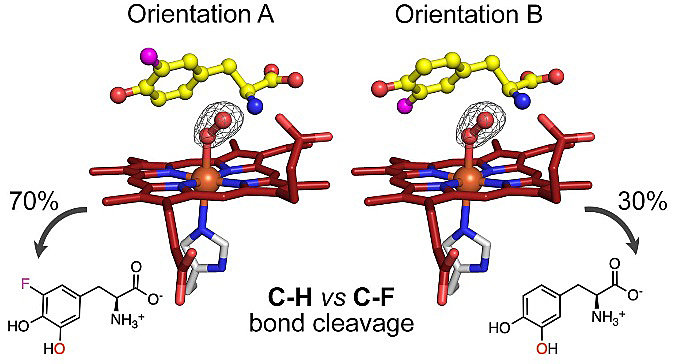
该课题组首先从功能上发现了一个新的、源于嗜热菌(Streptomyces sclerotialus )的TyrH,并由此获得了该类酶的首个蛋白晶体结构。酪氨酸在活性中心的结合构象揭示了在C-H键断裂的过程中,底物的活化是由电子转移引发的。此外,由蛋白结构引导的突变研究确定了一个在催化过程中扮演重要作用的组氨酸。1.68 Å 分辨率的含3-氟代酪氨酸的复合体结构 (DOI: 10.2210/pdb7KQS/pdb, 2021/3/31发布) 解释了双重活性是由氟取代基的两种朝向引起的,其比例为7:3,对应了C-H键和C-F键断裂后形成的羟基化产物的比例。利用在晶体中极大减缓的反应速率,该课题组得以在1.58 Å的晶体结构 (DOI: 10.2210/pdb7KQU/pdb, 2021/3/31发布) 中观察到一个氢过氧化物结合的血红素中间体,并通过其特征吸收光谱确定该中间体为Fe3+-OOH。鉴于该中间体只积聚于含3-氟代酪氨酸,而非酪氨酸的蛋白复合体中,课题组提出Fe3+-OOH是促成C-F键而非C-H键活化的中间体的理论。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Molecular Rationale for Partitioning between C–H and C–F Bond Activation in Heme-Dependent Tyrosine Hydroxylase
Yifan Wang, Ian Davis, Inchul Shin, Hui Xu, and Aimin Liu*
J. Am. Chem. Soc., 2021, DOI: 10.1021/jacs.1c00175
Feradical课题组
http://feradical.utsa.edu/index.html
https://twitter.com/Dr_Feradical
https://www.x-mol.com/university/faculty/5229
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号