南佛罗里达大学蔡健峰课题组关于磺基-γ-AA拟肽近几年的研究进展
拟肽折叠体 (Peptidomimetic foldamer) 具有稳定的和可预测的结构、显著提高的抗蛋白降解能力、结构修饰多样化以及具有模仿生物分子的多功能性等优点,因此在生物医学应用中的有大的前景。然而,由于天然大分子展现出无穷无尽的折叠结构和功能,使得探索折叠体的应用仍然至关重要。因此,当务之急是继续发现具有新框架和分子支架的非天然折叠结构。为此,南佛罗里达大学蔡健峰课题组独立开发了一种新型的类肽模拟物,称为“γ-AA肽”,它们是基于手性肽核酸(PNA)骨架开发的γ-取代-N-酰化-N-氨基乙基氨基酸的低聚物。迄今为止,γ-AA肽已显示出对蛋白水解降解的完全抵抗力,并具有引入化学上多样化的官能团的无限潜力,这在生物医学和材料科学领域显示出了新的应用潜力。但是,γ-AA肽的结构最初是未知的,因此很长时间以来不可能为模仿蛋白质螺旋结构域进行合理的设计,这相当地限制了它们的潜力的发挥。令人高兴的是,自从2017年起,蔡健峰课题组获得了一系列螺旋磺酸基-γ-AA肽(γ-AA肽的亚类)的晶体结构。单晶X射线晶体学表明,磺基-γ-AA肽折叠成具有独特螺旋参数的前所未有的和明确定义的螺旋。因其明确的大小、形状和折叠构象,基于磺酰基-γ-AA肽的折叠剂的设计为开发替代性非天然拟肽在化学、生物学、医学、材料科学和生物化学领域的潜在应用开辟了一条新途径。
近日,南佛罗里达大学蔡健峰(点击查看介绍)课题组在最新发表的Acc. Chem. Res. 综述中简要介绍了磺基-γ-AA肽及其作为螺旋模拟物的应用。他们首先简要介绍磺基-γ-AA肽的设计和合成策略,然后描述螺旋形磺基-γ-AA肽的晶体结构,包括左手的均相磺基-γ-AA肽(Angew. Chem. Int. Ed., 2018, 9916-9920),右手的1:1α/磺基-γ-AA杂化肽(J. Am. Chem. Soc., 2018, 140, 17, 5661-5665; Angew. Chem. Int. Ed., 2019, 58, 7778-7782 )和右手2:1 α/磺基-γ-AA杂化肽(J. Am. Chem. Soc., 2017, 139, 7363-7369)。之后,作者举例证了螺旋磺酰基-γ-AA肽的几个在生物医学上的相关应用,例如破坏BCL9 /β-catenin(Proc. Natl. Acad. Sci. U. S. A., 2019, 116, 10757-10762),p53 / MDM2 / MDMX (J. Med. Chem., 2020, 63, 975-986)的癌症相关蛋白质-蛋白质相互作用(PPI)以及模仿GLP-1(Sci. Adv., 2020, 6, 20, eaaz4988)。此外,作者还举例说明了它们在材料科学中的潜在应用(J. Am. Chem. Soc., 2019, 141, 12697-12706)。希望这些工作可以揭示螺旋磺基-γ-AA拟肽的基于结构的设计和功能,这可以为探索和产生具有独特结构和功能特性的新型折叠拟肽提供一种新的替代方法。
1.螺旋磺基γ-AA肽的晶体结构
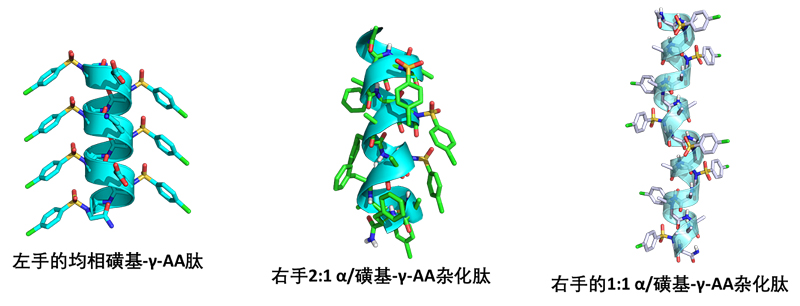
2. 螺旋磺基γ-AA肽在药物化学和材料科学领域的应用
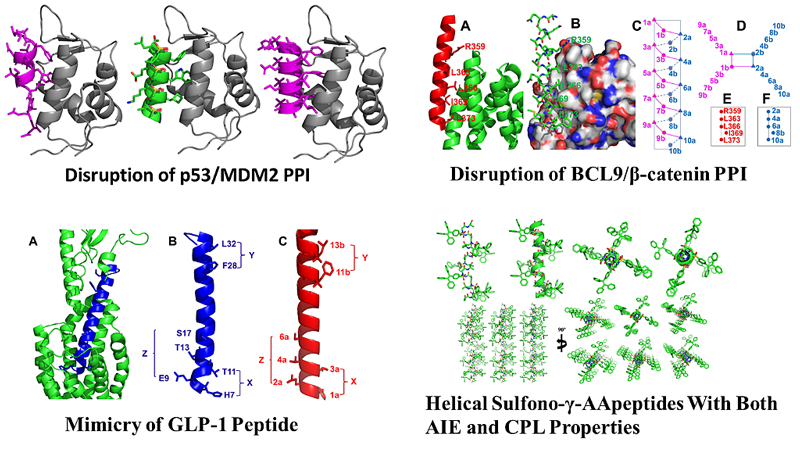
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Sulfono-γ-AApeptides as helical mimetics: Crystal structures and applications
Peng Sang, Yan Shi, Bo Huang, Songyi Xue, Timothy Odom, Jianfeng Cai
Acc. Chem. Res., 2020, 10.1021/acs.accounts.0c00482
蔡健峰现任南佛罗里达大学卓越教授(USF Preeminent Professor),英国皇家化学会会士。其团队主要从事生物有机、化学生物学、药物化学方面的研究。
课题组主页
http://jianfengcai.myweb.usf.edu/
https://www.x-mol.com/university/faculty/47852
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号