Cell Chem Biol:人CDY chromodomain结合选择性的结构基础
CDY家族蛋白是一个包含chromodomain的小家族,它的chromodomain与HP1和Polycomb蛋白非常相似,也能够识别组蛋白和非组蛋白赖氨酸甲基化的ARKS motif。尽管CDY蛋白的chromodomain具有~85%的序列相似性,但它们对嵌入在不同序列背景下的赖氨酸甲基化的ARKS motif显示出不同的结合能力。
为了更好地了解这些chromodomain的结合选择性,近日多伦多大学结构基因组中心(SGC)闵金荣教授团队与北京大学IDG麦戈文脑科学研究所王韵教授团队合作,完成了题为“Structuralbasis for the binding selectivity of human CDY chromodomains”的合作研究,相关工作发表于Cell Chemical Biology,天津医科大学基础医学院的董城博士、苏州大学药学院的刘艳丽博士、北京大学的Tian-JieLyu博士为本文的共同第一作者。
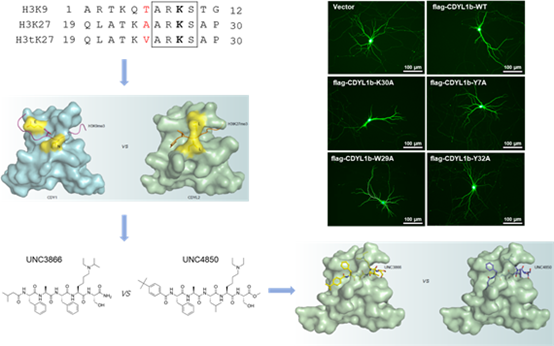
在本研究中,作者对人类基因组编码表达的CDY chromodomain进行了定量结合分析和结构分析。其ITC结合分析显示,CDY1的chromodomain选择性结合组蛋白H3K9me3,而CDYL1b和CDYL2的chromodomain倾向于结合H3K9me3和睾丸特异性的H3tK27me3。结构研究显示,CDY1利用一个E-Nclasp与H3T6形成氢键,选择性地结合H3K9me3。相比之下,CDYL2使用L-Lclasp与H3tK27me3肽段中的H3V24形成有利的疏水相互作用。作者使用CBX4/7特异性化学探针UNC3866进一步证实了不同蛋白chromodomain clasp在配体选择性中起重要作用。进一步的功能研究表明,CDYL1b调节神经发育依赖于其识别赖氨酸甲基化的ARKS motif。最后,作者利用一个更具有CDYL1/2选择性的化合物UNC4850进一步探索CDYL1/2结合配体的相互作用机制。这些结构和结合研究将促进日后对CDY家族蛋白chromodomain特异性小分子抑制剂的研发,从而推动对CDY家族蛋白的功能及其与配体相互作用的进一步研究。
上述研究得到NSERC基金(RGPIN-2016-06300)、国家自然科学基金(31500615、31500613、31530028、31720103908、81821092、31900865)等基金的资助。
原文:
https://www.cell.com/cell-chemical-biology/fulltext/S2451-9456(20)30153-7
Structural Basisfor the Binding Selectivity of Human CDY Chromodomains.
Cheng Dong, YanliLiu, Tian-Jie Lyu, Serap Beldar, Kelsey N Lamb, Wolfram Tempel, Yanjun Li, ZoeyLi, Lindsey I James, Su Qin, Yun Wang, Jinrong Min
Cell Chem. Biol., 2020, DOI: 10.1016/j.chembiol.2020.05.007
X-MOL导师网页:
闵金荣
https://www.x-mol.com/university/faculty/215040
王韵
https://www.x-mol.com/university/faculty/83178
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!








































 京公网安备 11010802027423号
京公网安备 11010802027423号