靶向线粒体代谢和糖酵解的金属抗肿瘤药物
线粒体是细胞内微小的细胞器,它通过产生ATP为细胞运转提供几乎全部所需的能量。线粒体广泛参与信号传导、能量代谢、自噬凋亡等细胞过程,对维持生物体正常生理功能至关重要;同时,其功能损伤也与癌症、老年痴呆等多种疾病的发生发展密切相关。线粒体功能需要在多种蛋白质和无机物共同参与下才能完成,所以可利用金属配合物的独特理化性质来进行干预或调控,从而实现预防或治疗疾病的目的。癌细胞的能量代谢过程不同于正常细胞,它们优先选择有氧糖酵解作为葡萄糖的代谢途径,这种异常的能量代谢过程涉及众多蛋白质和酶,从而为设计抗癌药物提供了潜在靶点。近年来南京大学郭子建院士和王晓勇教授研究团队以调控细胞线粒体功能和能量代谢为主题开展了系统研究,取得了一系列重要研究成果,引起国内外同行的关注。
(一)线粒体靶向性铂配合物抑制肿瘤能量代谢
顺铂是临床应用最广泛的金属抗癌药物,然而如何解决顺铂的毒性和耐药性一直是医药领域面临的挑战。糖代谢有两种途径:线粒体氧化磷酸化和糖酵解。正常哺乳动物细胞在有氧条件下,糖酵解被抑制。上世纪20年代,德国生物化学家Otto Warburg发现了著名的“Warburg效应”,即在氧气充足条件下恶性肿瘤细胞糖酵解同样活跃,表现为葡萄糖摄取率高,代谢产物乳酸含量高。因此,癌细胞的发生、生长和转化可以有线粒体氧化磷酸化和糖酵解两条途径来提供养分和能量。肿瘤细胞具有在两种能量代谢方式之间进行切换的能力,即代谢易变性,从而对化疗药物产生耐药性。针对肿瘤细胞能量代谢这一特点,可以设计一些新型铂类配合物,为克服肿瘤细胞对顺铂的耐药性提供有效方案。于是他们合成了一种能靶向线粒体的三联吡啶铂配合物(TTP),通过对线粒体和细胞质中硫氧还蛋白还原酶(TrxR)的抑制,破坏细胞内氧化还原稳态,损伤线粒体形貌和功能,同时抑制线粒体氧化磷酸化和糖酵解两条能量代谢途径,降低肿瘤细胞的整体代谢水平,最终达到抑制肿瘤细胞增殖、克服细胞耐药性的目的。化合物TTP的作用机理如图1所示,主要实验结果如图2所示。
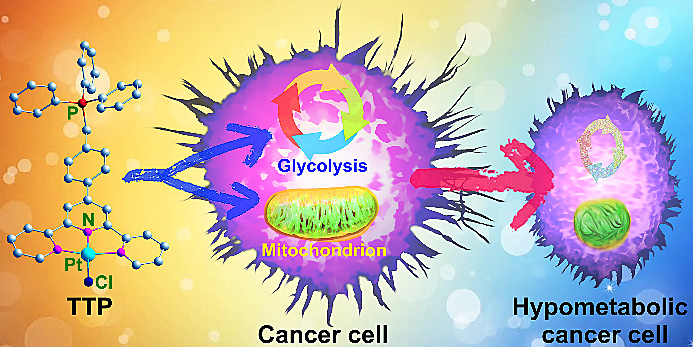
图1. TTP作用机理示意图
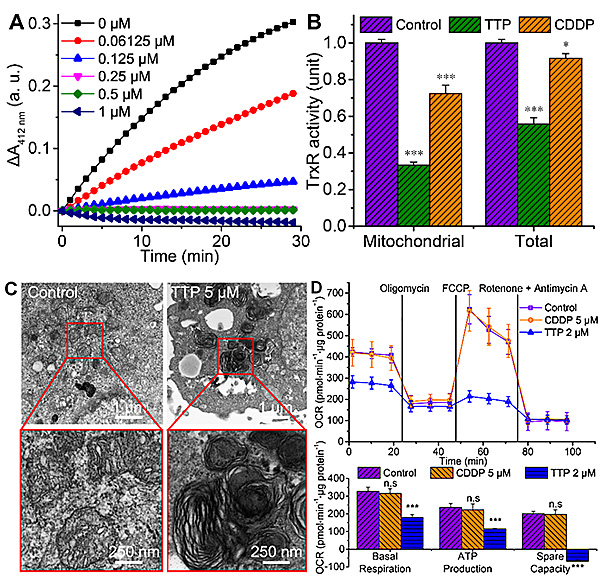
图2.(A)TTP对纯化TrxR蛋白的抑制,(B)TTP对细胞和线粒体TrxR蛋白的抑制,(C)TTP对线粒体形貌的影响,(D)TTP对线粒体能量代谢的影响。
该工作发表在Angew. Chem. Int. Ed. [1],南京大学化学化工学院博士生王坤为第一作者,王晓勇教授和郭子建院士为通讯作者。
(二)铂配合物通过干预多种遗传和代谢途径抑制肺癌
传统观点认为,细胞核DNA(nDNA)是铂类抗肿瘤药物的主要作用靶点。由于细胞内存在nDNA损伤修复机制,铂类药物对nDNA的损伤容易被修复,使肿瘤细胞产生耐药性。线粒体中含有环状线粒体DNA(mtDNA),是动物细胞内除了nDNA外唯一的遗传物质。mtDNA由于缺乏组蛋白保护和相对较弱的损伤修复能力,它更容易受到损伤,可以成为铂类药物潜在的作用靶点。因此将铂类配合物靶向mtDNA可能会影响肿瘤细胞的能量代谢和生存能力,克服传统铂类抗肿瘤药物的耐药性问题。最近该研究团队设计了一系列具有线粒体靶向功能的吡啶衍生物铂配合物(图3),并从DNA损伤、能量代谢和构效关系等角度研究了它们的抗肿瘤作用机理。其中,N-邻位取代的配合物OPT对A549肺癌细胞增殖具有明显的抑制活性,对正常细胞毒性较低;而且,OPT对人肺癌裸鼠移植模型表现出显著的治疗效果(图4)。

图3. 吡啶衍生物铂配合物的作用示意图。
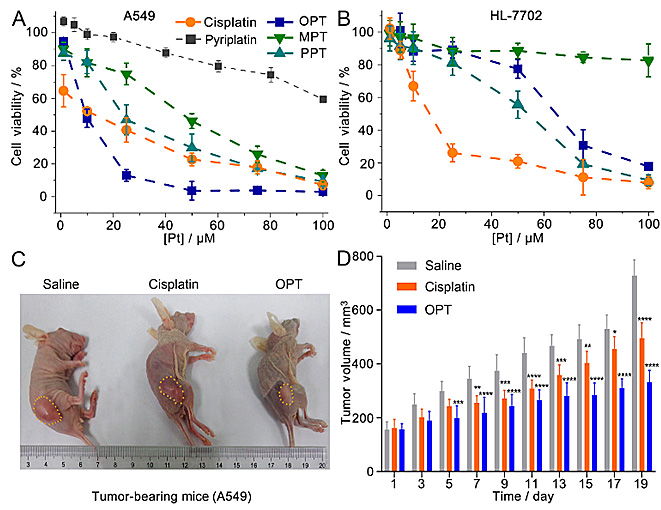
图4. OPT对A549肺癌细胞(A)和HL-7702正常肝细胞(B)的细胞毒性,以及对人肺癌裸鼠移植模型的治疗效果(C, D)。
研究发现,OPT一方面与nDNA和mtDNA结合形成Pt-DNA单加合物,使DNA构象发生改变,不能正常复制,并损伤mtDNA控制区基因;另一方面抑制肿瘤细胞糖酵解,影响线粒体结构和功能,致使线粒体氧化磷酸化和三羧酸循环过程不能正常进行(图4)。这种同时干预DNA复制和能量代谢途径的作用机制与现有铂类药物的作用机理完全不同。
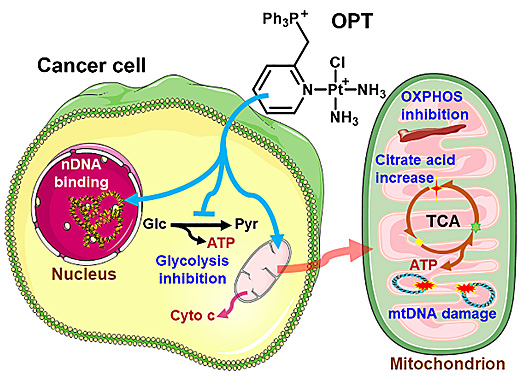
图5. OPT抑制肿瘤细胞的不同途径。
该工作发表在Chem. Sci. [2],南京大学生命科学学院全国“博士后创新人才支持计划”入选人朱珍珠博士为第一作者,王晓勇教授和郭子建院士为通讯作者。
1. 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Restraining Cancer Cells by Dual Metabolic Inhibition with a Mitochondrion-Targeted Platinum(II) Complex
Kun Wang, Chengcheng Zhu, Yafeng He, Zhenqin Zhang, Wen Zhou, Nafees Muhammad, Yan Guo, Xiaoyong Wang, Zijian Guo
Angew. Chem. Int. Ed., 2019, 58, 4638‒4643, DOI: 10.1002/anie.201900387
2. 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Mitochondrion-targeted platinum complexes suppressing lung cancer through multiple pathways involving energy metabolism
Zhenzhu Zhu, Zenghui Wang, Changli Zhang, Yanjun Wang, Hongmei Zhang, Zhenji Gan, Zijian Guo, Xiaoyong Wang
Chem. Sci., 2019, 10, 3089‒3095, DOI: 10.1039/c8sc04871a
导师介绍
郭子建
https://www.x-mol.com/university/faculty/11597
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号