手性双氮氧-镍配合物催化的Diels–Alder反应:高立体选择性合成酰胺环己基螺环吲哚酮
手性路易斯酸金属络合物催化的不对称Diels–Alder反应是构建手性六元环化合物最有效的方法之一,由于合成的多样性,人们不断将这类反应应用到生物活性分子和天然产物的合成中。虽然该类方法已经发展得比较成熟,但含有季碳手性中心以及连续手性中心的六元环化合物的构建仍存在着挑战。
手性酰胺环己基螺环吲哚酮具有独特的生物活性及潜在药用价值。但是到目前为止,还没有合成该类化合物的不对称催化反应报道。近期,四川大学的冯小明教授(点击查看介绍)、林丽丽教授(点击查看介绍)及其合作者成功地实现了手性双氮氧-镍配合物催化的Diels–Alder反应,高立体选择性合成了酰胺环己基螺环吲哚酮。
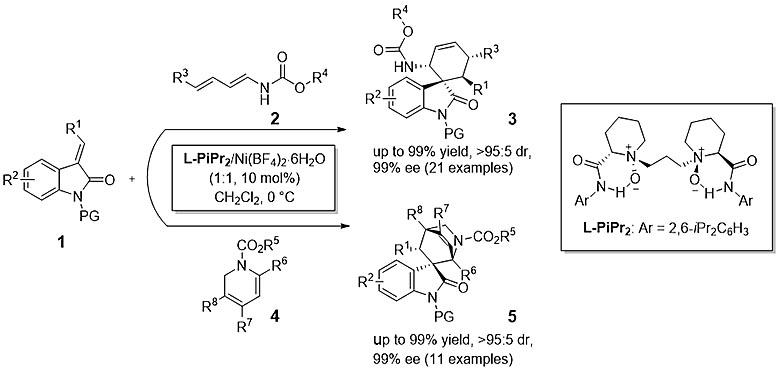
为构建目标化合物,作者选择具有吲哚酮骨架的底物1作为亲双烯体,拥有酰胺基团的底物2作为双烯体进行反应。经过条件筛选,作者发现在配体L-PiPr2及金属盐Ni(BF4)2·6H2O生成的配合物的催化下,该反应能得到理想的结果,且底物普适性好,不同取代基的底物1与2都能够很好地兼容。
在同一催化体系下,当链状双烯2被替换为环状1,2-二氢吡啶4时,构建得到具有四个连续手性中心且带有桥环的螺环吲哚酮化合物5。
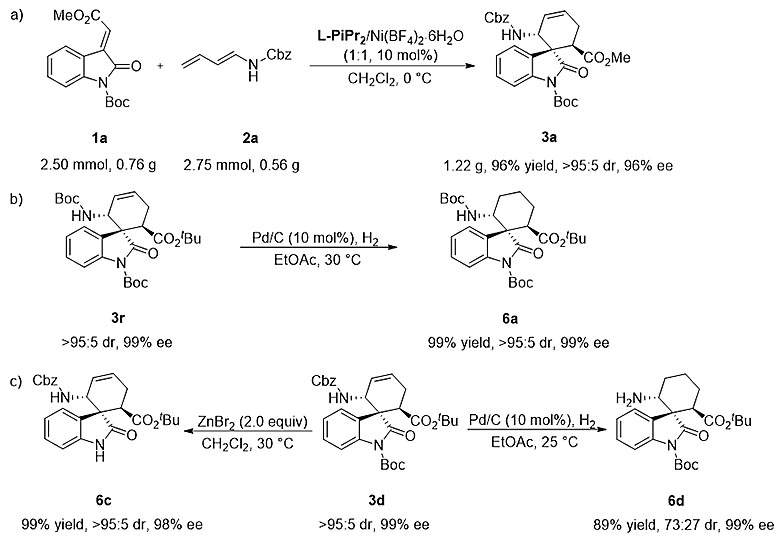
与此同时,该催化体系可进行克级规模的放大,反应活性和选择性均不会受到明显的影响。在合适的反应条件下,产物通过进一步衍生化可以还原产物的双键以及选择性消除不同氨基的保护基。
该论文作者为:Yuhang Zhou, Yan Lu, Xinyue Hu, Hongjiang Mei, Lili Lin, Xiaohua Liu, Xiaoming Feng
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Highly diastereo- and enantioselective synthesis of spirooxindole-cyclohexaneamides through N,N'-dioxide/Ni(II)-catalyzed Diels‒Alder reactions
Chem. Commun., 2017, 53, 2060-2063, DOI: 10.1039/C6CC10125A
导师介绍
冯小明
http://www.x-mol.com/university/faculty/12766
林丽丽
http://www.x-mol.com/university/faculty/12812
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号