5-exo环化:七元环内酯的自由基环化
寻找新的途径完成具有挑战的分子骨架的合成可以很好地促进有机合成化学的发展。由于具有非常高的环张力,八元环烷烃虽然是很多天然产物和药物分子的核心骨架,但是高效合成八元环也确实很有挑战。在著名的天然产物紫杉醇的全合成研究中,其八元环骨架的构建受到了广泛的关注。在这些反应中,只有少数文献通过卤素、醛、酮等化合物形成自由基,进行8-endo自由基关环来构造八元环(Scheme 1A)。最近,来自英国曼彻斯特大学的David J. Procter教授(点击查看介绍)课题组报道了通过七元环内酯的自由基环化反应制备八元碳环化合物。(Selective Synthesis of Cyclooctanoids by Radical Cyclization of Seven-Membered Lactones: Neutron Diffraction Study of the Stereoselective Deuteration of a Chiral Organosamarium Intermediate. Angew. Chem. Int. Ed., 2016, 55, 12499-12502, DOI: 10.1002/anie.201606792)

Scheme 1 八元环合成策略。图片来源:Angew. Chem. Int. Ed.
作者首先以内酯1a(R1 = Me; R2 = Ph; R3= H)作为模板底物进行条件筛选(Table 1)。如之前推测的一样,1a与SmI2在THF中并无反应发生,但加入额外的H2O后,有产物生成,最终H2O的添加量为800 equiv时,可以高收率的分离得到1,4-环辛二醇2a,2a经过Dess-Martin试剂氧化后可以得到3a,总分离产率达到72%。对于7-甲基取代的底物,与双键共轭的芳环上取代基的位置对于反应都没有影响,均可以得到较高的收率和对映选择性。但是当双键共轭的芳环被烷基取代时,收率会明显降低(3i、3k)。该反应对于空间位阻较大的底物也有很好的容忍性:α-位偕二甲基取代的内酯1j,也能够在SmI2-H2O体系中进行自由基关环反应,并且该产物经过DMP氧化后得到羟基酮产物3j。7位苄基取代的底物也有很好地收率,但是当7位没有取代基时,1,4-环辛二醇2o、2n的也只能得到中等收率。

Table 1 底物普适性研究。图片来源:Angew. Chem. Int. Ed.
有趣的是,将1a放入 SmI2-D2O体系中反应,可以以较高的对映选择性得到苄基为D代的产物d-3a(> 90:10 d.r.)。通过的d-3a晶体结构以及中子衍射实验,作者提出了可能存在的鳌和手性有机钐物种,1a与SmI2反应得到芳环和八元环位于同侧的手性SmIII中间体syn-IV,其可以快速的转变为较为稳定的反式中间体anti-IV,IV与Sm相连C上的H发生分子内重氢交换,生成SmIII醇盐V,最终得到d-3a。这也是首次报道的通过中子衍射实验证实含有重氢的对映异构体。
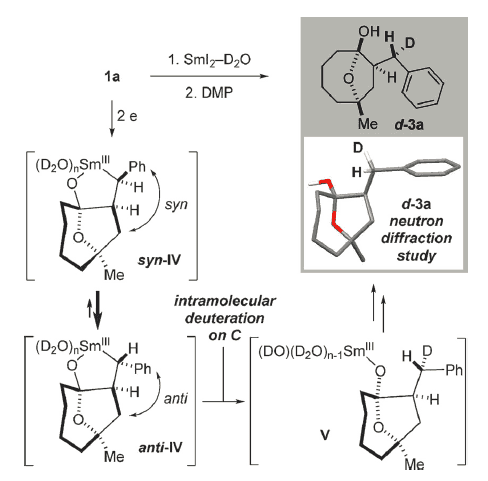
Scheme 2 中子衍射实验:手性有机钐。图片来源:Angew. Chem. Int. Ed.
小结:
Procter课题组首次报道了七元环内酯在SmI2-H2O体系中发生自由基5-exo环化反应,以高收率对映选择性地合成八元环。通过中子衍射实验,首次证明了通过手性有机钐中间体进行的不对称重氢交换反应。
http://onlinelibrary.wiley.com/doi/10.1002/anie.201606792/abstract
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!








































 京公网安备 11010802027423号
京公网安备 11010802027423号