靶向新型检查点Siglec-15的核酸适体免疫治疗策略
近日,厦门大学化学化工学院宋彦龄教授(点击查看介绍)领导的研究团队提出了一种针对唾液酸结合免疫球蛋白样凝集素-15(Siglec-15)的免疫治疗新策略。该策略利用核酸适体封闭免疫检查点Siglec-15,展现了在癌症治疗中的巨大潜力。相关研究成果已在Angewandte Chemie International Edition 杂志发表。
在癌症治疗领域,免疫治疗特别是免疫检查点阻断疗法已成为一种重要的治疗策略。通常该疗法能激活T细胞,促进肿瘤微环境中的抗肿瘤免疫反应。尤其是PD-1/PD-L1阻断策略,在多种癌症治疗中显示出显著的临床效果。然而,由于肿瘤的高异质性和复杂的免疫逃逸机制,这些疗法的总体响应率仍然较低。因此,探索新的免疫检查点和开发相应的创新疗法显得尤为重要。2019年,免疫学家陈列平发现了Siglec-15有望作为一种新的免疫检查点,其在多种癌细胞和肿瘤相关巨噬细胞中表达上调,且与PD-L1表达互斥,表明两者可能通过不同的免疫抑制机制。
基于这一发现,宋彦龄教授团队开发了一种基于核酸适体的新型免疫检查点阻断(Ap-ICB)策略,用于阻断这种免疫检查点Siglec-15与T细胞间的互作(图1)。与传统抗体疗法相比,这种策略利用核酸适配体,更好的组织渗透性及较低的免疫原性。该研究团队通过适体筛选方法,成功从随机文库中筛选获得系列适体序列。其中,WXY3具有最优的选择性和亲和力,不仅能有效区分Siglec-15阳性和阴性细胞,而且可以区分肿瘤组织和正常组。体外细胞实验表明,WXY3能够解除Siglec-15对T细胞的抑制作用,恢复T细胞增值活性;并在小鼠模型中显著抑制肿瘤生长和远端转移。此外,通过单细胞RNA测序技术揭示了WXY3治疗后肿瘤微环境中巨噬细胞和T细胞功能的显著增强,进一步验证了该种Ap-ICB的免疫学机制。此外,该研究团队还开发了基于WXY3的球形核酸(Ap-SNA),其多价结合和空间阻碍进一步增强了对Siglec-15的阻断效果,展现出更强的抗肿瘤活性。综上,WXY3适体及其衍生物Ap-SNA,为癌症治疗提供了一种新的可能性,特别是对于那些对传统PD-1/PD-L1疗法有抵抗性的病例。
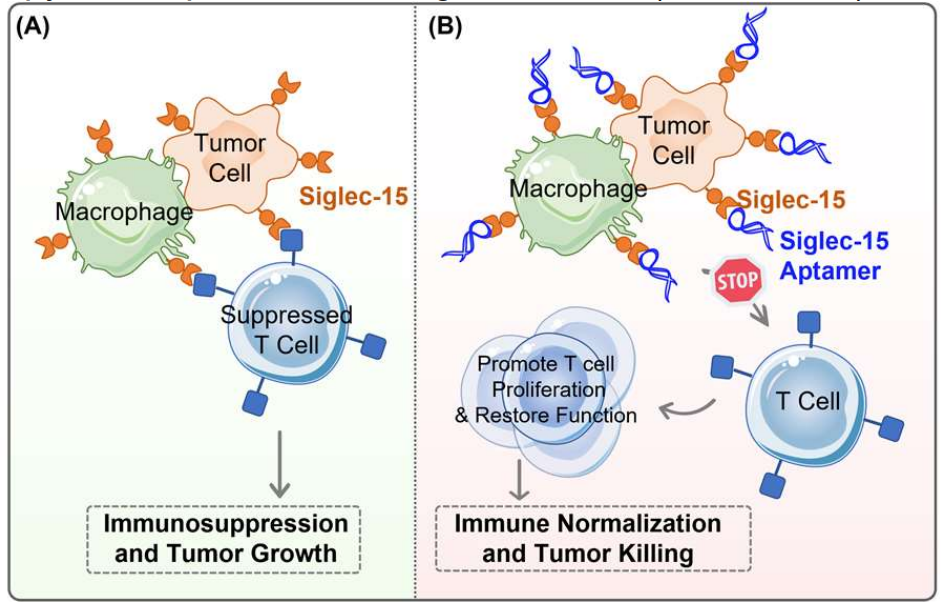
图1. 肿瘤微环境中Siglec-15通路和基于适体的免疫检查点阻断示意图。
该研究由厦门大学化学化工学院2019级博士研究生吴秋月(现任厦门大学博士后)作为第一作者,2019级硕士研究生魏心语为共同第一作者完成。在宋彦龄教授指导下的这项工作主要得到了国家自然科学优秀青年基金(22022409)等项目的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Aptamer-Assisted Blockade of the Immune Suppressor Sialic Acid Binding Immunoglobulin-Like Lectin-15 for Cancer Immunotherapy
Qiuyue Wu#, Xinyu Wei#, Fude Chen, Mengjiao Huang, Suhui Zhang, Lin Zhu, Leiji Zhou, Chaoyong Yang and Yanling Song*
Angew. Chem. Int. Ed., 2023. DOI: 10.1002/anie.202312609
研究团队简介

宋彦龄,厦门大学化学化工学院化学生物学系教授,博士生导师,获基金委优秀青年基金、重大研究计划等项目支持。近年来围绕微流控分析化学,系统性开展了适体筛选、适体结合构效规律、适体微纳界面组装等方面研究。本课题组目前正在招聘具有生物分析、DNA存储、糖化学、免疫学、微流控分析等方面研究背景的博士后,感兴趣的可以联系我们ylsong@xmu.edu.cn。
主页:
https://chem.xmu.edu.cn/info/1415/8098.htm
https://www.x-mol.com/university/faculty/353173
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号