相同底物,不同区域/化学选择性——P450酶IkaD和CftA的结构机理比较研究
惰性C-H键活化是合成高价值化合物的关键环节,主要依靠过渡金属催化,难以控制区域/立体/化学选择性,一度被称为有机化学中的“圣杯”。而在自然界中,少数细胞色素P450酶可以轻松有序地催化多步C-H键活化反应,且具有高度的区域/立体/化学选择性,是许多重要天然产物分子的氧化后修饰来源。这些P450酶被称为多功能P450酶,是合成生物学应用的重要酶元件,但由于解析的复合物晶体结构有限,多步反应和精准选择性的酶学机制仍有待阐明。以ikarugamycin为代表的多环大环内酰胺类天然产物(PoTeMs)是药物先导化合物和生物农药的重要资源。在PoTeMs生物合成中,P450酶介导的后修饰极大丰富了化学结构和生物活性。有趣的是,其中的多功能P450酶IkaD和CftA被报道都天然识别ikarugamycin(1),但得到不同的氧化产物:IkaD先氧化C7=C8双键形成环氧,再羟基化C29,获得产物capsimycin G(1b);而CftA先催化形成C29酮基,再微弱催化C30羟基化反应获得产物clifednamide C(1d)(图1)。
为了揭开P450酶IkaD和CftA催化功能差异的神秘面纱,近日,中国科学院南海海洋研究所张长生研究员(点击查看介绍)团队首先解析了IkaD和CftA与共同底物1的复合结构。发现二者的整体三维骨架基本重合,是典型的金字塔形P450骨架,但参与构成催化口袋的FG区域的构象明显不同,从而影响了催化口袋的形状(图1),使得同一个底物1朝向两个酶血红素铁反应中心的距离和角度不同(图2),最终决定了酶催化反应的区域和化学选择性。基于这一发现,研究团队通过理性设计,对远离血红素铁反应中心的极性氨基酸进行单点突变,发现IkaD的部分突变酶能够改变催化反应的区域选择性,形成新产物。
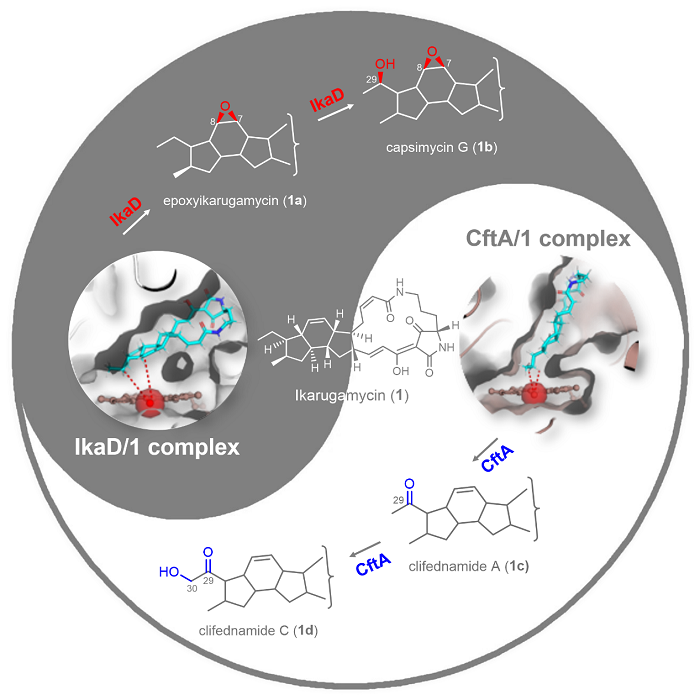
图1. 多功能P450酶IkaD和CftA对相同底物的不同区域/化学选择性及其结构基础
接着,研究团队以不同骨架的PoTeMs底物开展系统的体外酶学测试,发现IkaD和CftA都能识别催化非天然底物,但与区位选择性不同。分别解析IkaD和CftA与非天然底物的复合物晶体结构(图2),发现非天然底物并没有诱导IkaD和CftA发生构象变化,保持了二者FG区域的构象差异,最终决定了对非天然底物的位点选择性和反应顺序。有趣的是,远离血红素铁反应中心的极性氨基酸突变也显著改变了IkaD对非天然底物催化反应的区域选择性。
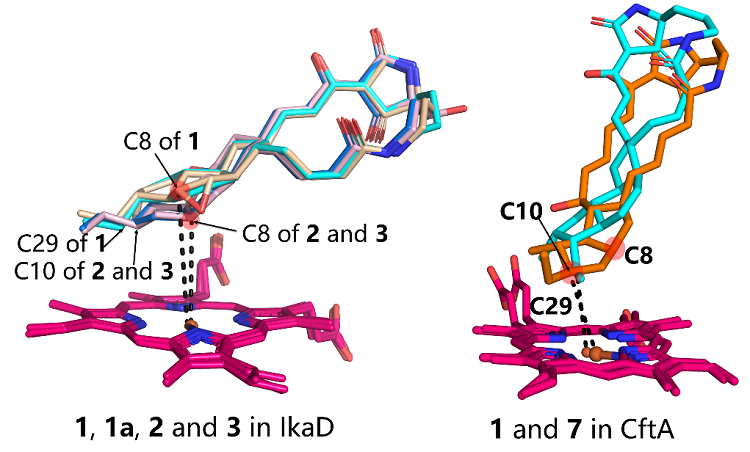
图2. P450酶与不同骨架的PoTeMs底物在IkaD和CftA晶体结构中的结合模式
虽然参与组成P450酶催化口袋的BC和FG区域存在构象变化的现象已经广为人知,本研究首次发现了FG区域的构象差异导致同一底物1在IkaD和CftA催化口袋中以不同的姿势朝向酶反应中心,造成了二者催化反应的区域选择性和化学选择性不同。这些发现为多功能P450酶如何控制位点选择性、反应顺序和反应类型提供了蛋白三维晶体结构方面的解答,并为P450酶理性改造提供了参考,对于认知海洋天然产物生物合成途径和丰富海洋微生物酶元件库具有重要的科学意义。
这一成果近日在线发表于Angewandte Chemie International Edition,蒋鹏博士生和金红波博士后为论文的第一作者,张长生研究员和张丽萍副研究员为共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Mechanistic Understanding of the Distinct Regio- and Chemoselectivity of Multifunctional P450s by Structural Comparison of IkaD and CftA Complexed with Common Substrates
Peng Jiang#, Hongbo Jin#, Guangtao Zhang, Wenjun Zhang, Wei Liu, Yiguang Zhu, Changsheng Zhang*, Liping Zhang*,
Angew. Chem. Int. Ed., 2023, DOI: 10.1002/anie.202310728
研究团队简介
张长生,研究员,博士生导师,中国科学院南海海洋研究所副所长。2002年毕业于德国Wuppertal大学获博士学位,2003-2008年在美国威斯康星大学麦迪逊分校从事博士后研究,2008年3月加入中国科学院南海海洋研究所,致力于海洋微生物天然产物发现、生物合成和创新药物研发研究。在Science、Nat Commun、JACS、Mol Cell、Angew Chem Int Ed、Sci China Chem、Chem Sci等期刊发表论文160余篇;授权专利近40件。2011年获得国家自然科学基金杰出青年基金,2014年入选科技部“中青年科技创新领军人才”、2015年入选“广东特支计划”杰出人才(南粤百杰),2016年入选国家“万人计划”科技创新领军人才,2021年入选英国皇家化学学会会士。获得第四届曾呈奎海洋科技奖-青年科技奖(2016年)。现任期刊Nat Prod Rep编委会成员。
https://www.x-mol.com/university/faculty/280580
张丽萍,副研究员,硕士生导师,2014年于中山大学获博士学位,2015年7月加入张长生研究员课题组,以X-ray蛋白晶体衍射为主要手段解析微生物天然产物生物合成酶结构和分子机制,部分研究结果发表于Nature Communications、Angewandte Chemie和Journal of Biological Chemistry等期刊。主持国家自然科学基金面上项目和青年项目、广东省自然科学基金面上和广州市基础与应用基础研究项目。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号