ACS Cent. Sci. | 重磅突破:北大刘燕/李巍然/谢正伟团队发现抗疟化合物二氢青蒿素有效治疗骨质疏松症
英文原题:Deep Learning-Predicted Dihydroartemisinin Rescues Osteoporosis by Maintaining Mesenchymal Stem Cell Stemness through Activating Histone 3 Lys 9 Acetylation

通讯作者:刘燕、李巍然、谢正伟
作者:王若茜、王禹、牛宇霆、何丹青、金姗姗、李紫昕、朱丽莎、陈丽媛、吴晓岚、丁承叶、吴天昊、史昕萌、张鹤、李畅、王昕、刘燕*、李巍然*、谢正伟*
背景介绍
在健康人群中,成骨细胞与破骨细胞之间的活动保持着平衡,维持着骨骼的健康状态。然而,当“破坏队伍”比“重建队伍”更为活跃时,会导致骨质流失,进而引发骨质疏松症。目前,骨质疏松症的治疗主要侧重于减缓破骨细胞活动;然而,对于成骨-破骨天平的另一端却缺少有效的治疗药物。骨髓间充质干细胞(BMMSC)作为成骨细胞的前体细胞,具有自我增殖及成骨向分化的能力,其功能在骨质疏松的发生发展及疾病治疗中均至关重要,近年来逐渐引起学者的注意。
另一方面,人工智能(AI)的崛起为药物研发带来了新的机遇。科学家们开始利用人工智能技术分析多种疾病的基因表达差异,从而推测可能的有效药物。目前人工智能已在癌症、神经系统疾病、传染病、心血管疾病等多个疾病的药物筛选中发挥重要作用,加速了治疗方法的发现和药物研发过程,而在骨质疏松症的药物开发中尚无相关探索。这一新兴的研究领域为寻找骨质疏松的治疗策略提供了新的思路和工具。
文章亮点
1
恢复受损的BMMSC功能对骨质疏松的治疗至关重要。利用基于深度学习的药效预测系统,我们发现二氢青蒿素(DHA)有望挽救受损BMMSC的干性及功能。
2
体外传代培养实验及动物实验均验证了DHA通过维持BMMSC干性抑制骨质疏松中的骨丧失。
3
DHA的干性促进作用通过表观遗传调控实现,具体的,DHA通过促进乙酰化酶GCN5的功能促进了组蛋白H3K9乙酰化,从而激活干性及成骨基因表达。
图文解读
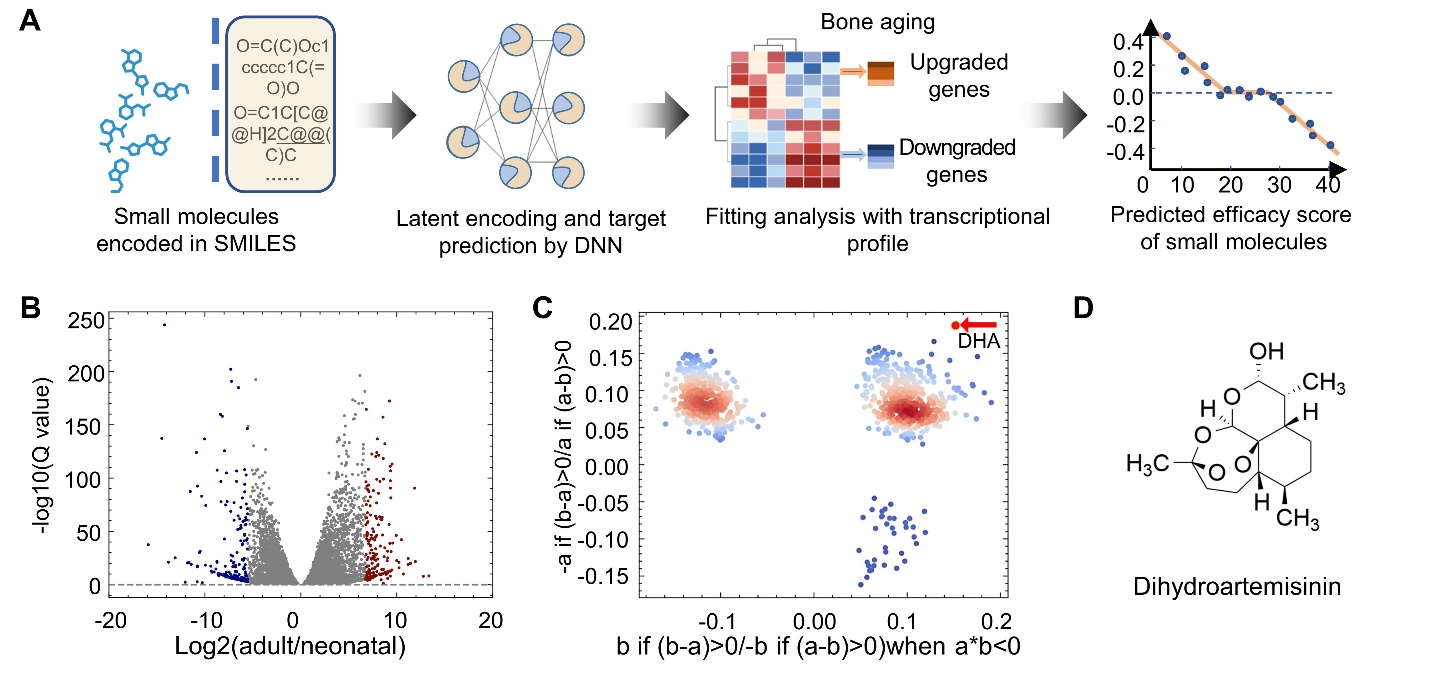
图1. 采用灵素系统(DLEPS)进行小分子药物发掘,根据新生小鼠和成年小鼠骨骼转录谱变化(B)进行小分子药物对干细胞功能影响评分预测(C)。
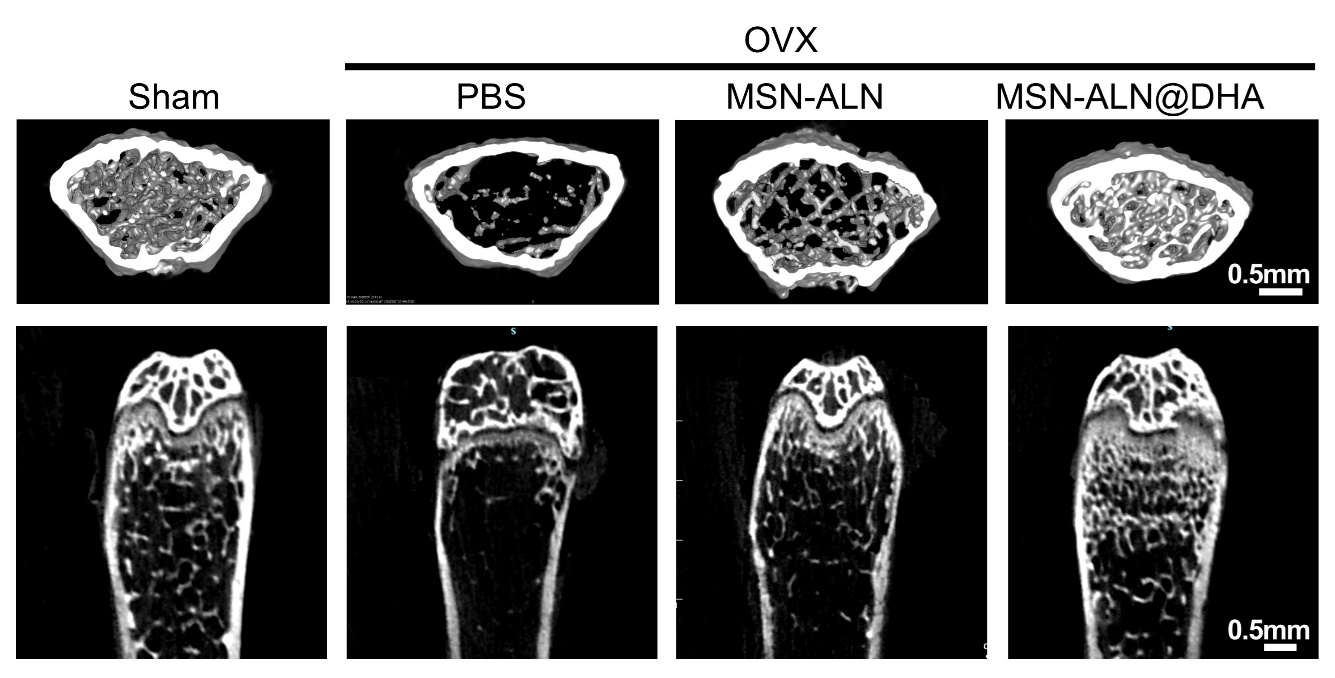
图2. DHA治疗有效抑制骨质疏松骨量丧失。MSN-ALN为骨靶向纳米载体。
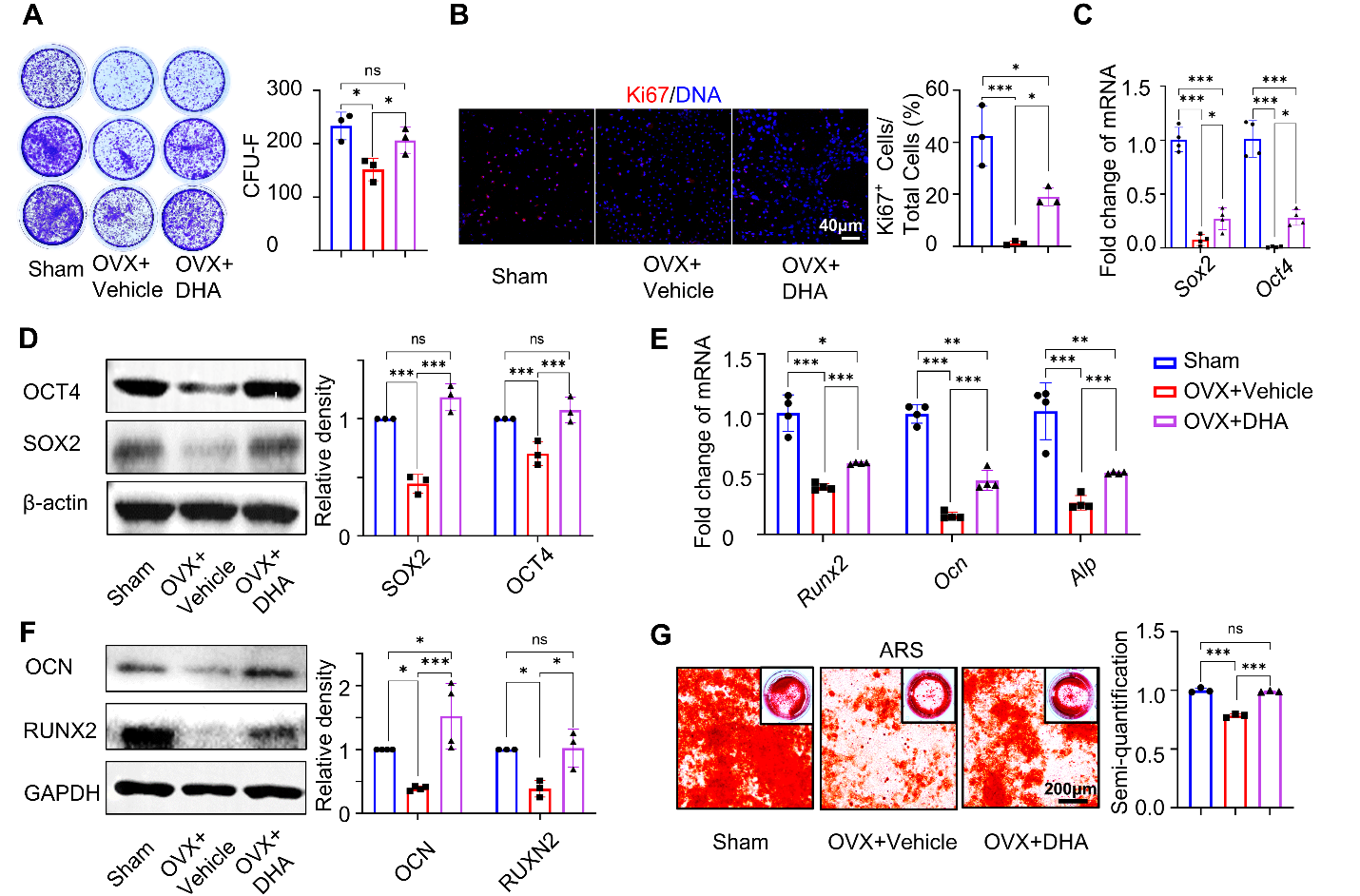
图3. DHA治疗有效促进骨质疏松小鼠BMMSC干性基因SOX2、OCT4及成骨基因RUNX2等表达 (C-F),并促进细胞的增殖分化及成骨能力(A、B、G)。
总结与展望
人工智能技术在医学领域的快速发展,其在药物开发和疾病治疗中的前景广阔。深度学习及对骨髓间充质干细胞(BMMSC)的深入研究将为骨相关疾病的精准干预提供基础,进一步提升治疗效果。此外,随着对骨质疏松症发病机制认识的深化,我们有望突破传统治疗局限,从根源上遏制疾病进程。基于人工智能的药物研发及生命科学研究将为患者提供更加有效、更精准的治疗方案,极大地改善生活质量,具有重要科学及临床价值。
通讯作者信息

刘燕,教授
orthoyan@bjmu.edu.cn
北京大学口腔医学院
中国北京

李巍然,教授
weiranli@bjmu.edu.cn
北京大学口腔医学院
中国北京

谢正伟,研究员
xiezhengwei@ bjmu.edu.cn
北京大学医学部国际癌症研究院
中国北京
扫描二维码免费下载全文

ACS Cent. Sci. 2023, ASAP
Publication Date: October 18, 2023
https://doi.org/10.1021/acscentsci.3c00794
Copyright © 2023 The Authors. Published by American Chemical Society

ACS Central Science是ACS最具包容性的交叉学科期刊,发表以化学为中心的多学科领域最前沿,最重要的研究成果。旨在为全球学者提供交流平台,文章即时发表,全球免费获取,作者也无需付费。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号