南京大学宋玉君教授团队Angew:可基因编辑的生物正交纳米平台实现巨噬细胞吞噬肿瘤
巨噬细胞的吞噬功能在抵抗外来入侵的异物与病原体中起着重要的作用,类似地,肿瘤相关巨噬细胞(TAMs)的吞噬功能在吞噬肿瘤细胞和抑制肿瘤生长方面也拥有巨大的潜力,那么要如何挖掘这一潜力并充分地使TAMs发挥出来呢?
近日,南京大学现代工程与应用科学学院宋玉君教授(点击查看介绍)团队开发了一种可基因编辑的钯生物正交纳米平台,并结合抗肿瘤前药alloc-DOX,用于提高TAMs抗肿瘤吞噬功能,使TAMs能够轻松地“吃掉”肿瘤细胞,实现巨噬细胞对肿瘤的吞噬杀伤,为肿瘤治疗提供了一条新的思路。
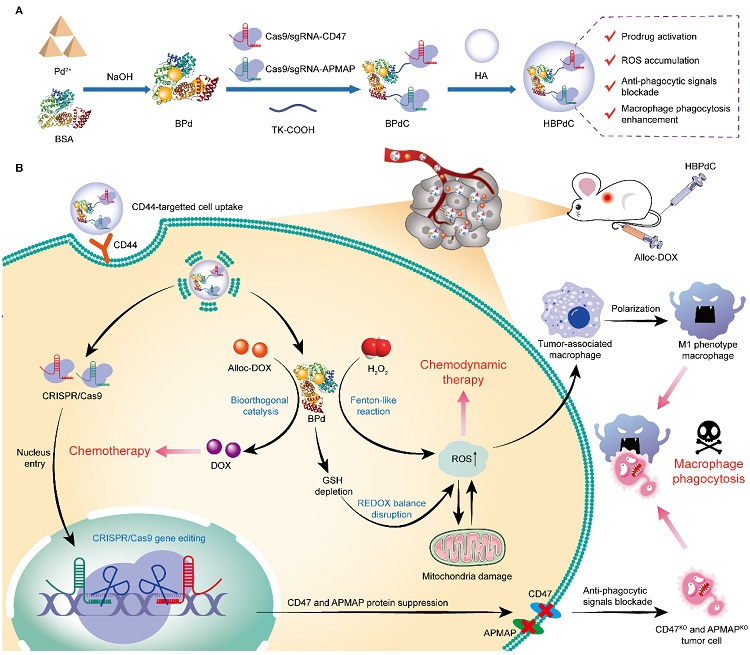
众所周知,肿瘤微环境中的TAMs主要表现为免疫抑制的M2表型,往往会导致肿瘤细胞的增殖和扩散。同时,肿瘤细胞表面抗吞噬信号蛋白的过表达使其能够逃避TAMs的吞噬机制,导致巨噬细胞吞噬失败,使治疗效果大打折扣。
为此,作者将可代谢的钯簇与CRISPR/Cas9进行有效连接,并在表面修饰靶向材料,实现对肿瘤细胞的精准给药。当药物到达肿瘤细胞后,钯簇诱导的类芬顿催化反应促进活性氧的累积,用于化学动力学治疗及TAMs的M1极化。同时,钯簇诱导生物正交催化反应,激活抗肿瘤前药alloc-DOX,用于化疗。此外,CRISPR/Cas9对肿瘤细胞进行重编程,抑制表面抗吞噬蛋白CD47和脂肪细胞膜关联蛋白的表达,大大提高了巨噬细胞的吞噬效率,从而抑制肿瘤细胞的增殖与转移。
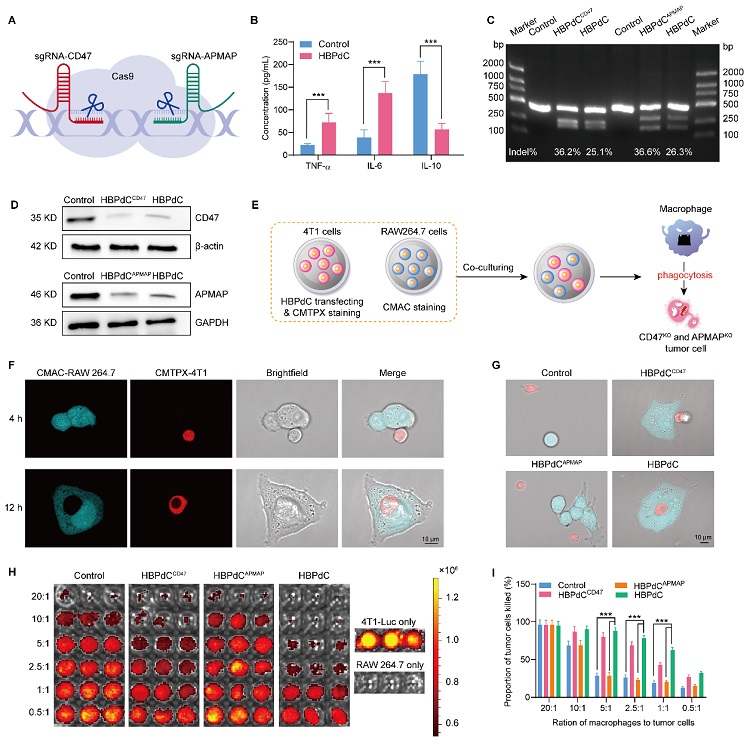
值得注意的是,作者使用该平台对肿瘤细胞进行了两段基因的改造,除了与SIRPα受体结合的CD47这一经典靶点外,还对肿瘤细胞内脂肪细胞膜关联蛋白(APMAP)的基因进行敲除,更好地对肿瘤细胞发出的抗吞噬信号进行阻断,实现协同提高巨噬细胞吞噬功能,达到抑制肿瘤的目的。
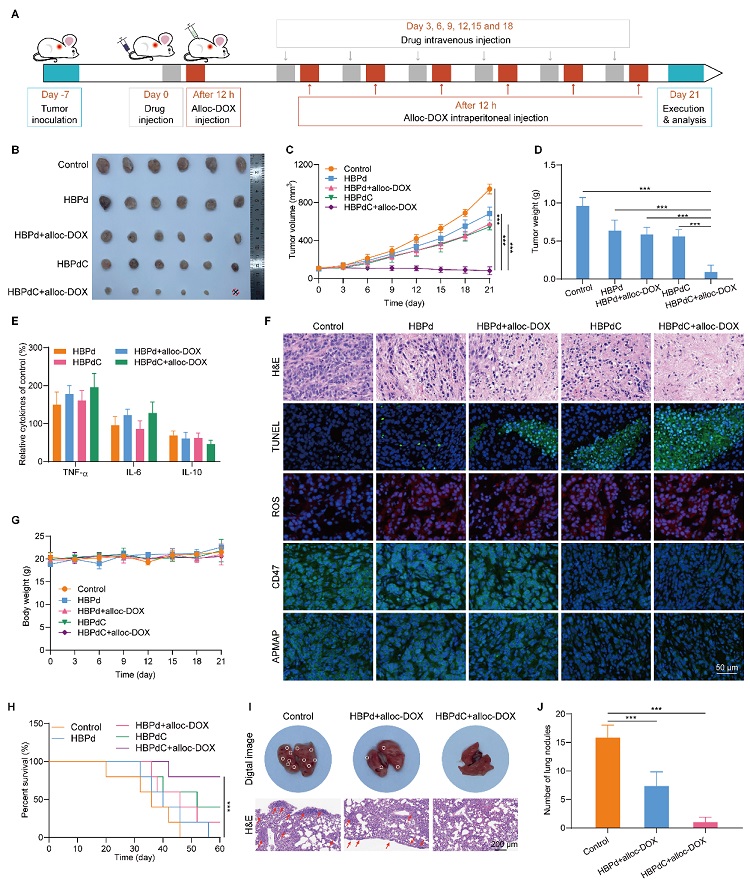
在小鼠体内药效学研究中,该纳米平台表现出优异的抗肿瘤效果,并有效抑制肿瘤转移率,延长生存期,具有较高的临床转化潜力。
小结
在该工作中,作者构建了一种可基因编辑的钯生物正交纳米平台,通过重编程肿瘤细胞,实现巨噬细胞吞噬功能的激活与改善,使其能够轻松“吃掉”肿瘤。该研究对于基因编辑介导的巨噬细胞吞噬疗法具有重要启发并提供了新思路。
文章的第一作者是南京大学现代工程与应用科学学院博士研究生冯淑君、南京理工大学化学与化工学院张宇博士和南京大学现代工程与应用科学学院高彦峰博士,文章的通讯作者是南京大学现代工程与应用科学学院宋玉君教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Gene-Editable Palladium-Based Bioorthogonal Nanoplatform Facilitates Macrophage Phagocytosis for Tumor Therapy
Shujun Feng, Yu Zhang, Yanfeng Gao, Yuta Liu, Yanyi Wang, Xin Han, Tao Zhang, Yujun Song
Angew. Chem. Int. Ed., 2023, DOI: 10.1002/anie.202313968
导师介绍
宋玉君
https://www.x-mol.com/groups/song_yujun
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号