锰配合物诱导DNA损伤有助于激活cGAS-STING信号通路
环磷酸鸟苷-腺苷合成酶(cGAS)-干扰素基因刺激因子(STING)是体内感受细胞质DNA的重要信号通路。激活cGAS-STING通路能影响下游一系列免疫相关事件,如刺激和募集TANK-结合激酶1(TBK1)和干扰素调节因子3(IRF3)、诱导I型干扰素(IFN-I)、促炎因子IL-6和TNF-α的分泌和释放、促进树突状细胞(DC)成熟和迁移、交叉启动肿瘤特异性T细胞等,由此可以调节先天及适应性免疫反应。由于该通路在抗肿瘤免疫中发挥重要作用,因此是肿瘤免疫治疗的重要靶点。
锰是人体内重要的微量元素,参与许多生理过程。新近研究表明,Mn2+可以增强cGAS的灵敏度,并触发第二信使cGAMP的产生,从而增强STING和cGAMP之间的亲和力。然而,激活cGAS-STING通路需要高剂量的Mn2+,但是高浓度的Mn2+会引起神经毒性和心血管毒性,所以其医学应用受到很大限制。锰配合物具有较高的生物稳定性和惰性,可以降低游离Mn2+的系统毒性,使其治疗肿瘤的潜力得以充分发挥。
南京大学王晓勇教授(点击查看介绍)研究团队最近报道了两种多功能锰(II)配合物MnPC和MnPVA(图1),其中1,10-邻菲啰啉(P)作为DNA嵌入剂有利于DNA损伤,丙戊酸(VA)作为组蛋白去乙酰化酶(HDAC)抑制剂可阻碍DNA损伤修复,它们与锰形成配合物可以加强DNA损伤效果,并激活抗肿瘤免疫反应,实现以化学免疫机制治疗肿瘤的目的。
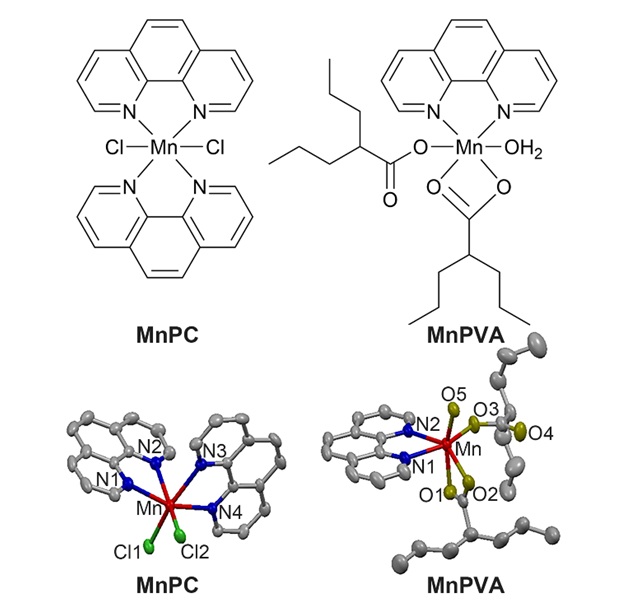
图1. MnPC和MnPVA的化学结构和晶体结构
一方面,MnPC和MnPVA通过嵌入和氧化作用损伤细胞核或线粒体DNA,而且作为HDAC和PARP抑制剂阻止DNA损伤修复,从而增强DNA损伤(图2),直接诱导肿瘤细胞凋亡,产生较强的细胞毒活性(表1)。
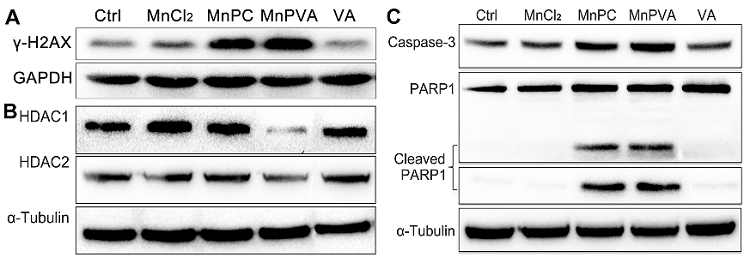
图2. 化合物(6 µM)与MDA-MB-231细胞孵育24 h后细胞内DNA双链断裂标志蛋白γ-H2AX(A)、孵育48 h后细胞内DNA修复相关蛋白HDCA1/2(B)和PARP1(C)的表达。

表1. 化合物对不同细胞的毒性(IC50,µM,72 h)
另一方面,由于MnPC和MnPVA能有效损伤DNA,增加细胞质中DNA片段的含量,从而促进肿瘤细胞和免疫细胞中cGAS-STING通路的激活及下游TBK1和IRF3的上调(图3),启动了固有免疫应答和肿瘤细胞与邻近免疫细胞之间的双向交流。
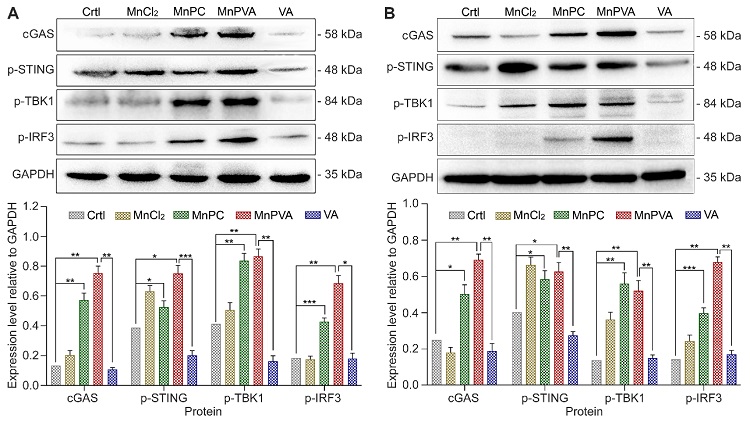
图3. MDA-MB-231细胞(A)和THP-1细胞(B)分别与6 µM和3 µM化合物孵育24 h后cGAS-STING通路相关蛋白的表达及蛋白相对含量。
激活的TBK1和IRF3转位到细胞核,诱导产生IFN、IL-6和TNF-α,它们从细胞核分泌到细胞质和肿瘤微环境中,促进DC和巨噬细胞成熟和抗原提呈,并诱导巨噬细胞由促肿瘤M2表型向抗肿瘤M1表型极化,刺激细胞毒性T细胞(图4)杀伤肿瘤细胞。
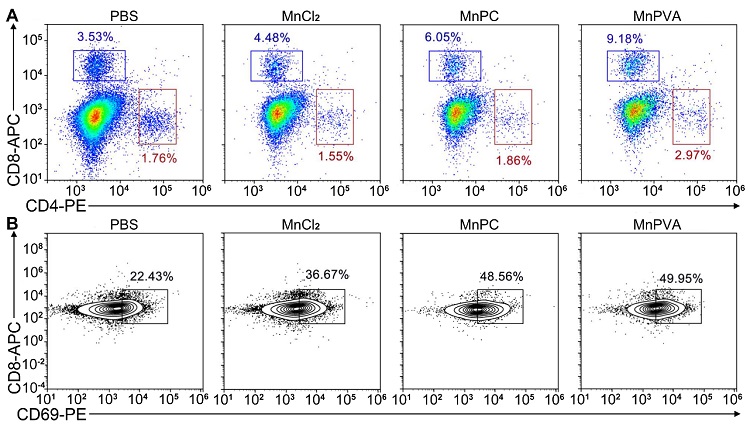
图4. 化合物(1.3 mg Mn kg‒1)治疗4T1荷瘤小鼠16天后,肿瘤组织中CD8+ T(蓝框)和CD4+ T(红框)细胞的表达(A)及CD8+ T细胞中CD69+亚群的表达(B)。
由于1,10-邻菲啰啉和丙戊酸配体使配合物的DNA损伤能力增强,从而提高了MnPC和MnPVA激活cGAS-STING通路的能力,使其表现出比Mn2+更强的免疫活性和抗肿瘤活性,显示出作为肿瘤化学免疫治疗剂的巨大潜力(图5)。
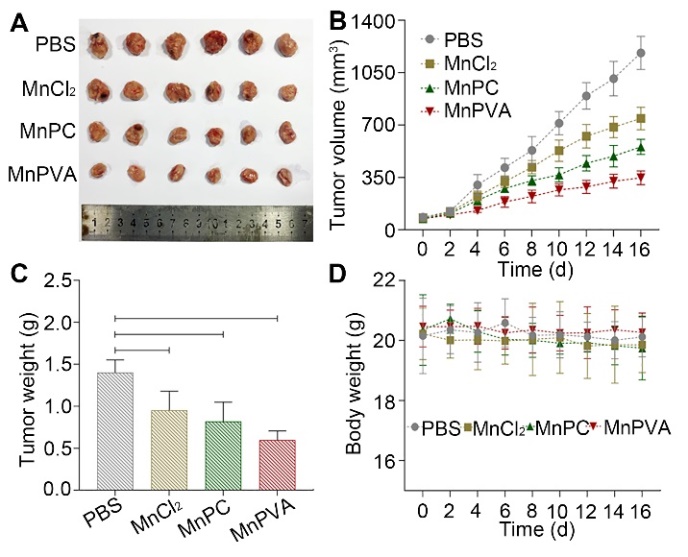
图5. 化合物(1.3 mg Mn kg‒1)对4T1荷瘤小鼠的治疗作用。(A)16天后肿瘤图像,(B)肿瘤体积,(C)肿瘤重量,(D)小鼠体重。
锰配合物不仅通过损伤DNA直接杀死肿瘤细胞,也通过激活免疫反应间接杀死肿瘤细胞,具有化学免疫协同治疗的特点,其作用机制概括如下(图6)。
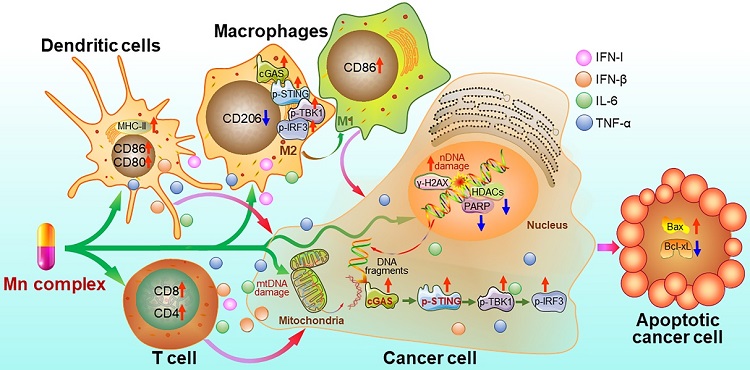
图6. 锰配合物损伤DNA、激活抗肿瘤免疫反应的作用机制
以上结果表明,在肿瘤细胞和免疫细胞中,MnPC和MnPVA对cGAS-STING信号通路的刺激能力远高于MnCl2或Mn2+,因为它们能诱导产生更多的DNA碎片释放到细胞质中,激活cGAS-STING通路。所以,通过构建具有损伤DNA或阻断修复DNA损伤功能的锰配合物可以获得更有效的cGAS-STING激动剂。
该论文发表在Chem. Sci.,第一作者是南京大学生命科学学院博士生蔡林祥,通讯作者是南京大学医药生物技术国家重点实验室王晓勇教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Manganese(II) complexes stimulate antitumor immunity via aggravating DNA damage and activating cGAS-STING pathway
Linxiang Cai, Ying Wang, Yayu Chen, Hanhua Chen, Tao Yang, Shuren Zhang, Zijian Guo, Xiaoyong Wang
Chem. Sci., 2023, 14, 4375–4389, DOI: 10.1039/d2sc06036a
导师介绍
王晓勇
https://www.x-mol.com/groups/Wang_Xiaoyong
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号