Angew. Chem.:自组装、模块化抗体偶联药物MADC平台的构建
抗体偶联药物(ADC)是一类由抗体和具有强效细胞毒性的小分子药物通过生物活性连接子偶联而成的生物治疗药物,该类药物由于兼具特异靶向性和高细胞毒性近年来受到广泛关注。但是由于ADC药物组成较为复杂,含有抗体、连接子、小分子化学毒素多个组成部分,往往存在药物抗体比(DAR)不均一、单一抗体或毒素易产生耐药等问题。因此,克服ADC 药物组分(抗体、毒素)的肿瘤耐药性是提升ADC临床治疗效果面临的关键挑战之一,这需要一个具有高度组合灵活性的 ADC 平台。
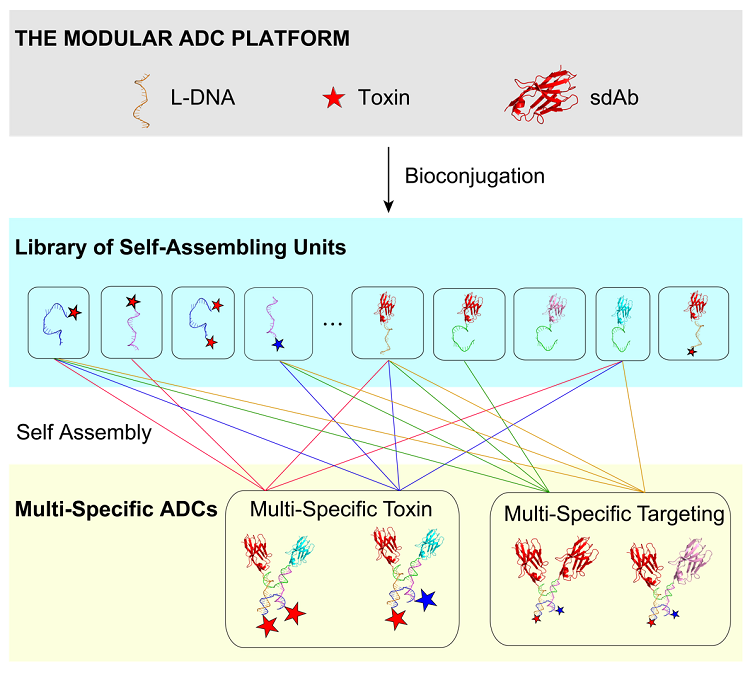
针对以上问题,本文通过化学生物学、人工智能、细胞生物学、药效学多学科的交叉融合,构建了一种自组装、模块化的多特异性抗体偶联药物平台,称为Modular ADC (MADC),并对其在细胞层面及动物体内进行了药效验证。
首先,作者引入镜像核酸作为中心框架以提高其体内稳定性。镜像核酸主要由β-L-脱氧核苷基元组成,与天然右手螺旋D-型DNA镜像对称,该特征使其不被体内核酸酶降解,这为体内稳定提供了前提条件;其次,作者利用化学生物学技术,将修饰后的镜像核酸与抗体蛋白、化学毒素等多个组装单元进行单-位点或双-位点定点偶联,通过条件筛选达到了定量高效偶联;第三,设计镜面对称四聚体核酸自组装框架,使用Metropolis Monte Carlo算法对自组装核酸序列进行优化,使镜像核酸链在溶液里混合后可即时组装成均一的四聚体;最后,作者制备了不同DAR、不同靶向、不同毒素的MADC药物,证明其在细胞及动物体内具有DAR依赖性杀伤作用,并有潜力成为多靶向-多毒素药物的构建与筛选平台。
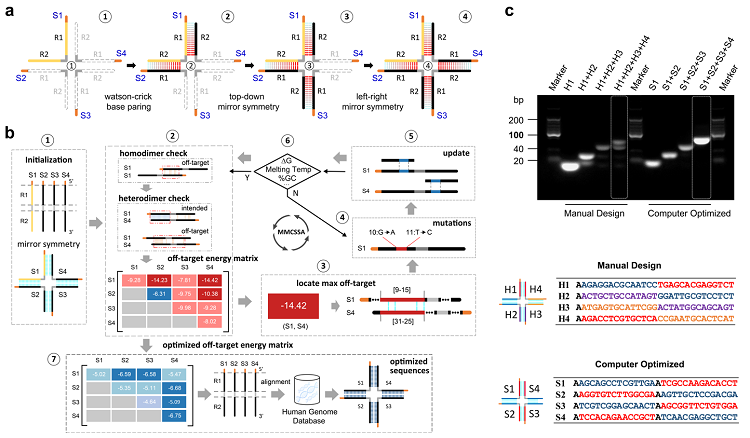
该工作主要有以下三个创新点:1)利用镜像核酸无法被体内核酸酶降解的这一特征实现了体内稳定性,且证明镜像核酸骨架可经代谢安全排出体外;2)巧妙设计镜像核酸自组装框架,人工智能优化自组装核酸序列;3)实现了抗体偶联药物的多靶向或多靶向+多毒素,展现出相较于单靶向抗体偶联药物的优势。
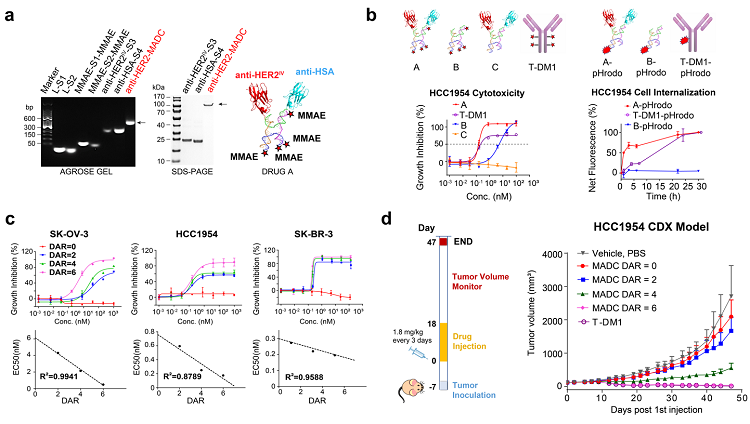
综上所述,该工作发展了一种具有成药潜力的自组装多特异性抗体偶联药物平台,为抗体偶联药物提供了一种可实现多靶向+多毒素及精准控制DAR的新策略。
这一成果近期发表在Angewandte Chemie 上,由南开大学曹婵教授、安升(上海)医药科技有限公司、江西科技师范大学杨凡教授与中国科学院上海有机化学所生物与化学交叉中心周界文教授合作完成。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Self-Assembled L-DNA Linkers for Rapid Construction of Multi-Specific Antibody-Drug Conjugates Library
Liujuan Zhou, Fan Yang,* Zhaoshuai Bai, Xiaohui Zhou, Zhihai Zhang, Zhihang Li, Junyuan Gong, Junqi Yu, Liqiang Pan, Chan Cao,* and James J. Chou
Angew. Chem. Int. Ed., 2023, DOI: 10.1002/anie.202302805
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号