改变PROTAC研发逻辑,李子刚/尹丰团队JACS:分而后合的PROTAC策略
近日,深圳湾实验室坪山中心/北京大学深圳研究生院李子刚/尹丰课题组,在Journal of the American Chemical Society 上发表研究论文,报道了一种创新的多肽自组装Split-and-Mix PROTAC(SM-PROTAC)技术,该技术在多种靶标中均取得了显著的蛋白降解效果,包括ERα、EGFR、MEK1/2、BRD2/4、CDK4/6、AR、BCR-ABL等。
作为一种新兴的蛋白降解技术,靶向蛋白降解技术(Proteolysis targeting chimeras,PROTAC)具有靶向不可成药靶点、克服耐药性等小分子抑制剂不可比拟的潜在优势,正处于快速发展时期。然而,现有的PROTAC底层专利技术主要被发达国家掌握,如何突破现有格局,开发具有自主知识产权的PROTAC技术对于中国生物医药产业的发展至关重要。
本研究以不同生物分子在相互识别后就可以发挥其生物学功能这一现象为出发点,提出了分而后合的PROTAC策略。这种策略基于纳米自组装技术,利用自调节平台筛选配体分子和调节组装过程中的配体比例。与传统小分子PROTAC不同,SM-PROTAC将靶向E3泛素连接酶的配体小分子和靶标蛋白的配体小分子分开成两个模块,然后将二者混合溶解后进行组装。最终组装成直径在50-300 nm范围内的纳米球(SM-PROTAC),该纳米球表面同时含有多个靶向E3配体小分子和多个靶向靶标蛋白的配体小分子,从而招募E3泛素连接酶和靶标蛋白。由于邻近效应,靶标蛋白会被E3泛素连接酶打上泛素标签,从而被蛋白酶体识别并降解。SM-PROTAC不需要费时费力去筛选linker,因此缩短了PROTAC的研发周期。
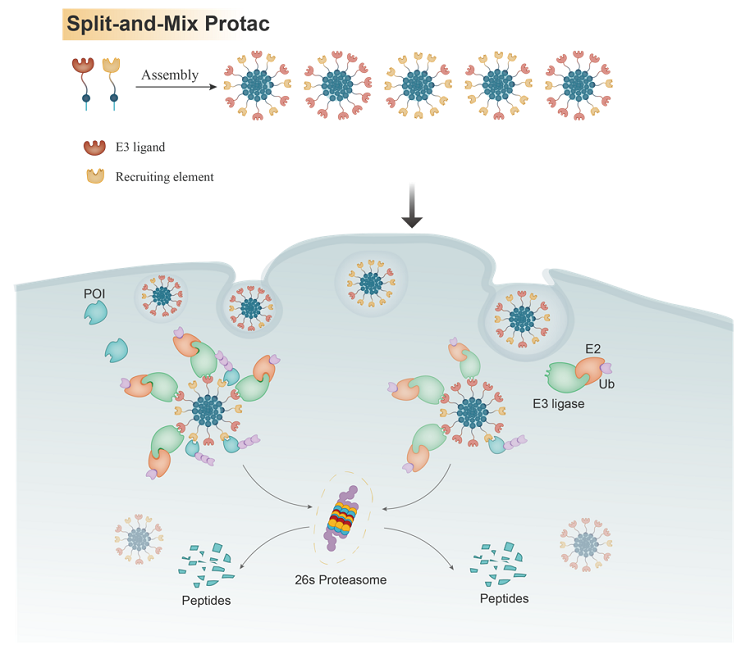
图1. Split-and-Mix PROTAC概念图
SM-PROTAC纳米球表面分布了若干E3配体和POI配体,因此可以同时招募多个E3泛素连接酶和POI蛋白,使得POI蛋白周围会有多个E3泛素连接酶,从而可以被临近的E3泛素酶标记上泛素标签。这省去了传统的小分子PROTAC需要费时费力去筛选linker的过程,从而缩短了开发PROTAC所需的时间。
首先,作者使用二苯基甘氨酸(Phg-Phg)作为模块化E3配体和POI配体的自组装核心二肽基序,该二肽基序可以自组装成球形,然后将其优化为穿膜性更好的δδRR基序。作者将设计的两种自组装模块VHL-δδRR和Br-δδRR混合后组装,使用SEM和EDS验证了这两种自组装模块混合后组装成的同一个纳米球VHL+Br-θθ(1:1)上,会同时含有加入的两种模块VHL-δδRR和Br-δδRR。
接着,作者进行了细胞实验以探索SM-PROTAC的降解效果和降解机制,并在ERα蛋白上验证了VHL+TMXF-θθ(1:1)可以在乳腺癌细胞系T47D和MCF-7中发挥降解功效。对于SM-PROTAC纳米球,由于E3配体和POI配体已经通过连接自组装基序模块化,因此E3配体模块和POI配体模块混合的比例并不局限于1:1,可以变换成n:m(n=1-10,m=1-10),从而形成SM-PROTAC(n:m)去发挥降解蛋白的功效。因此,也组装形成了VHL+TMXF-θθ(n:m)等纳米球,同样可以发挥降解ERα蛋白的效果。
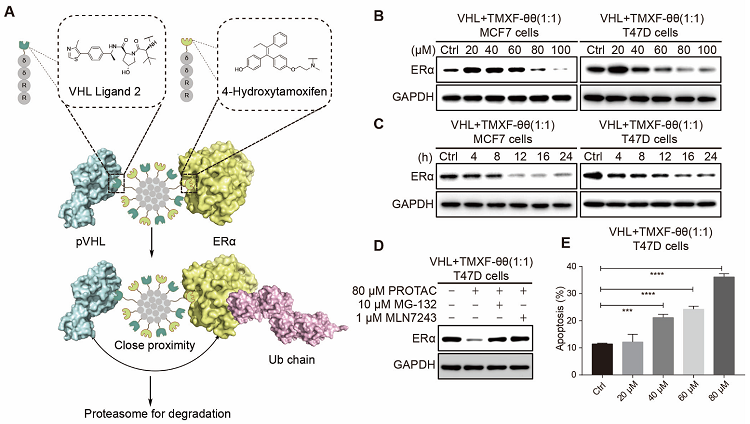
图2. SM-PROTAC VHL+TMXF-θθ(1:1)可以降解ERα蛋白
最后,作者在CDK4/6、AR、EGFR、MEK1/2、BRD2/4、BCR-ABL等多个靶标上进行了细胞实验验证,证明SM-PROTAC平台针对这些靶标都可以发挥降解效果,并验证了SM-PROTAC平台的通用性。作者继续选用CDK4/6靶点进行验证SM-PROTAC的降解活性、降解机制和可调比例能力,并在AR、EGFR、MEK1/2、BRD2/4和BCR-ABL等多个靶标上验证了SM-PROTAC平台的通用性。
SM-PROTAC的目标是作为一个PROTAC平台,为解决PROTAC药物开发中遇到的一些挑战提供新的解决思路,例如快速并有效地筛选靶标蛋白配体、快速筛选E3泛素连接酶配体、扩大PROTAC中E3泛素连接酶的可使用范围,并有助于合理设计传统的小分子PROTAC。在药物研发领域具有广泛的应用前景。分合(Split-and-Mix)纳米平台概念可以应用于其他降解剂体系,例如LYTAC、AUTAC、RIBOTAC等分子,形成SM-LYTACs、SM-AUTACs、SM-RIBOTACs等,以发挥其效用。
总之,这项研究通过将分合纳米平台和多肽自组装技术应用于PROTAC技术中,成功开发了一种新型的药物研发平台SM-PROTAC,具有高效、可靠、节省时间等优点。SM-PROTAC的成功开发对于药物研发具有重要意义,为药物研发提供了一种新的思路。SM-PROTAC可以通过调节配体比例和使用不同的配体模块来实现对不同靶标的靶向,具有更强的通用性和灵活性。李子刚/尹丰课题组在本研究中提出的分合后合的PROTAC策略为中国生物医药产业的发展注入了新的活力,为中国生物医药产业在蛋白降解技术领域的竞争提供了新的机会和优势。
深圳湾实验室坪山中心李子刚/尹丰课题组的阳芬芳(指导老师:李子刚教授/尹丰研究员)和深圳市第二人民医院药学部的罗钦宏博士(指导老师:吴建龙主任)为该论文的共同第一作者,为本文做出贡献的作者还有:北京大学深圳研究生院的王玥琛、王亚琪、侯占峰、万川博士和王跃娜博士,坪山生物医药研发转化中心的梁慧婷、刘志宏博士和叶宇鑫博士,深圳市第二人民医院的朱礼志博士 (药学部) 和吴建龙博士 (药学部主任)。以上工作得到了国家自然科学基金、广东省自然科学基金、深圳市科技创新委员会以及深圳市医学重点学科建设(临床药学)等基金的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Targeted Biomolecule Regulation Platform: A Split-and-Mix PROTAC Approach
Fenfang Yang, Qinhong Luo, Yuechen Wang, Huiting Liang, Yaqi Wang, Zhanfeng Hou, Chuan Wan, Yuena Wang, Zhihong Liu, Yuxin Ye, Lizhi Zhu, Jianlong Wu, Feng Yin*, and Zigang Li*
J. Am. Chem. Soc., 2023, 145, 7879–7887, DOI: 10.1021/jacs.2c12824
李子刚/尹丰团队
研究领域主要包括稳定多肽二级结构的方法学研究、治疗性靶点研究、微生物毒力及抗感染治疗研究、多肽自组装材料研究和免疫医学等四个方面。
研究领域:
1. 稳定多肽二级结构的方法学研究
蛋白-蛋白相互作用 (PPIs) 通常被视为药物发现的非药物性靶点,大多数PPIs包括少于15个氨基酸残基的短螺旋多肽,通过化学手段将多肽稳定在某一固定构象的稳定多肽是重要的调节PPI的代表性化合物。我们课题组的相关研究关注多肽工程战略,致力于发展新型多肽螺旋构象稳定方法,以解释稳定多肽的二级构象对其生物物理性能的影响。与此同时我们通过化学稳定的多肽来研究重要蛋白靶点的生物功能和作用机制,为探索更加有效的药物前体奠定基础。
2. 治疗性靶点研究
基于不同治疗性靶点的特征(ER-α, USP 30, Raf, LSD1, p53, HDAC1, IDE)设计和开发新的稳定多肽。
3. 微生物毒力及抗感染治疗研究
我们课题组一个研究方向是关注人类重要病原微生物的毒力,利用结构生物学或计算化学手段及高通量药物筛选方法对小分子库进行筛选。针对人类病原体重要靶标蛋白开发一些小分子抑制剂用于抵抗病原微生物感染。
4. 多肽自组装材料研究
生物纳米材料相比于许多无机材料更为环境友好。研究发现,许多短肽分子会自组装成规则有序的纳米结构,并常常会展现出许多独特的性质。我们课题组采用化学方法设计与合成具有特殊结构的短肽,开发更为便捷的组装体系,诱导和构建多肽纳米材料。在生物医药、可穿戴设备、植入设备以及可降解材料等领域具有广泛的应用前景。
李子刚课题组主页:
https://scbb.pkusz.edu.cn/info/1015/1012.htm
深圳湾实验室:
https://www.szbl.ac.cn/scientificresearch/researchteam/68.html
深圳湾实验室招聘:
https://www.szbl.ac.cn/careers/recruitment/
深圳湾实验室坪山生物医药研发转化中心招聘:http://www.szbl.ac.cn/careers/recruitment/?unit=10
李子刚博士简介

李子刚博士,2001年本科毕业于中国科技大学,2008 年获芝加哥大学化学系博士学位,2010年获得哈佛大学化学与化学生物学系博士后。2010年回国,获得北京大学“百人计划”特聘研究员称号,目前担任北京大学化学基因组学专业博士生导师、课题组长,深圳湾实验室坪山生物医药研发转化中心执行主任,资深研究员。研究团队致力于化学和生物交叉领域用化学方法解决生物学问题,研究领域包括多肽工程和微生物研究,包括稳定多肽二级结构方法学的构建,多肽药物用于人类重要疾病的研究以及抗病毒多肽的研发。近年来在J. Am. Chem. Soc.、Science Advances、Nature Chemical Biology、Cell Chemical Biology、Proc. Natl. Acad. Sci.、Angew. Chem. Int. Ed. 、J. Med. Chem.、Chemical Science、Cancer research、Chemical Reviews等国际顶级学术期刊发表论文150余篇,研究成果多次入高水平杂志封面,并受到了国际、国内同行的广泛关注。申请专利80余项(10项授权),并于辉瑞制药,拜尔医药保健、罗氏中国等跨国药企开展了多项创新药物新技术的国际合作。
https://www.x-mol.com/university/faculty/17147
尹丰博士简介

尹丰博士于2014年毕业于北京大学细胞生物学专业,在癌症及肿瘤干细胞表观领域进行了深入的研究。2014-2015年间,在新加坡南洋理工大学从事博士后工作,研究癌症靶向的纳米材料递送体系,并且设计和开发了靶向胰腺癌的纳米硅荧光探针和以金纳米棒为基因/抗癌药物双载体的胰腺癌治疗复合物。2016-2017年间,在北京大学深圳研究生院李子刚教授课题组从事博士后工作从事稳定多肽的生物医学研究和多肽递药系统的研究,2017年底任北京大学深圳研究生院副研究员,设计和开发了一系列具有抗癌活性的稳定多肽抑制剂。2019年底任深圳湾实验室研究员,2020年加入深圳湾实验室坪山生物医药研发转化中心担任生物部部长,致力于开发基于稳定多肽的抗癌新药。近五年来,申请专利50余件,授权专利10件,发表国际学术期刊论文70余篇(第一作者及通讯作者的文章40余篇),均发表在国际知名的 学术刊物如Cancer Research、Nano Letter、Material Horizons、Chemical Science、Coordination Chemistry Reviews、Theranostics、Advance Materials、Cell Reports、Chemistry Communication 等。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号