Science:电氧化钴催化,对映选择性C-H键活化
近十年来,电化学方法已成为现代有机合成化学研究的热点并在许多领域中得到了广泛应用。相比多步官能团相互转化的传统方法,与析氢反应(HER)结合的电氧化C-H键活化反应策略无需使用化学计量的氧化剂,对有机化合物的后期转化来说颇有应用潜力(图1A)。但迄今为止,基于电催化开发选择性完全受控的反应,所取得的成功却相对有限。近期才有研究小组通过结合过渡金属催化与电催化实现了对映选择性C-H键活化,通过钯催化实现了电氧化C-H键烯基化和烯丙基化反应,并对映选择性地合成了轴手性联芳基化合物和苯胺。这些方法通常需要昂贵的4d过渡金属催化剂,并且涉及两电子转移过程(图1B)。尽管第一行过渡金属的地球储量丰富,但目前并不能实现对映选择性电催化C-H键活化,该活化涉及单电子转移过程。
近日,德国哥廷根大学的Lutz Ackermann教授(点击查看介绍)课题组利用电氧化钴(Co)催化策略,成功地实现了苯甲酰胺类底物的高化学选择性、区域选择性和对映选择性C-H键环化、N-H(C-H和 N-H串联)键环化以及亚磷酰胺的脱氢C-H键醚化反应,构建了一系列碳中心手性、磷中心手性和轴手性化合物(图1C)。该过程具有以下优势:1)电作为牺牲氧化剂以及质子耦合电子转移的双重作用;2)H2作为唯一的化学计量副产物。值得一提的是,使用成本效益高的不锈钢作为阴极材料同样可以高效催化反应。相关成果发表于Science 上。
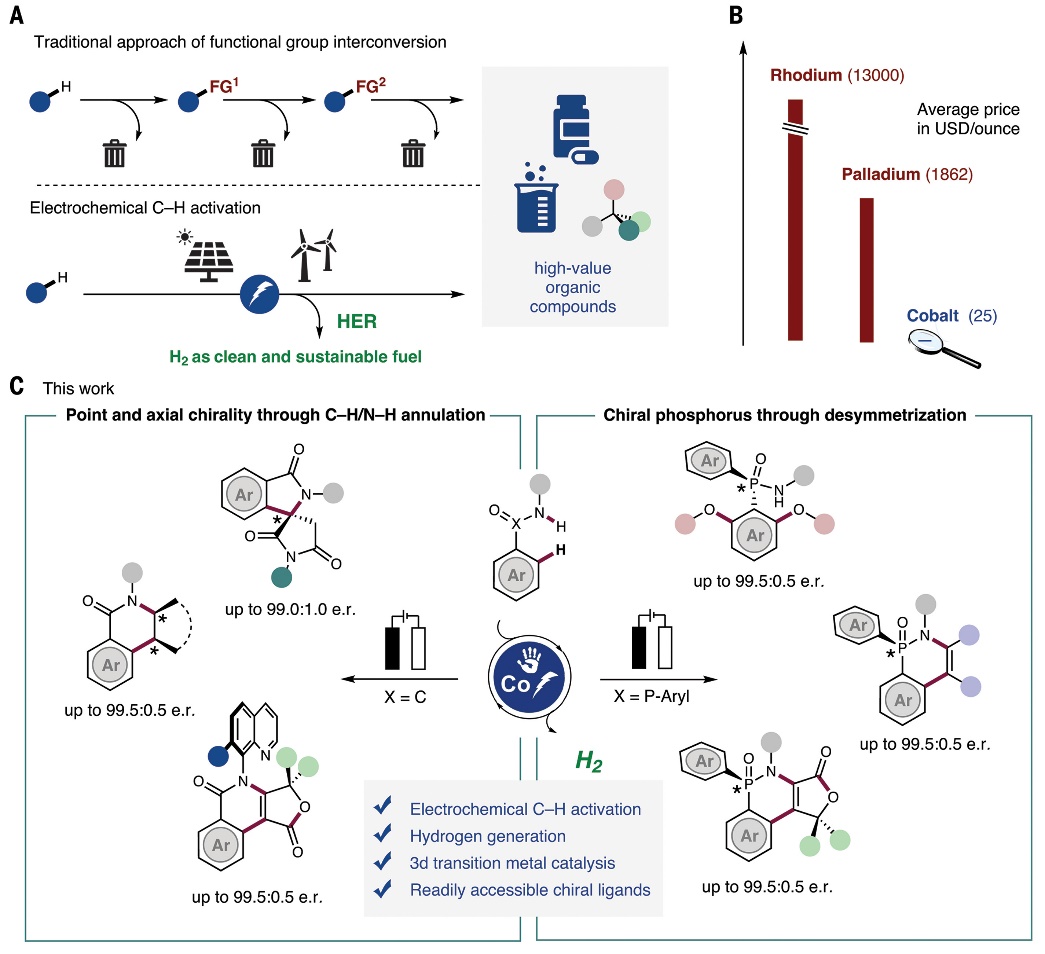
图1. 电化学钴催化C-H键对映选择性活化的价值和策略。图片来源:Science
首先,作者选择苯甲酰胺1和烯烃2为模型底物、乙酸钴(Co(OAc)2•4H2O)和S-BINOL磷酸(CPA1)为催化体系对螺环化反应条件进行了优化(图2A),结果显示在恒电位下可以19%的产率和88:12 e.r.值获得产物3,同时观察到铂电极钝化,这表明需要阴极过电位控制。随后,作者筛选了各种添加剂,发现新戊酸可以在对映选择性保持的情况下显著提高产率,并且通过GC分析检测到分子氢,证实了HER是阴极半反应。此外,更方便的恒电流条件被证明是可行的,没有电流反应无法进行。在最优条件下,作者对底物范围进行了探索(图2C),结果显示苯环上不同吸电子(5、6、9、13、14)、给电子(4、10、11和12)以及易氧化硫醚(8)取代的苯甲酰胺、N原子上不同基团取代的马来酰亚胺(15-20)甚至丙烯酰胺类底物(21-23)均可兼容该反应,以中等的产率和优异的对映选择性获得所需产物。
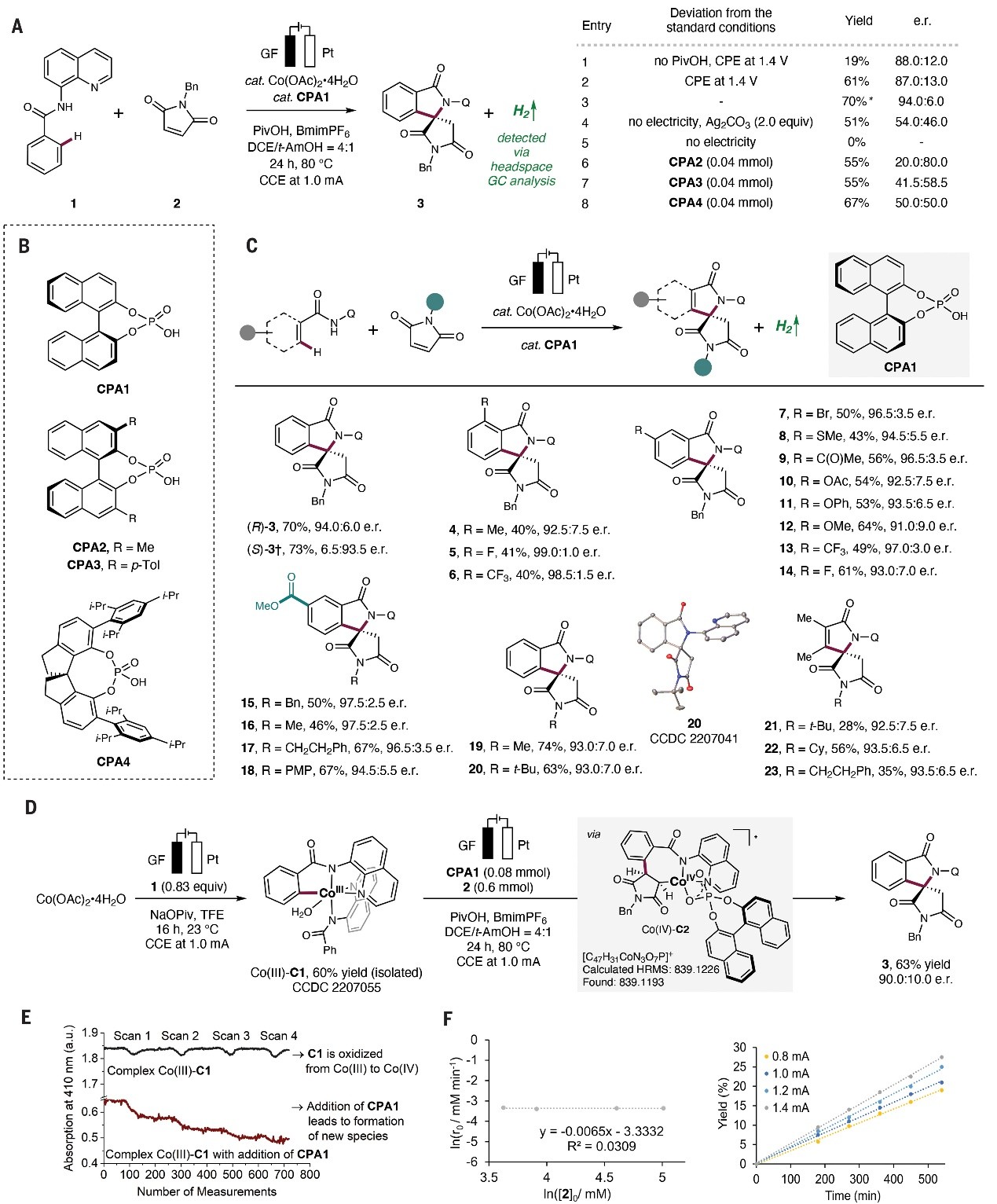
图2. 电化学钴催化C-H键活化的螺环化反应。图片来源:Science
其次,作者进行了相关实验对反应过程进行了深入的研究,具体而言:1)在恒定电流下,环金属化、C-H键活化的配合物Co(III)-C1可以化学计量制备,这表明产物高效的形成和选择性均需要电,进而说明该反应机制可能是通过氧化诱导的还原消除进行(图2D);2)高分辨率质谱(图2D)和紫外-可见光谱电化学分析(图2E)支持了Co(III/IV/II) 歧化的现象并证明钴-CPA1中间体的形成,进而说明CPA1与钴中心是直接配位来诱导反应的对映选择性;3)平行反应的动力学同位素效应为kH/kD≈1.0,这表明除了C-H键裂解之外还有其它决速步骤;4)不同马来酰亚胺浓度的初始速率对数图表明迁移插入步骤相对较快(图2F);5)不同电流与产物的形成有直接的相关性,进而说明电子转移也是速率的决定因素;6)改变配体CPA1的e.e.值,发现产物3的e.r.值取决于催化剂,这意味着酸的缔合和多配体催化剂是无效的。
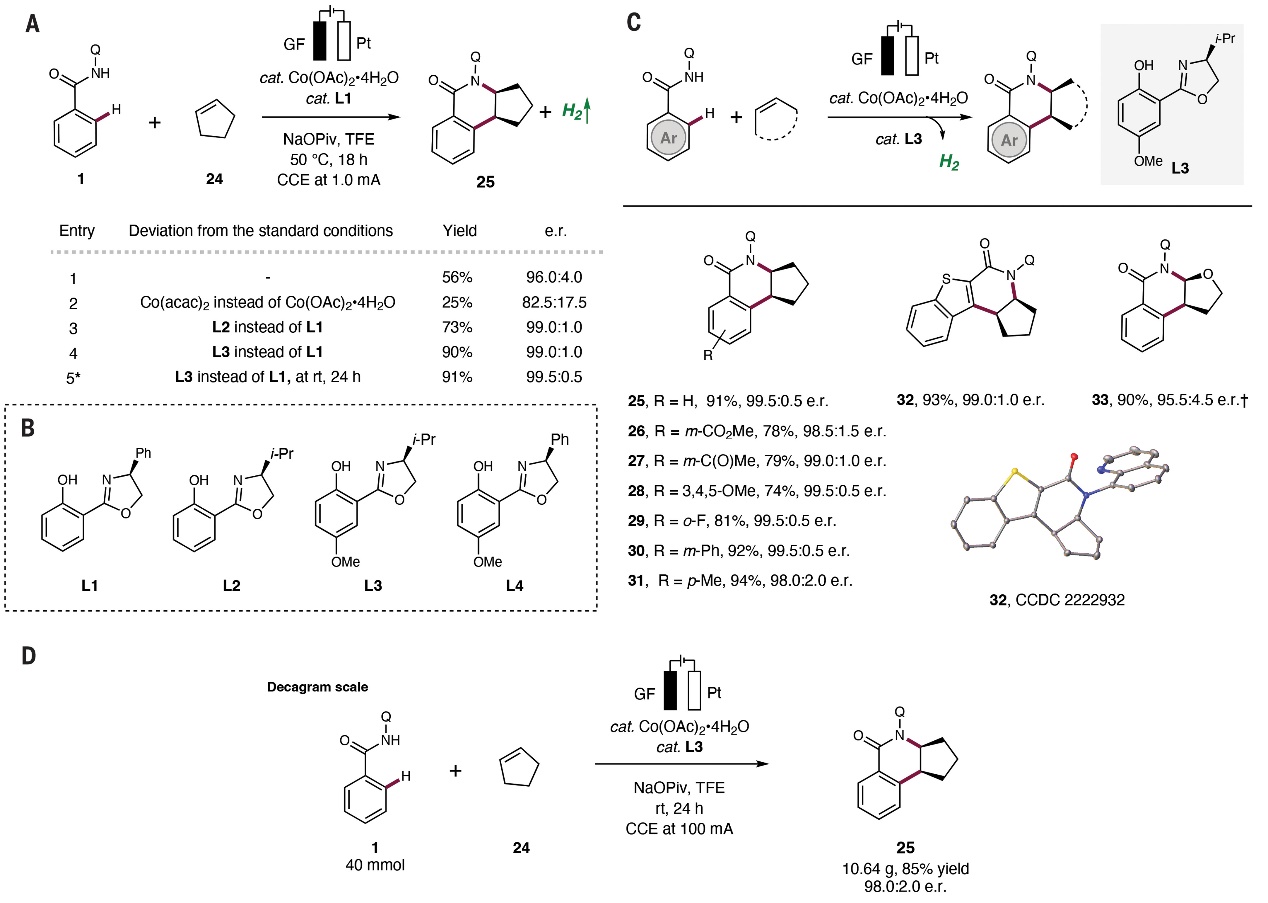
图3. 电氧化钴催化烯烃对映选择性碳胺化反应。图片来源:Science
接下来,作者以苯甲酰胺1和未活化烯烃24为模型底物对烯烃碳胺化反应进行了条件优化(图3A-B),结果显示L-缬氨酸衍生的配体L3效果最好,在室温下能以高收率和优异的对映选择性获得一系列手性二氢异喹啉酮(25-32,图3C),其中产物32的绝对构型通过X-射线衍射分析证实。此外,当使用L4作为最佳配体时,含杂原子的环烯烃(33)也可实现这一转化。值得一提的是,该反应还可以十克级规模进行制备且反应的收率和对映选择性不会降低(图3D),同时反应的法拉第效率为89%,这表明所提供的电能可被有效利用。
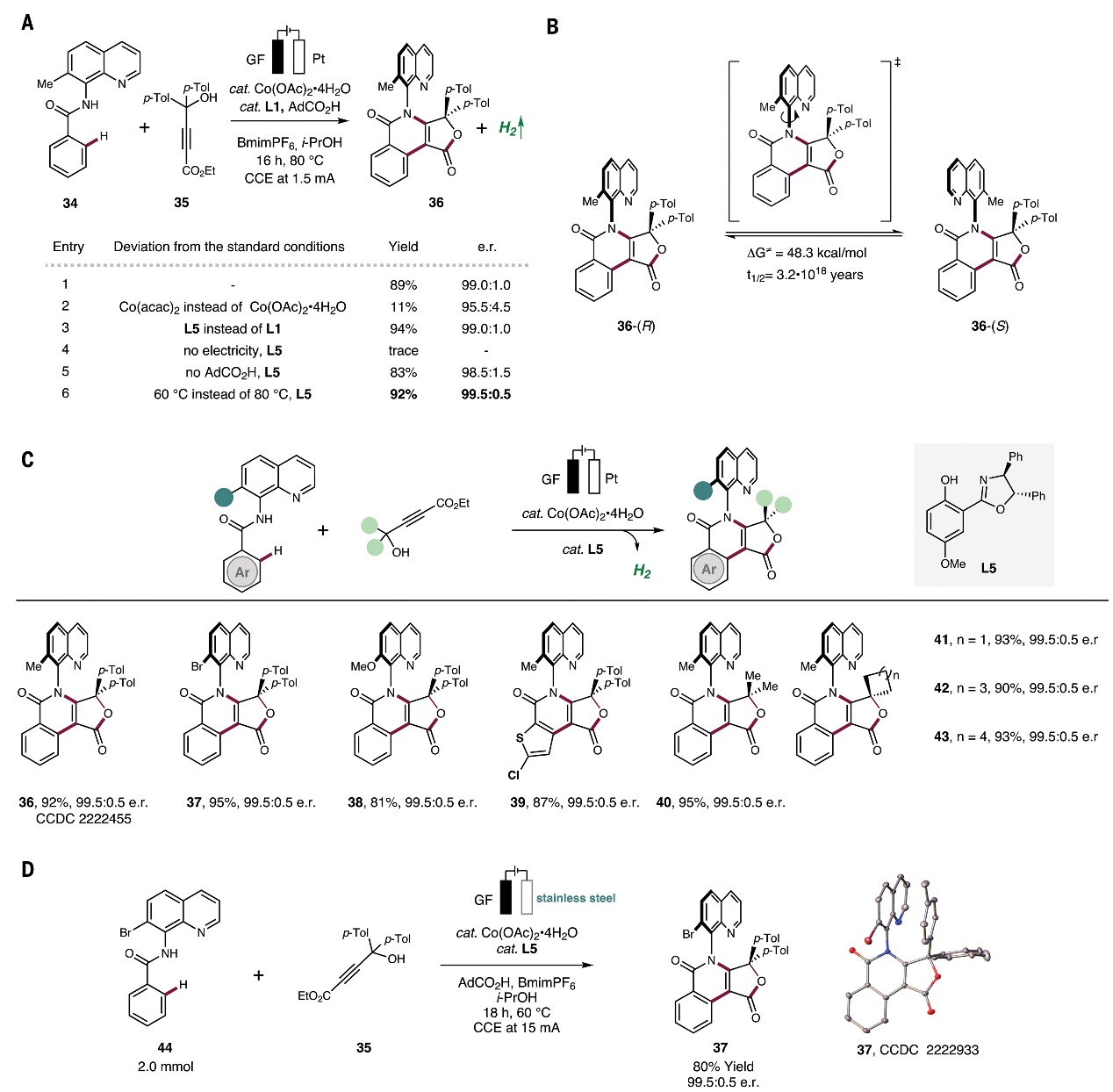
图4. 电氧化钴催化对映选择性C-H键和N-H键环化获得轴手性分子。图片来源:Science
鉴于轴手性化合物在有机合成和新药研发中发挥着越来越重要的作用,因此作者尝试利用苯甲酰胺34和4-羟基炔酸酯35的C-H键和N-H键串联环化反应来构建C-N轴手性化合物36(图4A),密度泛函理论计算显示C-N轴的旋转能垒为48.3 kcal/mol(图4B)。对反应条件进行优化后,发现在L5为配体、i-PrOH为溶剂的条件下于60 ℃反应16 h,能以92%的收率和99.5:0.5 e.r.值获得产物36,并通过X-射线衍射分析证实其绝对构型。在最优条件下,作者对底物范围进行了考察(图4C),结果显示不同基团取代的酰胺底物(36-38)、4-羟基炔酸酯(40-43)甚至杂环底物(39)均能实现这一转化,以优异的收率(81-95%)和对映选择性(99.5:0.5 e.r.)获得相应的轴手性产物。需要指出的是,当用不锈钢替代铂电极进行反应时,也可以80%的收率和99.5:0.5 e.r.值获得产物37(图4D),并且能以2 mmol规模进行制备。
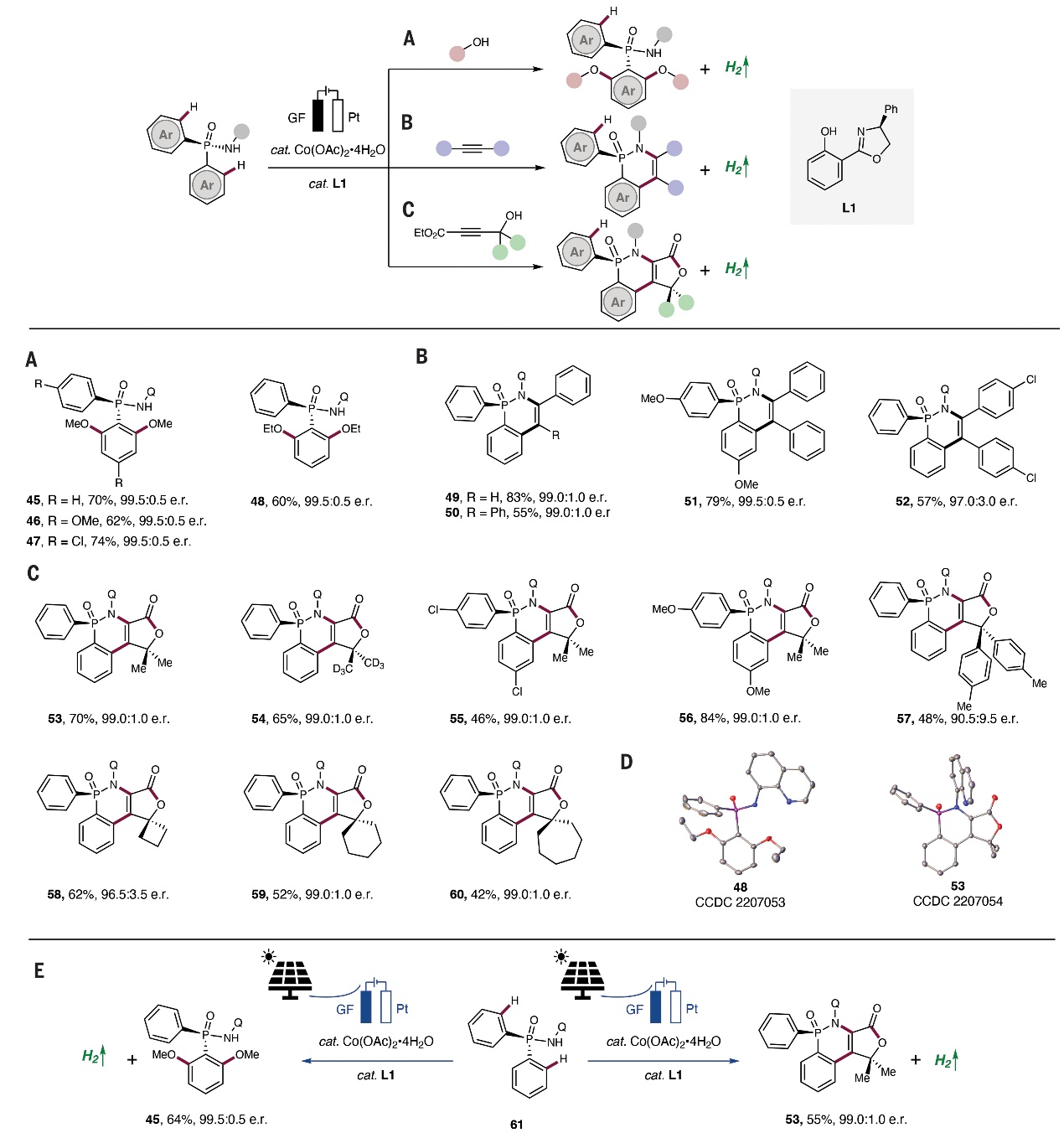
图5. 电氧化钴催化对映选择性C-H键和N-H键环化构建P-中心手性分子。图片来源:Science
最后,作者稍微修改Co-电催化的反应条件即可实现亚膦酰胺的去对称化(图5),即双齿配体(L1)诱导对映选择性脱氢C-H键醚化反应,以高对映选择性获得了各种无环手性亚膦酰胺(45-48,图5A),其中48的绝对构型通过X-射线衍射分析证实。除此之外,C-H键和N-H键活化的炔环加成反应同样也可实现去对称化,并且内炔(50-52)、苯乙炔(49)均可以良好的收率和优异的对映选择性转化为所需产物。类似地,亚膦酰胺与4-羟基炔酸酯经C-H键和N-H键串联活化构建C-C、C-N和C-O键,进而以高对映体纯度获得各种稠合多环P-中心手性化合物(53-60),包括不同环尺寸的螺环骨架(58-60),其中产物53的绝对构型通过X-射线衍射分析证实(图5D)。值得注意的是,市售光伏电池产生的可再生太阳能也可实现HER耦合的电氧化钴催化,进而显示了该方法的实用性(图5E)。
总结
Lutz Ackermann教授课题组利用电氧化Co催化策略,成功地实现了苯甲酰胺类底物的高化学选择性、区域选择性和对映选择性C-H键环化、N-H(C-H和 N-H串联)键环化以及亚磷酰胺的脱氢C-H键醚化反应,构建了一系列碳中心手性、膦中心手性和轴手性化合物。这种策略通过HER产生分子氢作为唯一的副产物,有望在有机合成获得广泛应用。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enantioselective electrochemical cobalt-catalyzed aryl C-H activation reactions
Tristan von Münchow, Suman Dana, Yang Xu, Binbin Yuan, Lutz Ackermann
Science, 2023, 379, 1036-1042, DOI: 10.1126/science.adg2866
导师介绍
Lutz Ackermann
https://www.x-mol.com/university/faculty/49786
(本文由吡哆醛供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号