钴催化吲哚C–H官能团化介导的桥环烯烃不对称开环反应
桥环烯烃的不对称开环反应近年来引起了人们的关注。特别是与过渡金属催化的C–H键活化策略相结合,为构建复杂环状分子提供了有效的方法 (Chem. Soc. Rev. 2021, 50, 3013-3093)。氮杂桥环烯烃是该类反应中应用较多的底物 (Angew. Chem. Int. Ed. 2019, 58, 322-326; Angew. Chem., Int. Ed. 2019, 58, 2514-2518),而氧杂桥环烯烃的不对称开环反应鲜有报道,主要原因是易发生脱水等副反应。一般认为,该类反应经过芳基C–H键活化、芳基金属物种对烯烃的exo-配位和迁移插入,最终通过顺式β-杂原子消除得到顺式目标产物。迁移插入通常被认为是反应的手性决定步骤(图1)。
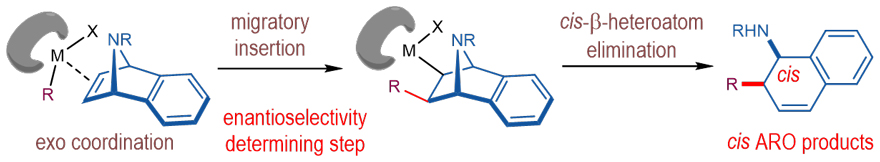
图1. 桥环烯烃不对称开环反应的一般机理假设
最近,中国科学院上海有机化学研究所游书力研究员(点击查看介绍)团队报道了通过钴催化吲哚C–H官能团化介导的氧杂桥环烯烃不对称开环反应(图2)。研究人员发现当使用非手性五甲基环戊二烯基钴催化剂和联二萘衍生的手性环戊二烯基钴催化剂时,反应分别得到反式和顺式构型的开环产物,其中顺式开环产物的对映选择性最高可达 >99% ee。这一结果打破了桥环烯烃的不对称开环反应只能得到顺式开环产物的传统认知,还更正了文献报道的产物相对构型的错误(Adv. Synth. Catal. 2017, 359, 513-518)。
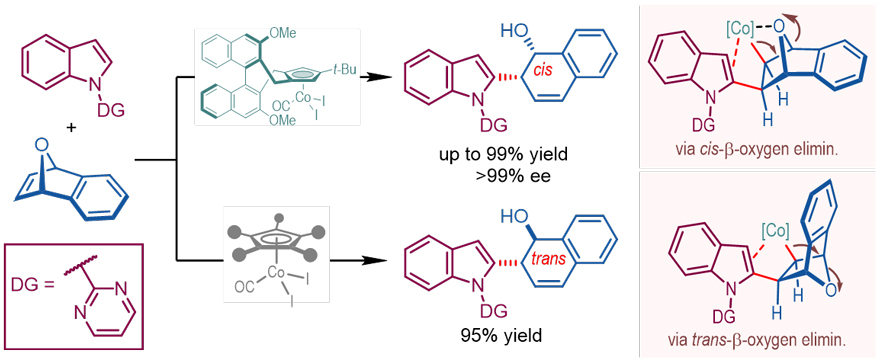
图2. 钴催化吲哚C–H官能团化介导的氧杂桥环烯烃不对称开环反应
研究人员进一步通过DFT计算提出该反应的机理。指出使用非手性钴催化剂或手性钴催化剂的反应分别通过反式或顺式β-氧消除进行。β-氧消除是该反应的决速步骤和(手性反应的)对映选择性决定步骤。这一推测通过H/D和12C/13C动力学同位素实验得以证实(图3)。
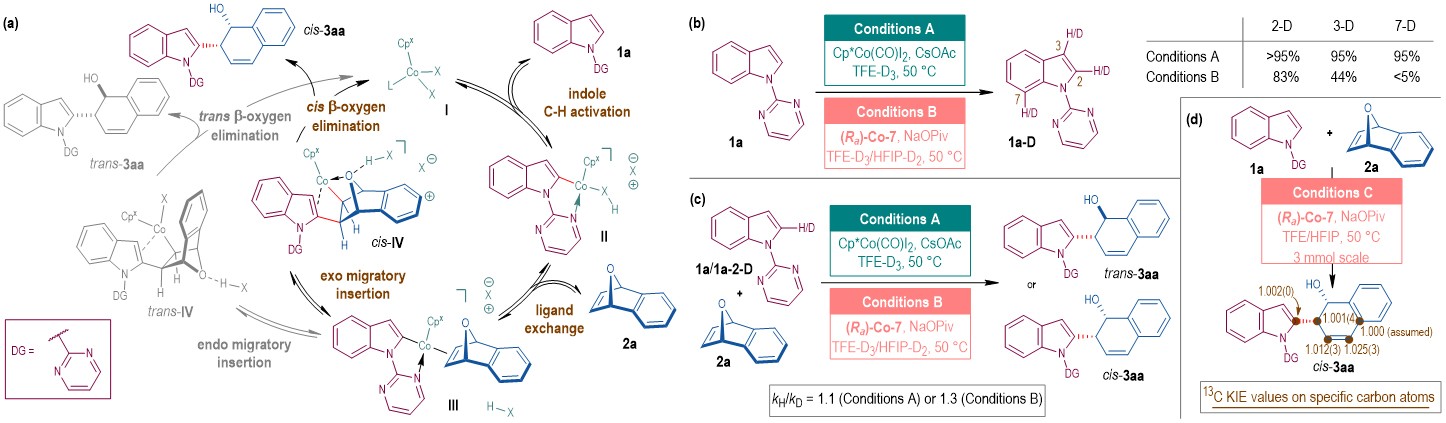
图3. 催化循环和机理实验
在类似的条件下,研究人员还实现了钴催化吲哚C–H官能团化介导的氮杂桥环烯烃不对称开环反应,通过变换溶剂实现了产物的立体发散性合成(图4)。
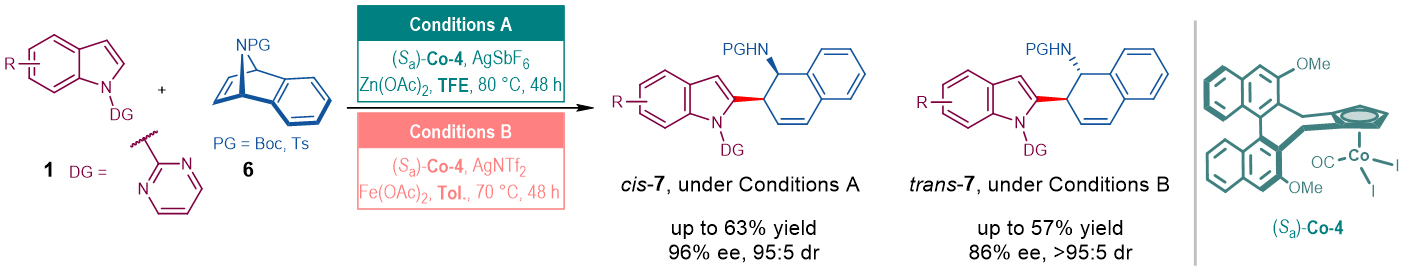
图4. 钴催化吲哚C–H官能团化介导的氮杂桥环烯烃不对称开环反应
小结
游书力研究员团队发展了钴催化吲哚C–H官能团化介导的桥环烯不对称开环反应,通过使用不同骨架的钴催化剂实现了开环产物非对映体的选择性合成。反应条件温和,底物普适性广泛。通过DFT计算和动力学同位素实验提出了由β-氧消除控制反应非对映和对映选择性的新机理模型。并在类似条件下实现了氮杂桥环烯烃立体发散式开环反应。相关研究结果近期发表在Nature Communications 期刊上。郑洋博士为本文的第一作者,郑超副研究员和游书力研究员为本文的通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cobalt(III)-catalyzed asymmetric ring-opening of 7-oxabenzonorbornadienes via indole C–H functionalization
Yang Zheng, Wen-Yun Zhang, Qing Gu, Chao Zheng & Shu-Li You
Nat. Commun., 2023, 14, 1094, DOI: 10.1038/s41467-023-36723-6
导师介绍
游书力
https://www.x-mol.com/university/faculty/15598
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号