格罗宁根大学Roelfes组Angew:人工酶参与的胞内生物催化级联
细胞的新陈代谢是经典的生物催化级联反应。天然产物的复杂分子结构源于复杂的生物合成网络。研究人员可通过代谢工程对代谢途径中的酶进行改造调控,获得新的天然产物。然而获得产物的结构多样性本质上受自然界反应类型的限制。相比之下,化学合成在反应类型上提供了更多的可能性,但目前化学合成的复杂程度却无法与生物合成相媲美。因此在细胞内将化学合成与生物催化结合起来,创造一种人工生物合成路径来实现非天然产物的合成将会是一种很有潜力的途径。
近日,江南大学周志教授作为共同一作与格罗宁根大学Gerard Roelfes教授在国际知名期刊Angew. Chem.上发表论文,基于该课题组成功构建并进化的人工酶(Angew. Chem. Int. Ed. 2019, 58, 2083–2087),将其与天然酶一并转化至大肠杆菌中。该人工酶可接受天然酶催化产生的苯甲醛衍生物与外源添加的肼类化合物为底物,催化合成腙类化合物,从而实现了人工酶参与的体内生物催化级联反应。这种包括人工酶催化的体内生物催化级联是实现人工生物合成路径创制的重要一步。
生物体可利用简单的有机物通过酶促级联反应合成复杂的天然产物。生物合成的反应通常都在水相以及温和的反应条件下进行,具有环境友好性,但这也限制了其反应类型。化学催化中可通过高温、强酸、强碱条件活化底物,并供给反应所需能量,实现天然条件下难以实现的转化。目前,生物催化的反应范围明显小于化学催化。为了扩展生物催化的范畴,致力于实现非天然生物转化的人工酶得到了越来越多的关注。人工酶构建是将合成化学催化剂整合至蛋白质骨架中,蛋白骨架可提供额外的相互作用加速反应,并保护化学催化剂免受细胞环境的影响。
本研究中的人工酶基于一种乳酸乳球菌多药耐药性调节剂(LmrR),在这项研究中使用的LmrR蛋白变体为LmrR_V15pAF,其15位为一非天然并具备催化活性的pAF残基。pAF残基可通过正交翻译系统直接引入。引入的非天然苯胺侧链可活化醛形成瞬态亚胺离子中间体,该中间体是有机催化中多功能反应性中间体。在课题组前期研究中,LmrR_V15pAF被证明可以催化苯甲醛衍生物与肼的非生物反应以形成腙,随后的定向进化得到的突变体 (LmrR_V15pAF_RMH) 将催化效率提高了57 倍(Angew. Chem. Int. Ed. 2019, 58, 2083–2087)。LmrR_V15pAF和进化的变体利用相同的亚胺离子活化策略,还可成功用于烯醛的共轭加成反应 (ACS Catal. 2021, 11, 6763–6770)。
目前已有多篇报道羧酸或醇类化合物为起始合成醛的天然酶报道,因此设想使用已报道的天然醛合成酶与LmrR_V15pAF及其变体可在体内进行酶促级联反应以实现非天然的腙合成(图1)。为实现体内酶促级联反应,首先需要在体内过表达人工酶。该课题组基于琥珀终止密码子抑制技术,使用正交翻译系统OTS可直接在LmrR特定位置插入pAF,但此方法同时也伴有其他氨基酸的插入而引入的空白干扰。因此,作者首先通过优化表达条件来改善pAF的直接插入。在MMV培养基中,苯丙氨酸的错引率较低,非天然氨基酸引入率最高。
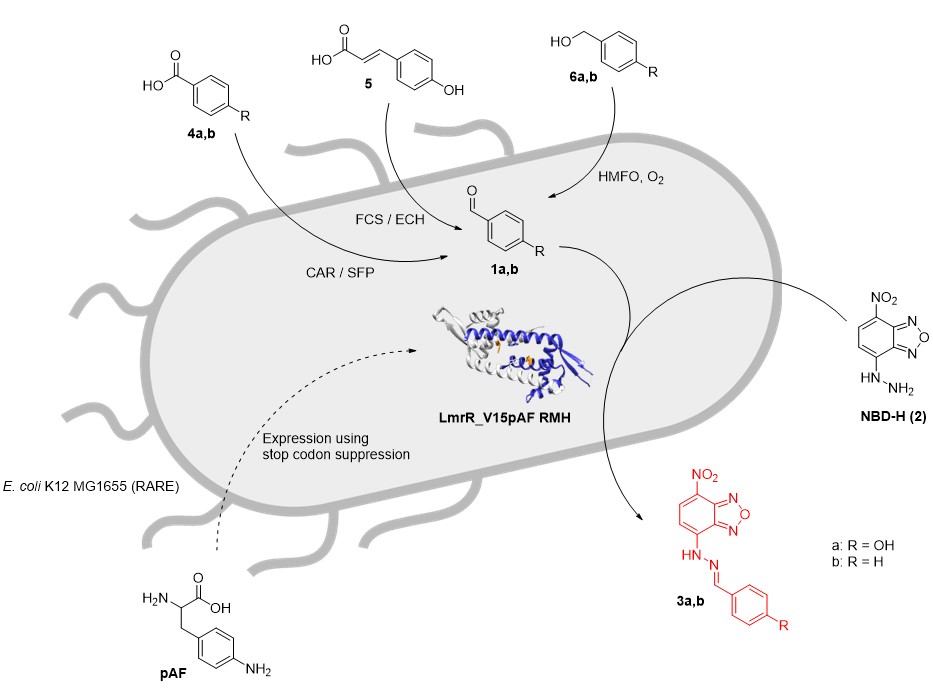
图1. 人工酶LmrR_V15pAF_RMH催化非天然成腙成反应的细胞内级联反应示意图。
此后,作者考察了全细胞中实现人工酶的腙合成反应。将LmrR_V15pAF及其变体分别转化至该菌株中,外源加入1a /苯甲醛(1b)与NBD-H,孵育3 h以测定产物生成,并同时考察了在磷酸盐缓冲液(pH 7)中的产物产生情况。当使用含有LmrR_V15pAF_RMH的细胞时,MMV培养基和磷酸缓冲液中分别以62%和82%的产率和31%和73%的产率获得腙产物3a和3b(图2)。该结果充分显示了LmrR_V15pAF_RMH具备全细胞催化腙合成的能力。
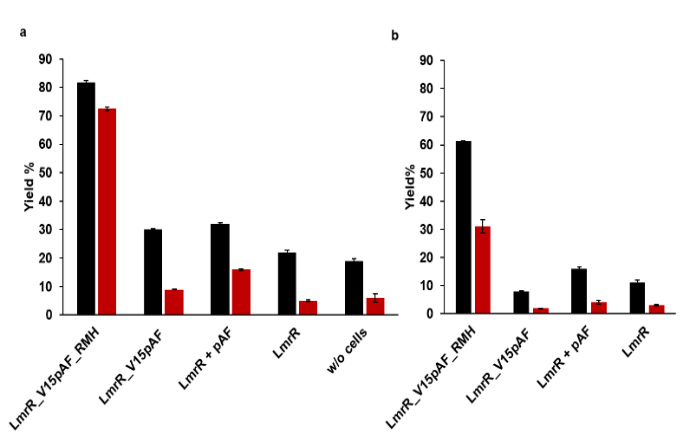
图2. 全细胞催化腙合成反应(黑色:MMV培养基中,红色:磷酸盐缓冲液,pH 7)
接下来,作者研究了细胞中芳香醛的生物合成途径,主要考察三种天然酶体系以生产醛底物1a和1b。第一种醛合成策略为Nocardia iwensis 来源的羧酸还原酶(CAR)与Bacillus subtilis 来源的磷酸泛乙基转移酶(SFP)体系,该体系依赖NADPH和ATP,可将苯甲酸还原为相应的苯甲醛。第二种策略通过使用来自Amycolatopsis thermoflava 的阿魏酰辅酶A合成酶(FCS)和烯醇辅酶A水合酶/醛缩酶(ECH),可将香豆酸转化为对羟基苯甲醛。第三种策略则使用Methylovorus sp.来源的5-羟甲基糠醛氧化酶(HMFO),此酶为黄素依赖蛋白,可利用分子氧氧化各种芳香醇,同时生成H2O2。作者将三种醛合成体系分别转化至E. coli细胞中,蛋白24 ℃诱导表达16 h后,直接向MMV培养基中加入各自底物并继续孵育2 h。结果显示HMFO体系可实现全细胞催化氧化苄醇和对羟基苄醇分别以30%和79%产率获得对应芳香醛3a和3b。CAR-SFP体系与FCS-ECH体系均可实现较好的合成对羟基苯甲醛收率(图3)。
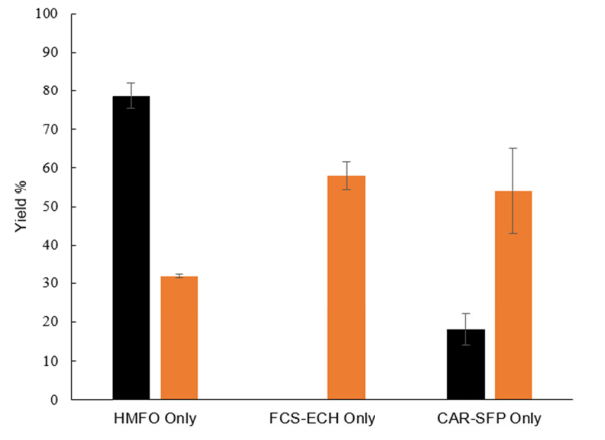
图3. 三种醛合成体系产率比较(黑色:产物为1a的反应,橘色:产物为1b的反应)
在证明LmrR_V15pAF_RMH的腙合成产物以及参与反应的底物1a和1b均可在E. coli RARE细胞中产生后,作者尝试将这些过程结合起来,建立体内生物催化级联反应。三质粒系统:pETDuet-1、pET28b+、pDULE-pAF共转化至E. coli中。向培养基中加入NBD-H和醛前体后,24 ℃下反应24 h。具有LmrR_V15pAF_RMH的CAR-SFP在以4a或4b为醛前体的全细胞中均显示出高于背景反应的腙产率。表达FCS-ECH / LmrR_V15pAF_RMH的体系同样可以获得良好的3a产率(图4)。
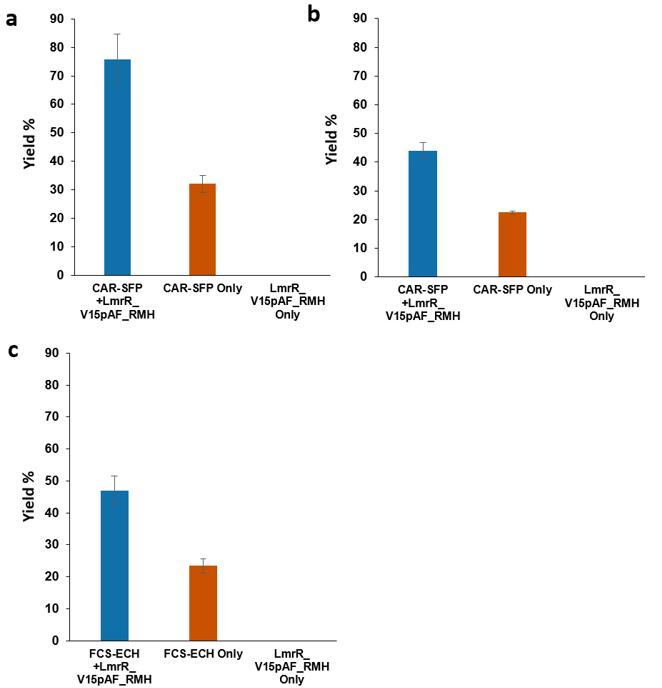
图4. 三质粒系统的体内级联反应中腙产物的产率。(a)CAR-SFP/LmrR_V15pAF_RMH体系中3b的合成;(b)CAR-SFP/LmrR_V15pAF_RMH体系中3a的合成;(c)FCS-ECH / LmrR_V15pAF_RMH体系中3a的合成
HMFO基因较小,因此作者采用pBAD质粒(HMFO + LmrR_V15pAF_RMH)与pDULE-para-aminoPhe 2的双质粒系统。表达HMFO和LmrR_V15pAF_RMH的细胞在pH 6.5磷酸缓冲液体系中加入NBD-H和醛前体苄醇(6b),反应2小时可以81%的产率得到相应的腙产物3b(图5a)。相比之下,仅表达HMFO的细胞对照实验产率仅为6%。由于HFMO/LmrR_V15pAF_RMH级联反应与背景反应的明显差异,甚至可以目测观察反应性的差异(图5b)。这些结果表明,人工酶与天然酶共同参与的体内酶促级联反应是成功和有效的。
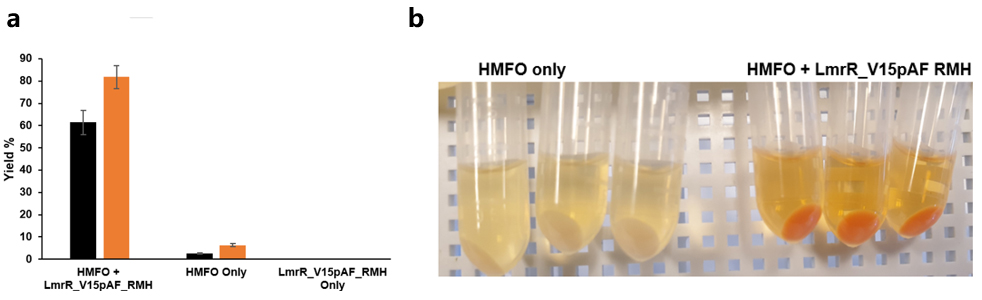
图5, HFMO/LmrR_V15pAF_RMH体内级联反应体系腙产物的产率。(a)HFMO/LmrR_V15pAF_RMH体内级联反应产率,黑色:反应1 h,橘色:反应2 h;(b)反应2 h后反应体系的比较
总结
本研究在大肠杆菌中创建了包含天然酶和人工酶的细胞内生物催化级联体系。这些结果表明,异源生物合成途径不仅可以通过引入天然酶对代谢路径进行改造,还可以通过引入人工酶来进行改造以生产非天然的化合物。这项工作是对创建新型人工生物合成路径的探索,也是朝着创造人工代谢系统迈出的一步。未来这种人工代谢系统将活细胞中的多种天然酶和人工酶结合起来,可以从简单的生物基起始材料出发生产复杂分子,为利用合成生物学手段创造非天然新分子提供新的理念和技术。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

In vivo Biocatalytic Cascades Featuring an Artificial-Enzyme-Catalyzed New-to-Nature Reaction
Linda Ofori Atta, Zhi Zhou, Gerard Roelfes
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202214191
导师介绍
Roelfes group
周志课题组主页
https://www.x-mol.com/groups/zhouzhi
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号