肿瘤选择性激活的TLR7/8激动剂纳米免疫调节剂用于肿瘤免疫治疗
小分子TLR7/8激动剂作为一种有潜力的固有免疫调节剂,能够通过树突状细胞的激活途径增强细胞毒性T淋巴细胞的肿瘤内浸润。目前咪喹莫特(IMQ)已被FDA批准用于基底细胞癌的治疗,然而,静脉注射导致的系统性免疫相关毒副作用(如系统性免疫风暴)极大限制了其临床剂型的进一步开发和应用。如何将IMQ的调节作用限制在肿瘤部位而不影响正常组织仍然面临系列挑战。因此,迫切需要开发一种基于小分子TLR7/8激动剂的安全有效的系统给药新策略。
近日,山东大学药学院张志岳教授团队利用晶体结构分析结果表明IMQ的C4位氨基是其发挥作用的关键活性位点,设计开发了一种巧妙的IMQ活性位点掩蔽策略(OFF),以期避免IMQ静脉注射后引发的免疫激活。在肿瘤环境中,IMQ的C4位氨基在肿瘤中能够通过1,6-消除反应得以暴露进而发挥其肿瘤特异性的免疫系统激活(ON)。
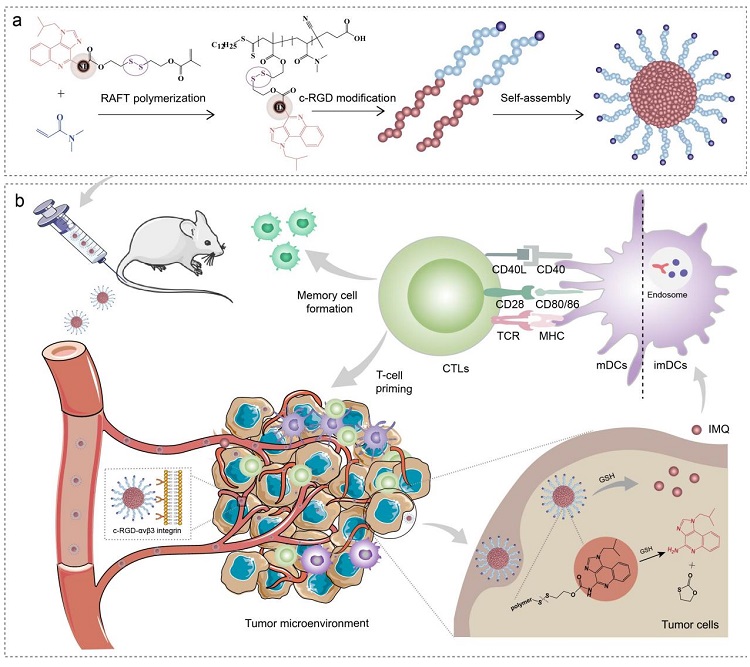
图1. TLR7/8激动剂纳米免疫调节剂的设计和体内精准递送
谷胱甘肽(GSH)在肿瘤中高表达,含量约为正常细胞的1000倍,在设计肿瘤微环境响应性材料方面具有较大应用前景。该团队利用GSH敏感的Linker掩蔽IMQ的C4位氨基构建了一种IMQ掩蔽性单体分子HEDSMA-IMQ。游离IMQ的亲脂性芳香环与TLR的Phe408和Tyr256发生π-π堆积相互作用。IMQ的碱性C4位氨基通过氢键直接与Asp555和Thr586结合,这是TLR7效力的关键驱动因素。而将HEDMSA基团引入IMQ的C4位氨基后导致了口袋中的显著结合构象变化。IMQ基团与相邻的口袋结合,并通过π–π堆积与Phe507相互作用。氨基甲酸酯基团与Lys410和Thr532形成多个氢键。末端酯基团占据先前的IMQ结合袋,并通过氢键与Thr586相互作用。与Asp555的关键相互作用的丢失表明其与TLR7的结合力降低。这表明与IMQ结合的TLR7能够保持其激活状态,而HEDSMA IMQ结合的TLR7转变为抑制状态。
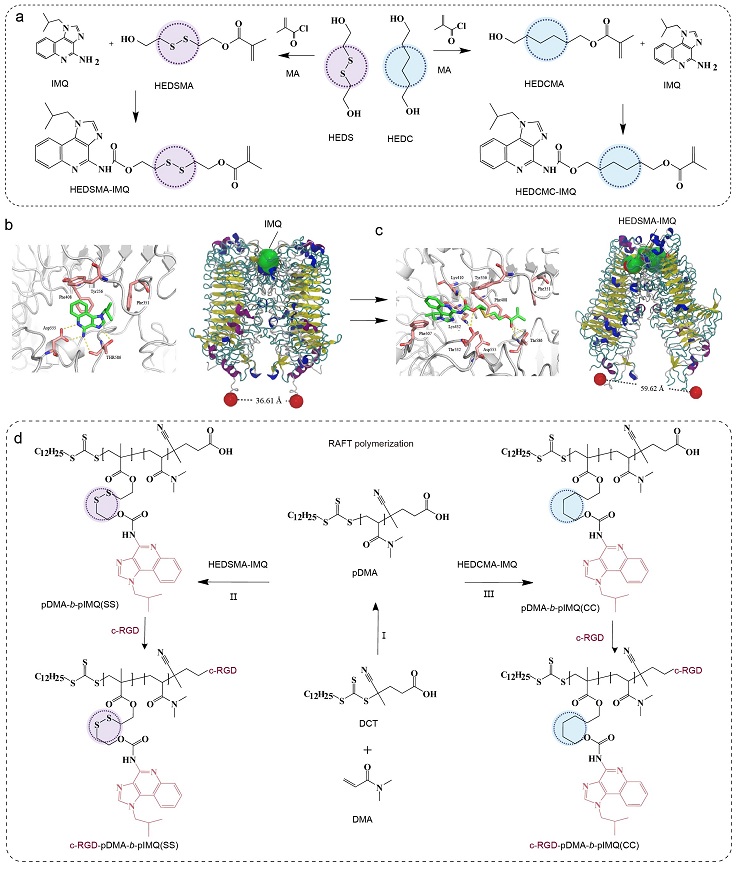
图2. TLR7/8激动剂掩蔽单体的合成和RAFT聚合技术路线
原位乳腺癌小鼠经纳米免疫调节剂治疗后,观察到了肿瘤免疫微环境中细胞毒性T淋巴细胞的有效浸润,显著调动了肿瘤特定部位免疫系统的激活。同时在小鼠体内形成了免疫记忆以阻止肿瘤复发。
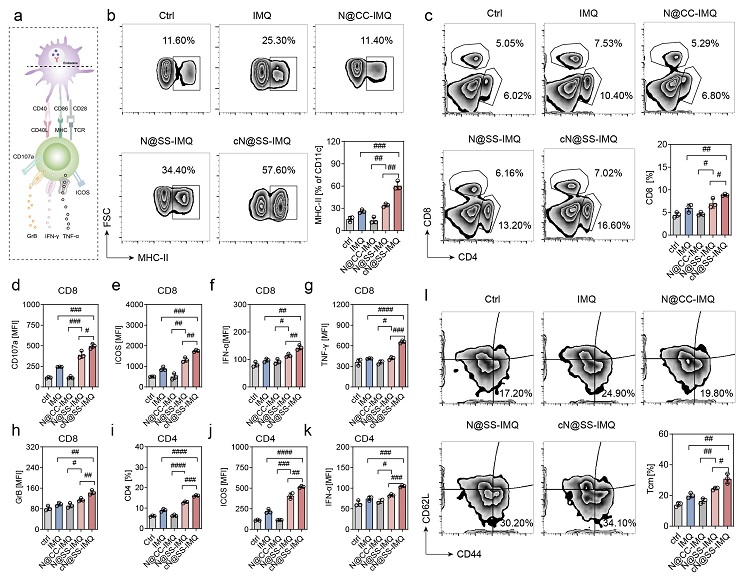
图3. TLR7/8激动剂纳米免疫调节剂促进了肿瘤免疫微环境中免疫细胞的浸润和激活
综上所述,该TLR7/8激动剂递送系统静脉注射后,由于IMQ的C4位氨基被掩蔽能够有效规避系统性免疫毒性。而到达肿瘤后,肿瘤部位高表达的GSH可以引发IMQ的C4位氨基再次暴露进而激发肿瘤特异性的免疫激活。该策略为安全递送免疫调节小分子提供了一种新思路。这一成果近期发表在Angewandte Chemie International Edition 上,第一作者为博士研究生郝燕云,张志岳教授为独立通讯作者,山东大学药学院为第一作者单位和唯一通讯作者单位。
近年来,张志岳教授团队在肿瘤的靶向递药、针对固有免疫激活用于肿瘤治疗等方面取得了一系列研究成果,先后开发了化疗-光热-免疫三合一的纳米精准递送体系(Adv. Healthc. Mater. 2022, 11, e2102739), 酸敏感钙交联原位肿瘤疫苗(Adv. Healthc. Mater. 2022, 11, e2102781),级联响应三嵌段聚合物递送载体(J Nanobiotechnology. 2022. 20, 369)等新型小分子免疫激动剂药物递送系统。上述研究得到了齐鲁青年学者启动资金、国家自然科学基金委员会与欧盟委员会“中欧人才项目”、国家自然科学基金、山东省自然科学基金等科研项目的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Tumor-Selective Activation of Toll-Like Receptor 7/8 Agonist Nano-Immunomodulator Generates Safe Anti-Tumor Immune Responses upon Systemic Administration
Yanyun Hao, Hui Li, Xiaoyan Ge, Yang Liu, Xia Li, Yutong Liu, Hongfei Chen, Shiying Zhang, Jing Zou, Lingling Huang, Fabao Zhao, Dongwei Kang, Bruno G. De Geest, Zhiyue Zhang
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202214992
张志岳博士简介

张志岳,男,山东大学药学院教授,博士生导师。中国药学会高级会员,国家公派出国留学评审专家。2009年、2012年分别获得山东大学学士、硕士学位,2016年博士毕业于比利时根特大学(Ghent University, Belgium)药剂学专业。主要从事多功能聚合物以及聚合物修饰金纳米粒在药物传递方面的研究工作。先后获得根特大学CSC-co-Funding 以及根特大学BOF博士后奖学金的资助,其中2014年和2015年两次受比利时弗兰德省FWO会议旅行奖学金资助参加美国化学会年会,展示了多功能聚合物修饰的金纳米粒作为纳米载体材料在生物医学方面的应用。2018年以山东大学‘齐鲁青年学者’特聘教授身份加入山东大学药学院,主要从事药用载体材料以及多功能纳米药物递送系统的设计开发研究工作。截止目前,已在Angewandte Chemie International Edition, Advanced Functional Materials, Advanced Healthcare Materials, Chemistry of Materials等药剂学/材料化学领域权威学术期刊发表SCI论文20余篇。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号