靶向乙肝病毒感染相关疾病治疗新策略:抑制钠-牛磺胆酸共转运蛋白(NTCP)
乙肝病毒(HBV)感染是亟待解决的全球公共卫生难题之一。据《柳叶刀》模型预测,在2018年全球有约2.9亿人遭受HBV慢性感染,且感染相关疾病将导致每年90万人死亡。中国是全球HBV流行的重灾区:感染人数多、感染率高、感染导致的相关疾病死亡率远高于世界平均水平。因此,抗HBV药物的研发十分迫切。近日,西南交通大学符雷蕾副教授(点击查看介绍)和张岚副教授(点击查看介绍)联合研究针对HBV进入受体钠-牛磺胆酸共转运蛋白(NTCP),就其生物学功能、结构特点以及在HBV相关疾病中的治疗潜力进行重点阐述。
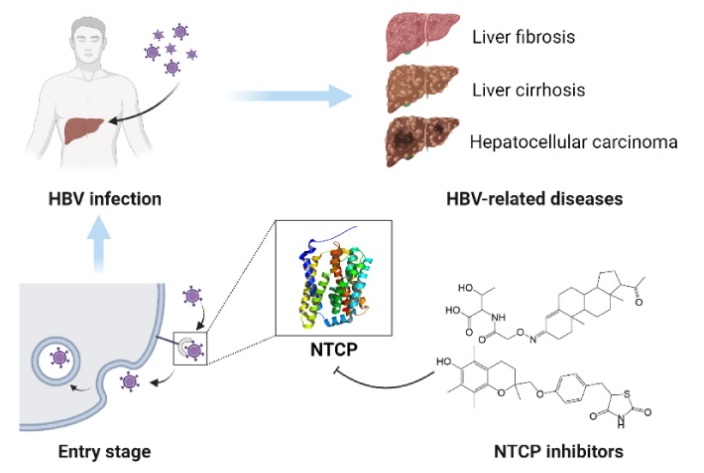
图1.在HBV感染相关疾病中靶向NTCP
乙肝病毒是典型的肝病毒家族成员,具有松弛的环状DNA,编码多种功能性蛋白。慢性乙肝病毒感染有很高的几率发展成为肝纤维化、肝硬化甚至是肝癌。乙肝病毒通过多种直接、间接机制参与肝癌的发生和发展:病毒DNA插入宿主细胞基因组导致基因不稳定或癌症相关基因插入突变、病毒功能性蛋白(如HBsAg、HBeAg和HBx)导致宿主细胞转录、增殖的失调,使宿主细胞对致癌因子和染色体畸变更敏感。2012年,李文辉教授团队发现肝细胞基底外侧膜上的钠-牛磺胆酸共转运蛋白是乙肝病毒及其卫星病毒丁肝病毒的进入受体,为乙肝病毒感染治疗带来另外一种可能。西南交通大学研究小组阐述了该受体在胆汁酸的肝肠循环以及乙肝病毒感染肝细胞的过程中的作用。特别地,他们总结乙肝病毒感染机制相关研究,描绘了较为完整的乙肝病毒进入肝细胞的过程。
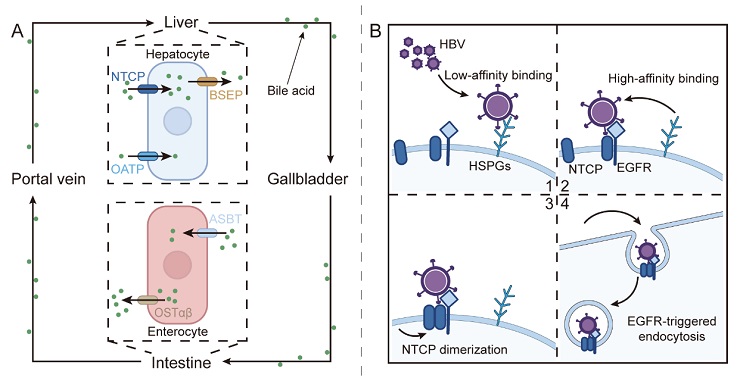
乙肝病毒进入抑制剂靶向肝细胞基底外侧膜上的跨膜蛋白钠-牛磺胆酸共转运蛋白,在病毒生命周期早期阶段阻止病毒感染。然而,目前还没有靶向该受体的小分子抑制剂进入临床试验阶段,一个主要原因是缺少蛋白质结构的指导。基于近期发布的钠-牛磺胆酸共转运蛋白的电镜结构,研究小组重点阐述了该受体的蛋白质结构特征。更重要的是,他们系统性总结并讨论了现有的氨基酸突变的实验结果,并结合基于人工智能的预测工具分析了NTCP的潜在药物结合位点。此外,他们从体内外活性、选择性、构效关系等角度归纳和阐述了靶向该受体的小分子化合物和生物大分子。
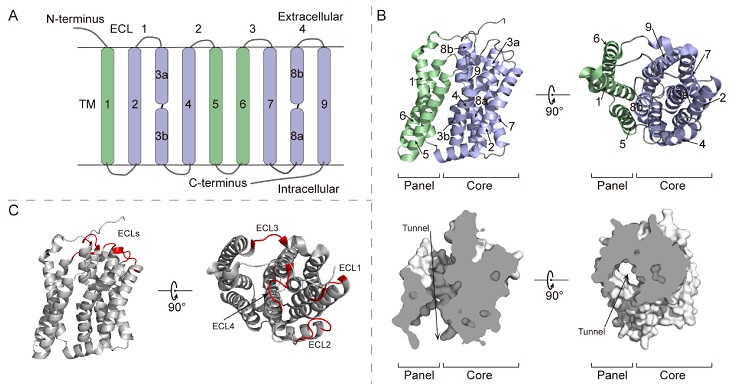
图3. NTCP的结构示意图
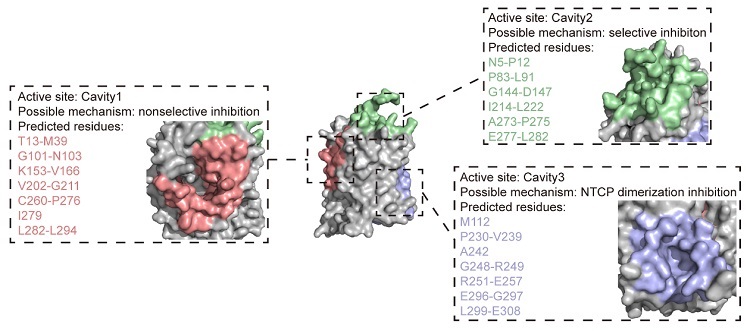
图4. NTCP的潜在活性位点
以上重要信息为基于结构的靶向钠-牛磺胆酸共转运蛋白的合理药物设计提供线索和理论依据。这一成果近期发表在药物化学Top期刊Journal of Medicinal Chemistry, 2022;DOI:10.1021/acs.jmedchem.2c01097(中科院药物化学一区,影响因子:8.039)上,西南交通大学符雷蕾副教授为通讯作者,硕士研究生陈思伟、张岚副教授为共同第一作者;四川大学华西医院胃肠外科陈亿教授为共同通讯作者。
符雷蕾和张岚研究小组长期从事于靶向NTCP小分子候选药物的发现及其作用机理研究。近年来,已累计发表相关研究成果论文多篇(Cell Prolif 2014, 47 (4), 326-335. Bioorg Med Chem 2015, 23 (5), 976-984. Eur J Med Chem 2018, 147, 205-217. Bioorg Med Chem Lett 2019, 29 (19), 126623. Chinese Chem Lett 2020, 31 (6), 1422-1426.),并相继发现多个靶向NTCP的小分子抑制剂。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Inhibiting Sodium Taurocholate Cotransporting Polypeptide in HBV-Related Diseases: From Biological Function to Therapeutic Potential
Siwei Chen, Lan Zhang, Yi Chen*, and Leilei Fu*
J. Med. Chem., 2022, DOI: 10.1021/acs.jmedchem.2c01097
导师介绍
符雷蕾
https://www.x-mol.com/university/faculty/186050
张岚
https://www.x-mol.com/university/faculty/186063
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号