核内自组装用于选择性杀灭骨肉瘤细胞
在癌细胞中通常可以观察到高表达的碱性磷酸酶(ALP)。与碱性磷酸酶(ALP)相关的酶促自组装常被用于癌细胞的细胞器靶向和选择性杀灭。近日,布兰迪斯大学的徐兵教授课题组设计了一类富亮氨酸磷酸化多肽,实现了骨肉瘤细胞的细胞核靶向和选择性杀灭。

图1. 磷酸化多肽细胞核内自组装示意图:多肽在细胞表面经ALP水解后自组装得到胶束,并经由内吞进入细胞,被ALP进一步水解后得到纳米带并在细胞核内与组织蛋白共组装(图中只画出了关键步骤)。图片来源:Angew. Chem. Int. Ed.
该磷酸化多肽作为ALP的作用底物,在ALP水解作用下依次自组装得到纳米胶束和纳米带。使用该多肽培养骨肉瘤细胞,可观察到多肽在细胞核内的富集,且多肽更多地富集在核仁内。研究证明,该富集过程伴随有细胞膜破裂、核膜破裂和肌动蛋白破坏等过程。通过研究细胞摄取方式,作者证明该多肽主要通过脂筏/小窝蛋白内吞路径进入细胞。蛋白组学研究证明,该多肽在细胞核内与组织蛋白发生了共组装作用。
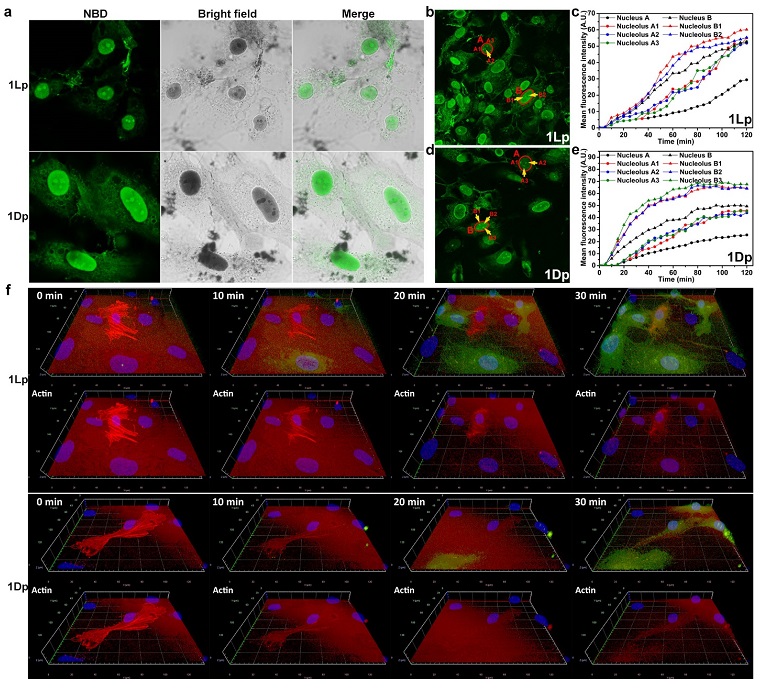
图2. a) 使用1Lp或1Dp(200 μM)孵育4小时后的SJSA-1细胞的共聚焦激光扫描成像图。b) 使用1Lp(200 μM)孵育SJSA-1细胞的共聚焦激光扫描时间成像图。c) b)图中选定区域的平均荧光强度随时间变化。d) 使用1Dp(200 μM)孵育SJSA-1细胞的共聚焦激光扫描时间成像图。e) d)图中选定区域的平均荧光强度随时间变化。f) 使用1Lp或1Dp与SJSA-1(RFP标记肌动蛋白)孵育0、10、20和30分钟后的3D共聚焦激光扫描显微图。图片来源:Angew. Chem. Int. Ed.
研究证明,该类磷酸化多肽对骨肉瘤细胞有选择性杀灭效果,可快速杀死骨肉瘤细胞的同时对正常细胞和其他多种癌细胞表现低毒性。研究证明,细胞的死亡模式综合了坏死、调亡和铁死亡等混合路径,且该细胞死亡被认为与之前提到的细胞膜破裂、核膜破裂和肌动蛋白破坏等过程密切相关。通过长时间反复刺激骨肉瘤细胞,作者尝试引发细胞的耐药性,然而实验结果证明,该多肽不仅无法引发癌细胞的耐药性,反而使癌细胞对该多肽更加敏感。

图3. a) 与1Lp、1Dp、1L或1D孵育24小时后SJSA-1细胞的存活率。b) 与1Lp或1Dp(200 μM)孵育24小时后HS-5、HEK293、HeLa、HepG2、OVSAHO、A2780和A2780cis细胞的存活率。c) 加入PLC或DQB与1Lp或1Dp(200 μM)共孵育24小时后,SJSA-1细胞的存活率。d) 表达RFP的SJSA-1细胞和HS-5细胞混合体系使用1Lp或1Dp(200 μM)处理4小时后,表达RFP的SJSA-1细胞的比例变化。e) 加入不同细胞死亡通路阻断剂后SJSA-1和1Lp或1Dp(100 μM)孵育24小时后的存活率。SJSA-1细胞被f) 1Lp或g) 1Dp长时间(5周)处理筛选后,被各自多肽处理后的存活率。图片来源:Angew. Chem. Int. Ed.
综上所示,该项研究提供了一种新的细胞核靶向策略,也为选择性杀死癌细胞且避免产生化疗耐药性提供了有效的方法。
这一成果近期发表在Angewandte Chemie International Edition上,文章的第一作者是武汉理工大学青年教师刘爽博士。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Intranuclear Nanoribbons for Selective Killing of Osteosarcoma Cells
Shuang Liu, Qiuxin Zhang, Hongjian He, Meihui Yi, Weiyi Tan, Jiaqi Guo, and Bing Xu*
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202210568
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号