云南大学高峰研究组Angew:双核钌配合物借助民用低能红外激光器在体内实现红外双光子光动力/光热协同抗肿瘤治疗
钌配合物类光敏剂借助优异的双光子吸收性质,能够在红外光激活下实现肿瘤的光动力学治疗。然而,当前所使用的激光器为昂贵的高强度红外激光器,其辐射峰值远超皮肤所能承受的最大光辐射量,从而不可避免地造成皮肤等组织损伤。另外,该种激光器只能在焦点范围使用,照射面积极小(<1 mm2),需要激光低速移动(如1 mm/5 s)扫描整个实体瘤,耗费时间长,难以临床应用。同时,肿瘤单位面积接受照射仅有数秒,无法充分发挥光敏剂的作用。
云南大学高峰研究组率先尝试使用光径可调(~ 1 cm2)的民用低能红外激光器代替高能双光子激光器,借助全新设计的具有超高双光子吸收截面值的双核钌配合物作为光敏剂,实现了低能红外光激活的单线态氧在溶液、体外细胞和体内实体瘤中的生成,并实现TypeII型抗肿瘤光动力治疗。该激光足以覆盖整个实体瘤范围,从而使肿瘤部位在整个光治疗期间得到充分的照射,充分发挥出光敏剂的全部潜力。惊喜的是,该双核钌配合物具有以往单核钌配合物不具备的超高的光热转换效率,能够在小鼠体内实体瘤的低能红外激光治疗中产生10 ℃的温和升温,从而实现光动力和光热协同治疗。
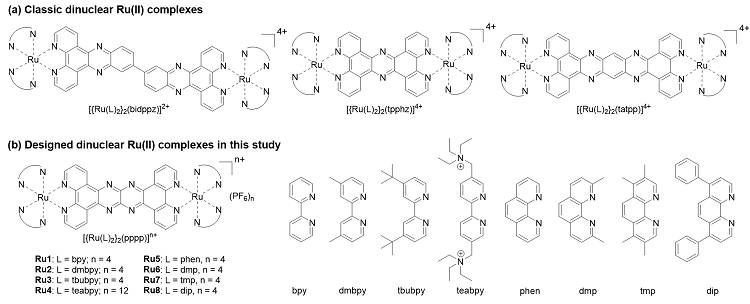
图1. 经典的和本研究所设计的双核钌配合物结构。图片来源:Angew. Chem.
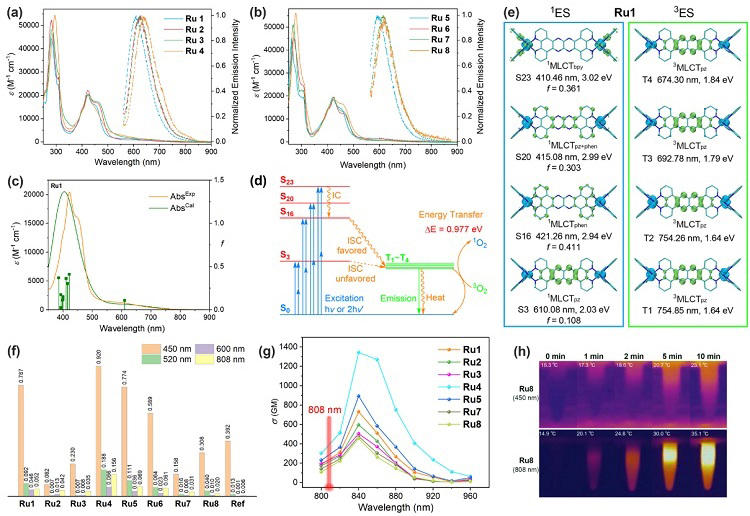
图2. 光物理和光化学性质。图片来源:Angew. Chem.
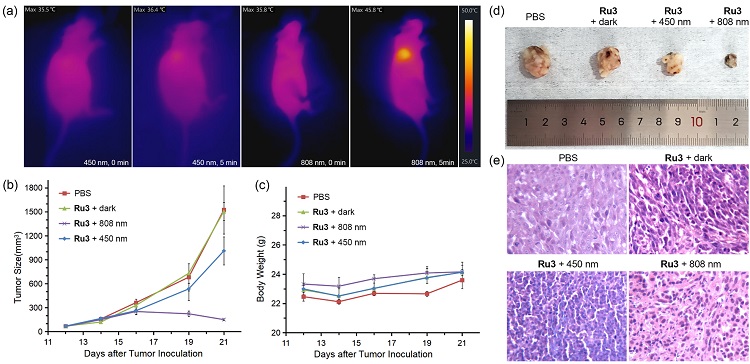
图3. 体内光动力/光热协同治疗。图片来源:Angew. Chem.
该类双核钌配合物以双核钌配合物特有的穿线结合方式结合双链DNA,表现为极强的DNA亲和力。意外的是,双核钌配合物几乎与线粒体选择性结合,而没有出现在富含DNA的细胞核内,推测是双核钌配合物相比于单核配合物更大的体积使得其难以跨过细胞核膜。进一步的死细胞染色研究表明,双核配合物几乎都集中在破裂的细胞核中,证实了推测。双核钌配合物的线粒体选择性既有利于提升其光细胞毒性,又有利于降低其暗细胞毒性(化学毒性),从而极大地提升了其作为抗肿瘤光动力学治疗试剂的能力。
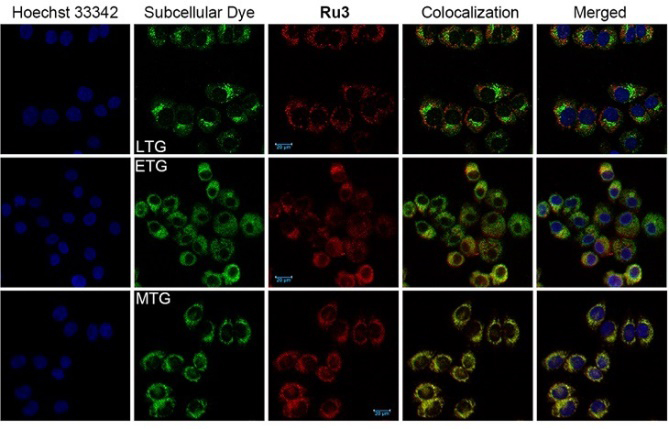
图4. 细胞共定位研究。图片来源:Angew. Chem.
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

In vivo Realization of Combined Photodynamic and Photothermal Therapy for Melanoma by Mitochondria Targeting Dinuclear Ruthenium Complexes under Civil Infrared Low-power Laser
Meng-Fan Wang, Rong Yang, Shi-Jie Tang, Deng Yu-Ang, Guo-Kui Li, Dan Zhang, Daomei Chen, Xiaoxia Ren, Feng Gao
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202208721
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号