Nature Physics:纳米界面上电化学势驱动的DNA纳米涡轮
导读:
近日,荷兰代尔夫特理工大学Cees Dekker 课题组报道了一种由跨膜电化学势驱动的DNA纳米转子。该工作首次在纳米尺度下构建了主动耗能的机械结构,其利用纳米尺度固体薄膜两侧的电势差或离子浓度差来驱动纳米转子的机械转动。该工作首次将宏观尺度的风车、水车中的涡轮结构引入了纳米尺度,为构建在纳米尺度下实现能量转化的电化学纳米引擎开辟了一个全新的途径。

纳米孔上的DNA纳米转子。图片来源 Cees Dekker Lab / SciXel
人类社会发展史可以说是一部能量转换引擎装置的进化史。数千年来,人类设计、使用了各式各样的机械结构,将自然界中存在的各种能量转化为可控可用的机械能。从最古老的风车,到现代的风力发电涡轮机,从在中华大地上延续千年的古水车,到当今社会不可或缺的水力发电机,每一次技术的革新都带来一次人类社会的变革。而这类转换能量、输出机械功的引擎装置不仅仅是推动人类社会发展的重要因素,更是众多生物生命活动的重要支柱。遍布生物界所有门类的ATP(三磷酸腺苷)合成酶就是这样的一个“机械结构”:它镶嵌在生物体内磷脂膜上(例如人类细胞线粒体内膜),将膜两侧的离子浓度差(一般为氢离子或钠离子)形成的化学势能转化为其自身中轴的机械旋转,进而驱动ATP的合成(图1)。此外,众多细菌的鞭毛运动也由类似的马达蛋白驱动,同样也是使用跨膜电化学势能作为能量来源。
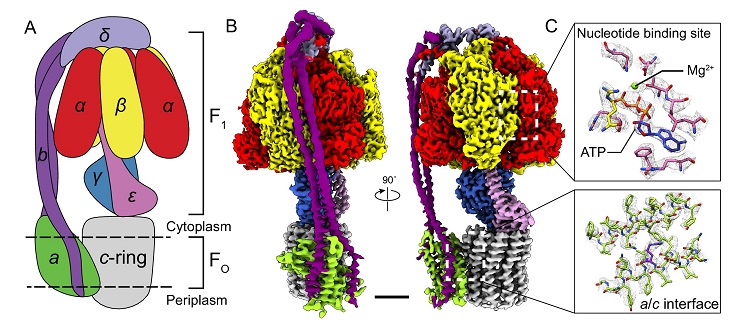
图1. ATP合成酶结构。图片来源:elife [1]
然而,我们仍未能充分利用在宏观尺度上建造流体驱动涡轮机械的经验,在纳米尺度下构建类似ATP合成酶这样的纳米涡轮结构。如果构建纳米涡轮引擎成为可能,其能使用电化学势(如离子浓度梯度)这一生命体中最广泛存在的能量来源作为驱动力,那么我们将迈入一个在纳米尺度下建造主动智能机器的新时代。
近日,荷兰代尔夫特理工大学Cees Dekker 课题组联合慕尼黑工业大学Hendrik Dietz课题组、德国马克斯普朗克研究所动态与自组织研究所Ramin Golestanian课题组,报道了这一领域的开创性突破:利用DNA折纸技术(DNA Origami)与纳米孔技术结合,构建了一个耗能持续单向旋转的纳米DNA转子(rotor)。该转子能够在直流电场或离子浓度梯度的作用下,在纳米孔上自组装、自构建为手性结构,首次实现了将薄膜两侧的电化学势能转化为转子转动的机械能。该成果发表在Nature Physics 上。代尔夫特理工大学师鑫博士为该文的第一作者。
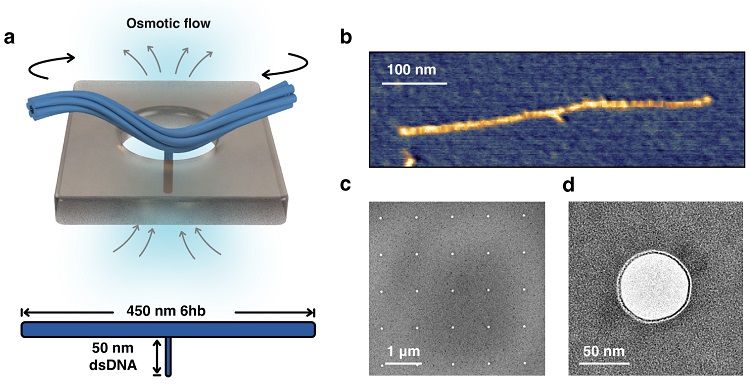
图2. 纳米孔上构建的自组装DNA转子。图片来源:Nat. Phys.
具体来说,作者利用DNA折纸技术将6条DNA链黏连成束作为转子,用荧光分子标记其两端以观察其运动,并利用微纳加工技术在20 纳米厚的氮化硅薄膜上制备约50 纳米直径的纳米孔阵列(图2)构建跨膜电化学势并作为转子转动的支架。作者首先在薄膜两侧外加直流电场,利用电泳作用将DNA转子运输至纳米孔上。由于DNA转子长度长于纳米孔直径,并且6条DNA链成束的机械强度使其在100 mV电压形成的电场下难以充分弯折而穿孔,多数DNA转子可以停留在纳米孔上。通过荧光超分辨单颗粒追踪技术,作者观察到了DNA转子在纳米孔上的运动,并且发现其显示出了明显的具有取向性的驱动转动,而非单一的随机布朗转动(图3)。
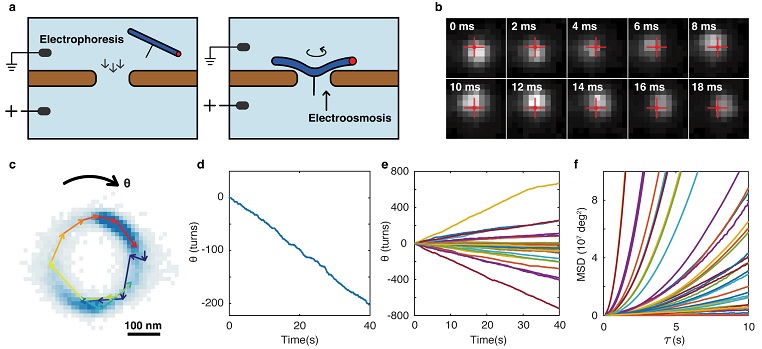
图3. DNA转子的持续定向转动。图片来源:Nat. Phys.
为了展示该自组装、自构建纳米转子的运行机理,作者通过双通道荧光实时测距,观察记录了DNA转子两端点的运动情况。实验显示该DNA转子在电场作用下,电场力使其发生机械形变,形成了稳定的手性结构。通过数值模拟,作者展示了电场下的DNA转子的可能形态。这些自组织形成的手性结构与纳米孔中电场引起的电渗流相耦合,从而将电势能转化为转子的机械旋转(图4)。
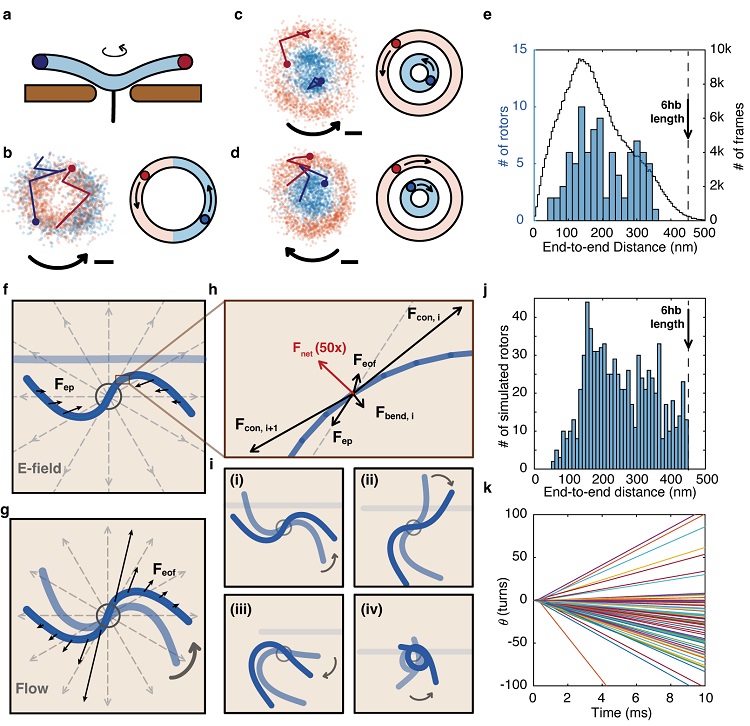
图4. DNA转子在纳米孔上形变构建为手性稳定结构。图片来源:Nat. Phys.
在自然界中,离子浓度差是比电场更加广泛存在的动力来源。因此,作者进一步移除外加电场,转而在膜两侧加入不同离子浓度的缓冲溶液。DNA转子在钠离子浓度梯度的驱动下同样会向纳米孔迁移,形变成为手性结构,并与盐浓度差引起的渗流耦合而旋转,由此将盐浓度梯度的化学势能转化为DNA转子的机械能。这一仿生过程重现了ATP合成酶将离子浓度差形成的化学势能转化为蛋白机械转动的生化过程(图5)。
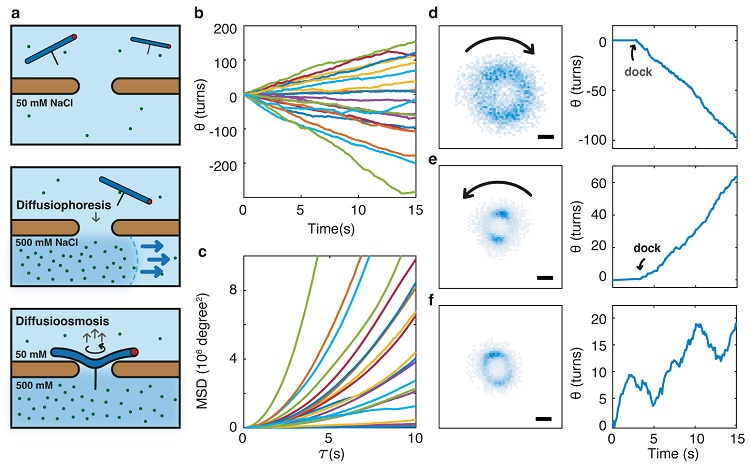
图5. Na+离子浓度梯度驱动DNA转子持续定向转动。图片来源:Nat. Phys.
小结
该工作从原理上开创了一类全新形式的纳米马达:纳米涡轮,即利用纳米尺度下的流体来驱动的纳米马达机械旋转结构。这一全新形式的纳米马达可以直接利用生物体中最广泛存在的离子浓度梯度作为能量来源,使我们距离构建可在生物体乃至人体中工作的纳米机器人的目标更进一步,并有望为体内传感、诊断、微创治疗开启一条全新的途径。
然而,目前这一工作仍存在一定局限:DNA转子结构是在纳米孔上自主形变形成的,其手性方向、形状等都无法直接调控。下一步本文作者将研究如何构建主动设计的纳米涡轮结构,以实现方向可控、速度可调、扭力可变的纳米电化学涡轮机。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Sustained unidirectional rotation of a self-organized DNA rotor on a nanopore
Xin Shi, Anna-Katharina Pumm, Jonas Isensee, Wenxuan Zhao, Daniel Verschueren, Alejandro Martin-Gonzalez, Ramin Golestanian,* Hendrik Dietz, * Cees Dekker*
Nat. Phys., 2022, DOI: 10.1038/s41567-022-01683-z
限时免费阅读链接:https://rdcu.be/cS3OD
参考文献:
1. Guo, H., Suzuki, T., & Rubinstein, J. L. (2019). Structure of a bacterial ATP synthase. elife, 8, e43128
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号