基于细胞表面精细生物偶联的微液滴-SERS平台用于单细胞外泌因子分析
注:文末有研究团队简介及本文科研思路分析
单细胞分析技术正在迅速发展,以解码不同水平的细胞异质性,并更好地了解细胞生理学。然而,由于单细胞的外泌体或外泌因子非常微量,因此需要建立高灵敏度的分析方法才能满足单细胞分析的挑战。以往研究单个细胞的特性可以通过流式细胞术进行量化,从而破译了细胞之间的差异;但这一方法是给定时刻状态的快照分析,对于细胞的历史以及随时间发展状态无法实现持续追踪。吉林大学超分子结构与材料国家重点实验室徐抒平教授团队多年来致力于发展基于微液滴-表面增强拉曼散射(SERS)的分析方法(Anal. Chem., 2019, 91, 2551-2558; Anal. Chem., 2019, 91,15484-15490),以探索了多种新型高灵敏的单细胞分析技术。
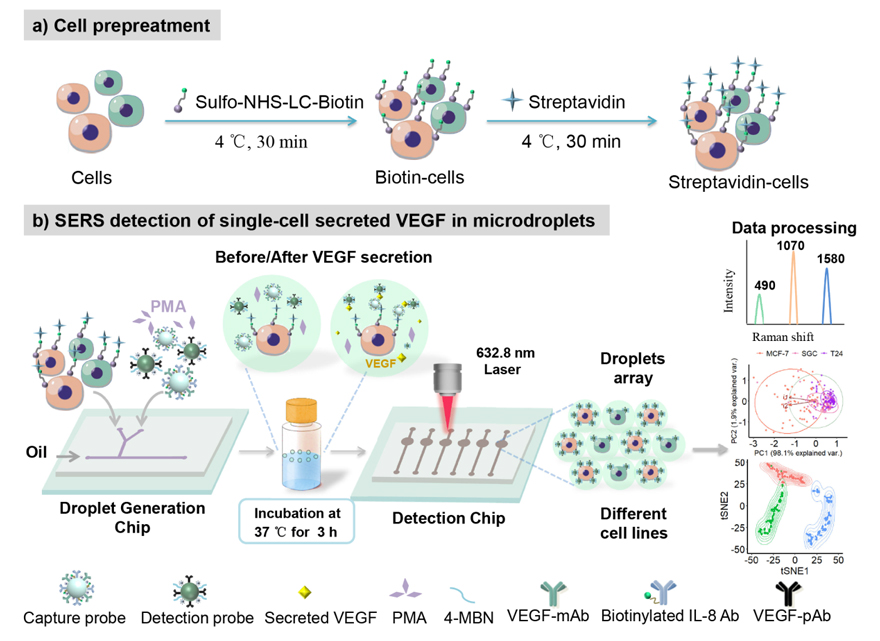
图1. 细胞预处理的工作流程,以及基于细胞表面生物偶联的微液滴-SERS分析平台用于单细胞外泌VEGF分析。图片来源:Anal. Chem.
最近,徐抒平(点击查看介绍)团队与吉林大学第一医院泌尿外科王伟刚副教授(点击查看介绍)合作开发了一种高灵敏度的SERS传感方法,通过在探针细胞表面精细的生物偶联,在微液滴-SERS平台上进行单细胞的细胞外泌因子分析。该微液滴-SERS平台集成了单细胞微流控液滴分离和SERS测量的双重功能,可将两类免疫纳米探针(捕获探针和SERS探针)与单个细胞一起包裹入微液滴中。通过捕获外泌因子将SERS探针锚定在目标细胞的膜蛋白表面,形成免疫三明治结构,实现细胞因子在细胞膜表面的富集效应和SERS探针的信号放大效应。应用该单细胞分析平台对不同细胞系(MCF-7、SGC和T24)的血管内皮生长因子(VEGF)进行异质性分析。采用化学计量学方法(PCA(主成分分析)和t-SNE(t分布随机邻域嵌入算法))对SERS数据进行解析,利用支持向量机(SVM)对判别模型进行检验。这些化学计量学方法的运用成功地识别出三种癌细胞系在细胞因子分泌能力方面存在显著差异,揭示了细胞异质性。这项工作证明了基于细胞表面生物偶联策略进行单细胞外泌因子分析的可行性。检测过程实现目标细胞锁定,也为未来成功实现单细胞分选提供极大便利。该平台为使用单细胞外泌因子作为生物标志物进行癌症早期诊断提供了实验依据,并为了解单细胞分泌物提供生理线索。
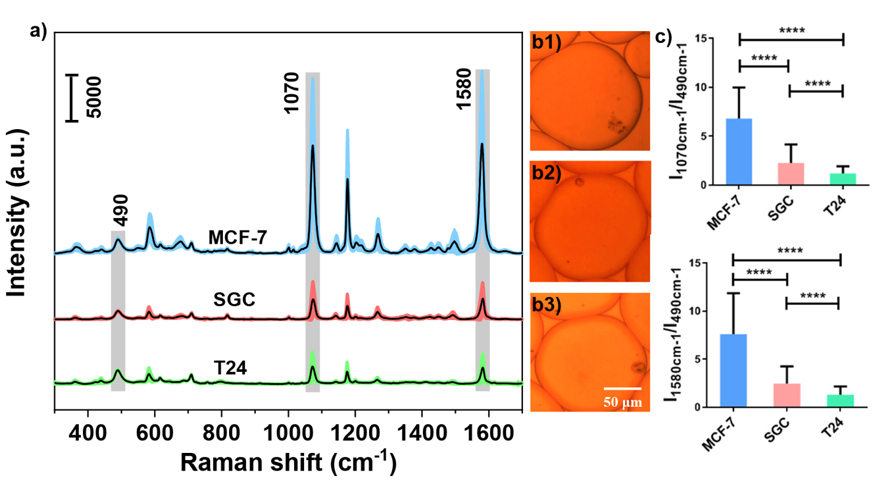
图2. 捕获探针、SERS探针和药物PMA与单个细胞在液滴中孵育3 h后的SERS光谱以及相对峰强的对照图。图片来源:Anal. Chem.
这一成果近期发表在Anal. Chem.上,文章的第一作者是吉林大学博士研究生丛丽丽,通讯作者为徐抒平教授、王伟刚副教授。该研究还受到吉林大学药学院梁重阳副教授团队、吉林大学分子酶学工程教育部重点实验室施维教授团队、长春长光辰英生物科学仪器有限公司的大力支持。该工作受国家自然科学基金(21873039, 22173035,21827805),长春光机所应用光学国家重点实验室开放课题(SKLAO2021001A14)、吉林大学交叉融合创新项目(JLUXKJC2020106)、吉林省健康科技创新项目(2019J020)和吉林省科技发展项目(20200403077SF和202104099YY)资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Microfluidic Droplet-SERS Platform for Single-Cell Cytokine Analysis via a Cell Surface Bioconjugation Strategy
Lili Cong, Jiaqi Wang, Xinli Li, Yu Tian, Shizhi Xu, Chongyang Liang, Weiqing Xu, Weigang Wang*, and Shuping Xu*
Anal. Chem., 2022, DOI: 10.1021/acs.analchem.2c01249
导师介绍
王伟刚
https://www.x-mol.com/university/faculty/340447
徐抒平
https://www.x-mol.com/groups/xushuping
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:以往基于微液滴的单细胞分析技术,都需要额外的载体(例如聚合物微球、磁珠、或者另一个细胞),需要将这些载体与目标细胞以及传感纳米探针同时包裹入单液滴中,且要保证每个液滴中仅有一个载体和一个细胞。这在液滴制备过程中具有非常大的难度,会出现大量只有载体或只有一个细胞的无效液滴。因此我们一直思考,是否可以摆脱对载体的依赖,从而在目标细胞本身上做文章,就将目标细胞当做载体,合二为一。
Q:研究过程中遇到哪些挑战?
A:若实现合二为一的目的,我们需要在细胞表面设计传感策略。这需要在细胞外膜表面进行接枝和修饰。这对于细胞活性以及细胞功能是否有影响是我们最为担心的。为此,我们探索了多种细胞膜上进行修饰和改性的方法,既保证细胞膜不受破坏,更要防止这些纳米级的探针被细胞内化入胞。在多次尝试失败之后,最终找到利用细胞膜蛋白表面生物素化的策略,成功实现在细胞膜表面构筑三明治传感策略。实验结果表明细胞在表面修饰之后仍然具有高活性;而且该方法为细胞膜表面带来一定的电荷可有效地解决纳米探针内化的问题。
Q:该研究成果可能有哪些重要的应用?哪些领域的企业或研究机构可能从该成果中获得帮助?
A:该方法最大的好处是将检测锁定在目标细胞自身上,我们称之为“target following”的模式。即使液滴破碎,我们依然可以锁定我们感兴趣的目标细胞,方便我们对目标细胞进行分选。在依赖载体的单细胞分析中,一旦液滴破碎,目标细胞和载体失去空间上的关联,目标细胞就追踪不到了。单细胞分析将来会跟单细胞测序进行对接,该方法将对单细胞外泌物分析,特别是对基于杂交瘤分析的单抗筛选是一项非常适用的工具。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号