去酰基化酶经GCE技术改造共价结合巴豆酰修饰
蛋白质巴豆酰化(lysine crotonylation,Kcr)是一种非常重要的赖氨素酰化的修饰类型,由芝加哥大学赵英明教授团队在组蛋白的翻译后修饰中发现,其在表观遗传方面发挥着不可或缺的调控功能。近年来的研究表明,Kcr参与了调控精子形成、急性肾损伤、HIV潜伏等多种生物学过程。相比于经典的赖氨酸乙酰化等修饰,Kcr在细胞内的丰度很低,并且目前基于抗体等检测和富集策略存在特异性不足、识别效率低的问题。针对该挑战,天津大学/南开大学轩维民(点击查看介绍)课题组与中科院大连化学物理研究所秦洪强(点击查看介绍)团队合作提出了蛋白酶结构域导向的邻近化学交联策略,设计并构建了共价结合蛋白质巴豆酰修饰的去酰基化酶变体,用于巴豆酰化的靶向检测(图1)。
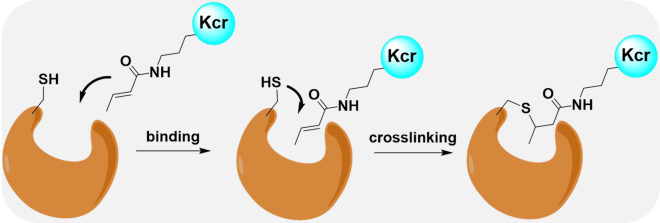
图1. 基于蛋白质的巴豆酰修饰共价交联体的工作原理
研究团队首先对Kcr的结构分析,发现其存在的不饱和双键反应活性较弱,难以与谷胱甘肽和半胱氨酸等巯基进行共价反应。蛋白质的微环境直接影响功能团的反应活性,基于此,研究者设想是否可以通过对特定蛋白质进行改造,实现巯基与Kcr不饱和双键的共价交联。大肠杆菌中的CobB蛋白具有广泛的去酰基化酶活性和底物序列容忍性宽的特征,研究团队通过基于基因密码子扩展技术对其进行特定位点的改造,即在其结构中引入具有巯基的非天然氨基酸(pTMF和mTMF),利用CobB与巴豆酰化蛋白质的结合所导致的邻近效应促使了巯基与巴豆酰基的迈克尔加成反应,实现了CobB变体与巴豆酰化蛋白质的共价结合。数据表明,该交联反应具有效率高、识别特异性强等优势,并且表现出了严格的NAD+依赖性(图2),实现了该交联反应的可控性,有效降低了背景干扰与假阳性。
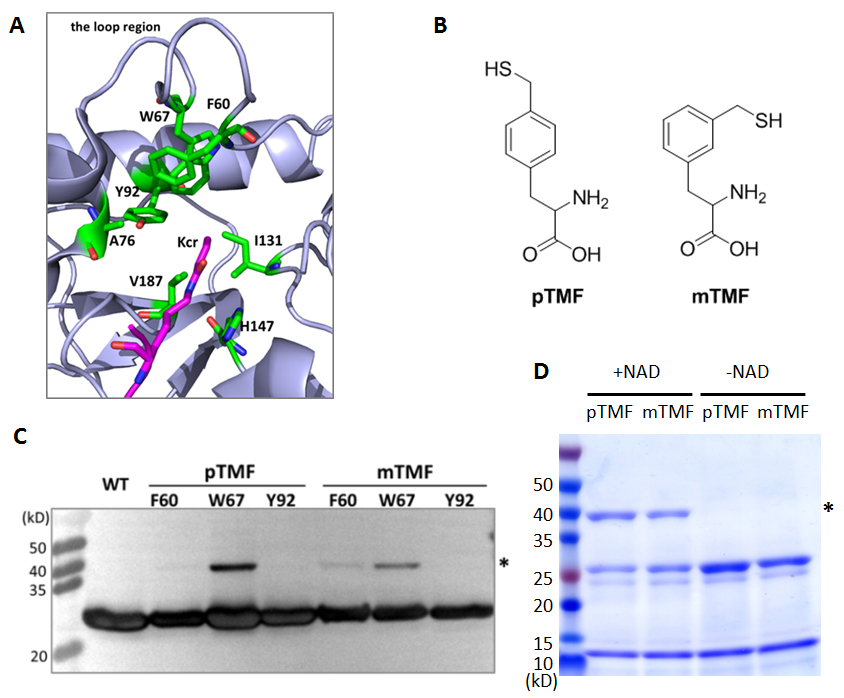
图2. A. CobB底物结合口袋的结构,PDB:6RXL;B. 非天然氨基酸pTMF和mTMF的化学结构式;C. CobB变体与巴豆酰底物共孵育后的western blot结果;D. CobB-H147A-W67ncAA与巴豆酰蛋白交联反应具备NAD+依赖性
进一步将该CobB变体(CobB-H147A-W67pTMF)用于细胞中组蛋白样品的巴豆酰化修饰检测(图3A)和原位免疫荧光研究(图3B),其在复杂生物样品依旧呈现了优异的识别特异性与NAD+依赖特征。该工作为巴豆酰修饰的基础研究提供了有力工具,同时对于其它类型赖氨酸酰基化修饰的相关研究具有借鉴意义。
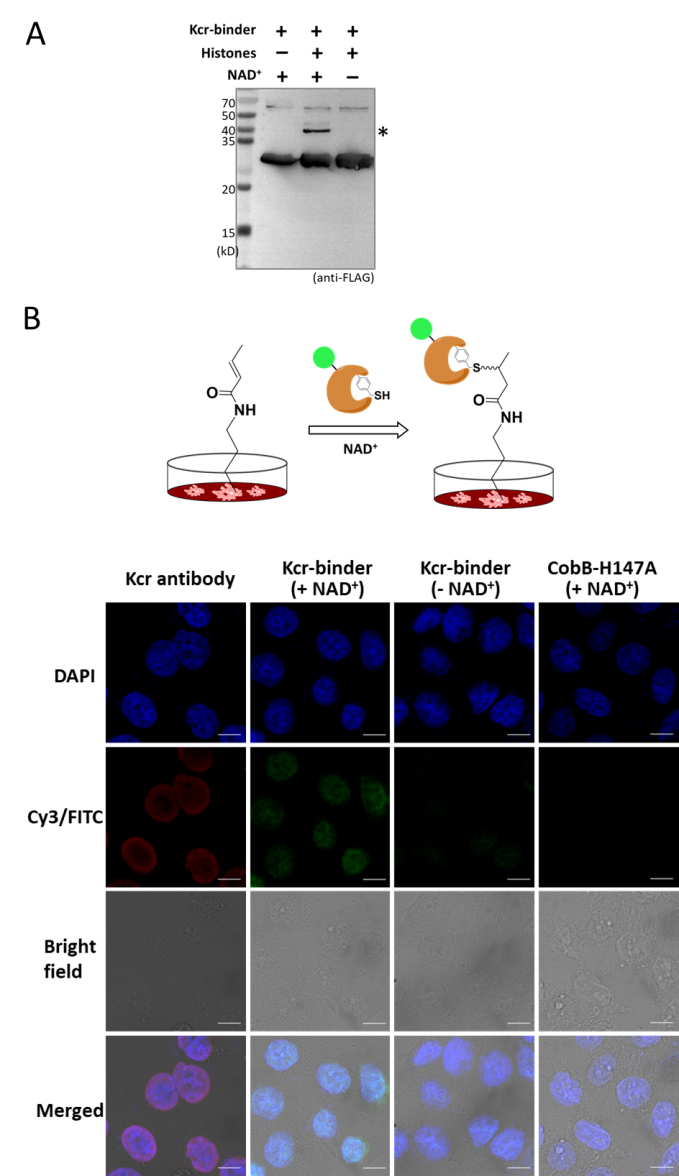
图3. Kcr-binder在巴豆酰修饰研究中的应用
这一工作发表在Angewandte Chemie International Edition 上,文章第一作者是南开大学博士研究生冀艳丽,轩维民研究员和秦洪强研究员为共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Sirtuin-Derived Covalent Binder for the Selective Recognition of Protein Crotonylation
Yanli Ji, Lin Sun, Yao Chen, Hongqiang Qin, Weimin Xuan
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202205522
导师介绍
轩维民
https://www.x-mol.com/university/faculty/63647
秦洪强
https://www.x-mol.com/university/faculty/202280
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号