JACS:钙铝双金属氢氧化物用于骨质疏松症的治疗
本文转载自“倪大龙课题组”公众号
目前全世界超过10亿人罹患各种程度的骨质疏松症,而现有的药物通常具有较大的副作用,因此急需新型的治疗方法。首先,患者的破骨细胞会大量分泌氢离子,患处局部为酸性微环境(pH大概为4),促进了骨中有机基质的降解,从而进一步恶化骨质疏松。另一方面,促炎的免疫细胞(比如Th17)和过量的促炎细胞因子(IL-6、IL-17、RANKL、THF-α)也会促进破骨细胞的形成。因此对于骨质疏松症的治疗要从两个方面入手,一是改善酸性微环境,二是改善炎症微环境。
基于这些考虑,最近上海交通大学医学院倪大龙课题组与中科院上海硅酸盐研究所施剑林院士、胡萍研究员合作在J. Am. Chem. Soc.在线发表论文,报道了一种钙黄绿素修饰的钙铝双金属氢氧化物纳米片(CALC nanosheets)。其中钙黄绿素起到靶向骨组织的作用;双金属氢氧化物(LDH)是一种常见的纳米材料,具有片层结构,双金属由一种二价离子和一种三价离子组成,组分可调性很强,因此广泛应用于催化和纳米医学等领域。如图1所示,本文中作者采用的是钙铝LDH,一方面可以消耗酸性微环境中的氢离子,另一方面反应后释放出的钙离子还会和磷酸根反应生成磷酸钙沉淀,可以促进生成抗炎的M2巨噬细胞和IL-10、TGF-β的分泌,并且召集大量调节T细胞来抑制Th17细胞的活性。

图1. 材料治疗骨质疏松症机理示意图。
LDH为粒径200-300纳米的薄片(图2b)。随着初始溶液pH的降低,LDH中的钙离子释放速度逐渐加快(图2g),并且溶液pH也逐渐恢复为中性(图2h)。

图2. 材料性能表征。
巨噬细胞RAW264.7在破骨诱导培养基中可以大量转化为破骨细胞,然而加入材料后只有少量破骨细胞生成(图3a)。材料和M2巨噬细胞培养基共同作用下,产生破骨细胞的数量更少了(图3a)。从凋亡实验可以看出,材料和M2培养液共同作用下破骨细胞大量凋亡(图3e)。Vinculin和鬼笔环肽染色显示材料处理后破骨细胞尺寸更小并且有更少的伪足小体(图3g)。
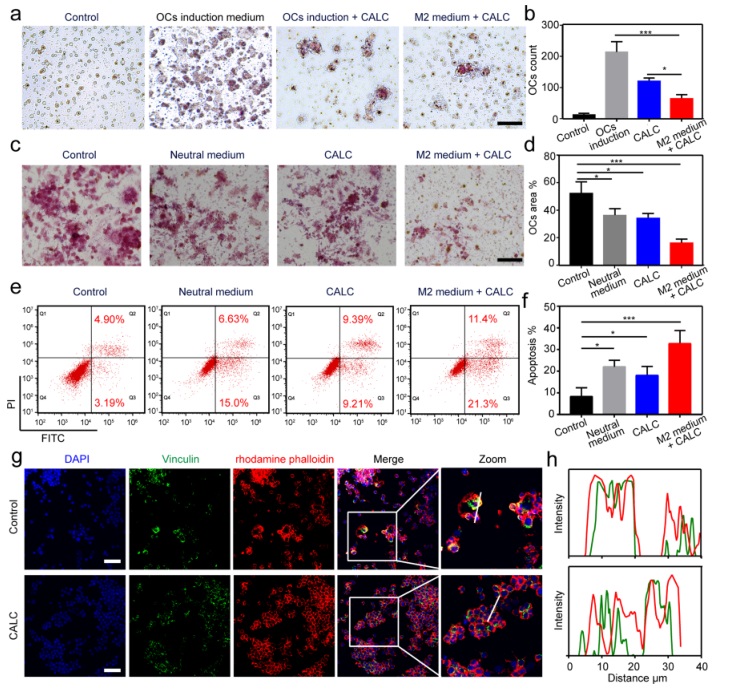
图3. 材料在细胞水平抑制破骨细胞转化的表征。
与IL-4相比,材料也可以有效的促进巨噬细胞的M2极化(图4a、c),并促进分泌大量抗炎因子IL-10(图4g)。这些因子还可以进一步促进成骨细胞的活性(图4h),并发生进一步的钙化和矿化(图4i)。

图4. 材料在细胞水平促进巨噬细胞极化和成骨分化的表征。
随后作者在活体水平验证材料的治疗效果。如图5b,microCT显示材料明显的阻止了老年小鼠的椎骨、股骨、胫骨的骨流失。H&E染色、Masson染色也表明材料治疗后的骨结构更完整,TRAP染色显示材料处理后骨组织中的破骨细胞减少(图6a)。同时,材料处理后骨组织中M2巨噬细胞增加,炎症细胞Th17减少,调节T细胞增加(图7a),说明材料可以调节骨组织的免疫微环境,增加抗炎细胞数量。

图5. 活体水平材料治疗骨质疏松症的效果

图6. 骨组织的H&E、Masson和TRAP染色

图7. 骨组织的M2巨噬细胞(CD206)、Th17细胞(IL-17)、调节T细胞(Foxp3)免疫染色。
综上所述,本研究中作者合成的钙铝LDH纳米片可以同时改善骨质疏松症的酸性微环境和炎症微环境,从而提高成骨细胞活性、抑制破骨细胞生成,最终实现了骨质疏松症的高效治疗。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Acid Neutralization and Immune Regulation by Calcium–Aluminum-Layered Double Hydroxide for Osteoporosis Reversion
Hao Fu, Lingtian Wang, Qunqun Bao, Dalong Ni*, Ping Hu*, and Jianlin Shi*
J. Am. Chem. Soc., 2022, 144, 8987–8999, DOI: 10.1021/jacs.2c00749
导师介绍
施剑林
https://www.x-mol.com/university/faculty/16222
欢迎关注倪大龙课题组公众号。课题组诚招博后和助理研究员,详见同时发布的招聘广告。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号