Nano Res.│南京大学郑鹏课题组;NGAL中非共价的cation-π相互作用的单分子力谱研究
本篇文章版权为郑鹏课题组所有,未经授权禁止转载。
背景介绍
Cation-π相互作用是阳离子和富电子芳烃之间的静电相互作用。它作为蛋白质折叠、稳定性和受体-配体相互作用/识别的重要驱动力,在许多生物系统中发挥着重要作用。目前,蛋白质中的cation-π相互作用大多是通过程序和理论计算进行统计分析来预测和发现的。由于缺乏高精度测量微小差异的手段,相关实验的验证和定量工作仍然非常有限。
成果简介 南京大学郑鹏教授课题组利用基于原子力显微镜的单分子力谱(AFM-SMFS)这一高精度的检测技术,通过半胱氨酸介导的位点特异性蛋白固定方法,测量了通过cation-π相互作用结合铁的蛋白质-中性粒细胞明胶酶相关脂质运载蛋白(NGAL)的稳定性及其三个阳离子残基与结合铁的儿茶酚之间的相互作用。两个不同拉伸位点(C122/C133)的力谱测量表明依赖于弱相互作用结合铁的NGAL具有更强的稳定性和动力学。这一工作实现了对NGAL中cation-π相互作用的高精度检测,揭示其结合的分子机制,也为理解蛋白质中普通存在的cation-π相互作用提供了一种新型的实验工具。 作者简介 郑鹏,南京大学化学化工学院教授,博士生导师。2008年获南京大学本科学位,2013年在加拿大不列颠哥伦比亚大学获得博士学位,之后在哈佛医学院从事博士后研究。2015年开展独立工作。主要利用单分子力谱研究蛋白的折叠、组装和相互作用。在病毒黏附、膜蛋白组装和金属对蛋白的调控等方向开展研究工作。课题组主页https://hysz.nju.edu.cn/pengzhenglab/。 文章信息 Jingyuan Nie, Yibing Deng, Fang Tian, Shengchao Shi & Peng Zheng*. Detection of weak non-covalent cation-π interactions in NGAL by single-molecule force spectroscopy. Nano Research https://doi.org/10.1007/s12274-021-4065-9. 识别二维码或点击左下角“阅读原文”可访问全文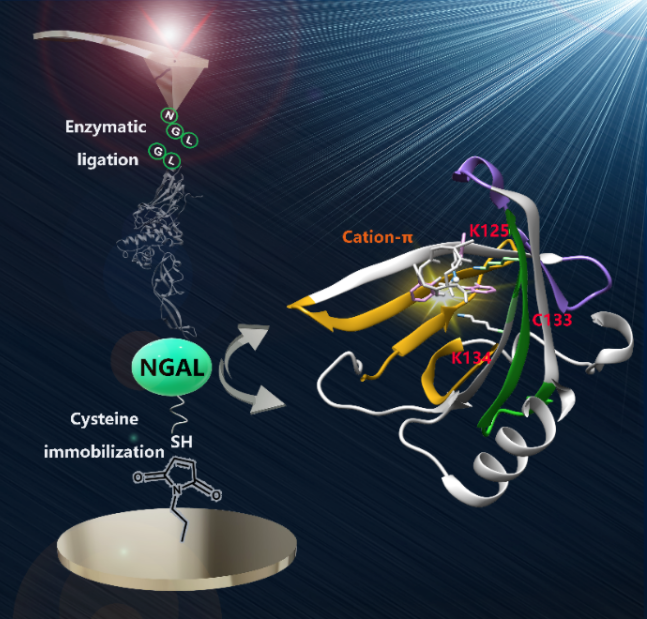


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号