“披金带甲”的破骨细胞治疗异位骨化
注:文末有本文科研思路分析
破骨细胞(OCs)能够在质子泵结构的局部形成高浓度“生物酸”酸化旧骨,是骨再吸收过程的关键所在。同时,该细胞可清除在骨吸收过程中释放的钙、磷酸盐、胶原片段等毒性的物质。然而,破骨细胞由于在异位钙化组织周围的活性低,限制其直接应用于异位骨化(HO)的治疗。异位骨化是一种异常普遍的现象,严重威胁患者的行动能力与健康。目前临床上针对异位钙化主要以抑制、延缓钙化进一步发展或手术治疗,对已形成的异位钙化仍然缺乏有效的可逆性治疗手段。
早在2008年,浙江大学唐睿康团队就提出了细胞表面工程化策略,通过在酵母菌表面层层自组装磷酸钙壳层以提高酵母菌的活性。自此以后,细胞表面工程作为一个全新的研究领域吸引了众多学者。尽管如此,在破骨细胞上修饰具有功能结构的材料壳层目前依然是一项艰巨的挑战。因此,如何利用材料的修饰,保留天然细胞人工不可复制的功能,同时赋予其新的功能,让其应用在更多的领域中,发展更多的细胞疗法是一项具有挑战性的工作。
浙江大学化学系唐睿康教授(点击查看介绍)与浙江大学医学院附属口腔医院谢志坚教授(点击查看介绍)研究团队合作,通过细胞工程化的策略,利用骨靶向的药物(四环素)对破骨细胞进行封装,制备获得四环素工程化的破骨细胞(TC-OCs)。通过细胞表面的四环素分子提高其对钙化组织的粘附力及靶向性,以此提升破骨细胞对异位钙化的酸噬能力。体外结果表明该工程化破骨细胞对异位钙化组织展现出了优异的靶向和粘附作用(提升到约3倍)。体内实验中,通过建立多种异位骨化模型(分别是手术模型、肌内模型和遗传模型)分别进行验证其治疗效果,结果均表明TC-OCs能够显著减少异位骨体积。这一方法无需手术即可去除跟腱异位骨化,有望解决异位钙化以往无法进行可逆性治疗的局限性,也展现了工程化细胞作为“活性治疗剂”的应用前景。
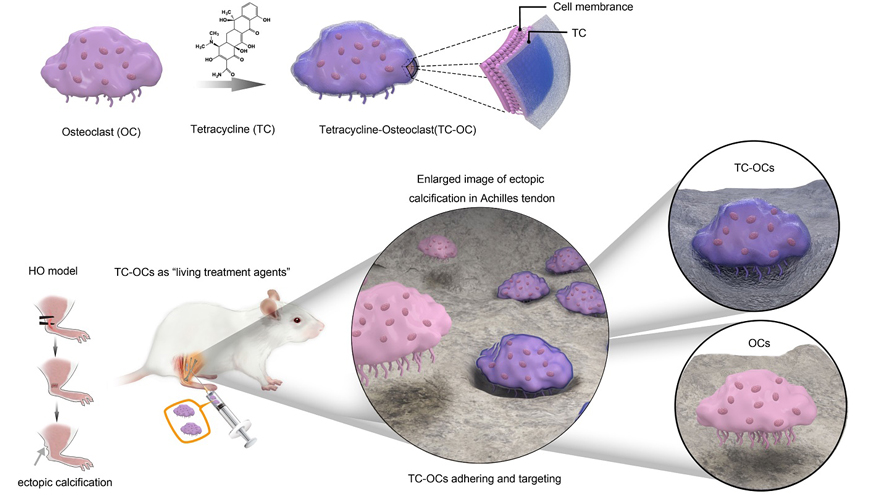
图1. 工程化的破骨细胞的制备方法及“吃掉”异位骨化的示意图。图片来源:Nat. Commun.
这一成果近期发表在Nature Communications,文章的第一作者是浙江大学博士后靳文静。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Engineered osteoclasts as living treatment materials for heterotopic ossification therapy
Wenjing Jin, Xianfeng Lin, Haihua Pan, Chenchen Zhao, Pengcheng Qiu, Ruibo Zhao, Zihe Hu, Yanyan Zhou, Haiyan Wu, Xiao Chen, Hongwei Ouyang, Zhijian Xie*, Ruikang Tang*
Nat. Commun., 2021, 12, 6327, DOI: 10.1038/s41467-021-26593-1
导师介绍
唐睿康
https://www.x-mol.com/university/faculty/14397
谢志坚
https://www.x-mol.com/university/faculty/71194
科研思路分析
Q:这项研究最初的想法是如何产生的?
A:课题组一直以来关注细胞表面工程化领域,致力于发展更多细胞疗法,并且发表了一系列重要研究成果。最初的启发来自利用病理性钙化治疗肿瘤,我们开始关注于异位钙化,目前异位钙化现有治疗策略为抑制或延缓钙化进一步发展,对于已形成的钙化组织需手术治疗,同时面临着复发的可能性。那么,钙化能否可逆性地去除?众所周知,破骨细胞(OCs)作为体内骨吸收过程中的独特细胞,可局部释放出大量“生物酸”,同时可清除钙、磷酸盐、胶原片段等毒性物质。如上所述,破骨细胞在异位骨化(HO)中无法直接发挥作用。我们设想能否通过细胞工程化的策略提高其粘附力与靶向性以提升其在异位组织环境中的酸噬能力。令人惊喜的是,通过工程化的策略, TC-OCs能够显著减少异位骨体积,这一结论在多种异位骨化模型中得到了初步的验证。
Q:研究过程中遇到哪些挑战?
A:本项研究最大的挑战是如何对破骨细胞进行工程化,找到工程化的最优条件。在这个过程中,我们团队在细胞表面工程化方面的经验积累起了至关重要的作用。破骨细胞的良好活性是工程化的前提,我们团队虽一直关注化学生物学领域,但破骨细胞的诱导技术对于起初的我们也是一项巨大的挑战,我们团队与浙江大学邵逸夫医院骨科团队合作攻克难关。
Q:该研究成果可能的重要应用及未来的发展方向?
A:该四环素工程化的破骨细胞可用于可逆性治疗异位骨化,这一结论在我们的实验中得到了初步的概念性验证。但应用到临床还有很长一段路要走,期待有更多通过化学生物学方法改造细胞的手段,赋予破骨细胞更多新的功能,并在其他部位的病理性钙化中探索其应用的可能性。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号