纳米金/含刚性DNA三角形外层多功能壳的核壳型结构及其作为siRNA癌症靶向递送载体研究
注:文末有研究团队简介及本文科研思路分析
在癌症治疗中,抗癌药物的脱靶副作用和免疫原性等通常是药物治疗所面临的急需解决的问题。近日,福州大学的吴再生教授(点击查看介绍)团队,构建了一种纳米金/含刚性DNA三角形外层多功能壳的核壳型结构siRNA/Ap-CS,用于靶向运载siRNA药物,能够提高siRNA药物的抗血清稳定性和靶向递送能力,通过设计刺激-响应药物释放机制,实现高效的肿瘤细胞基因调控与靶向治疗。这一成果发表在Nature Communications 上,第一和第二作者分别是福州大学博士后薛昌博士和福州大学硕士研究生胡舒瑶,吴再生教授是论文通讯作者。
RNA干扰(RNA interference, RNAi)是一种能够调控人类约30%基因表达的内源性调控途径,是由小干扰RNA(small interfering RNA, siRNA)触发的高特异性调控过程。由于RNA在生理环境中很脆弱,容易降解,递送载体的构建是siRNA核酸药物在临床治疗中获得应用的关键。例如,全球首款siRNA药物Onpattro (patisiran) 通过脂质体作为载体而用于遗传性ATTR(hATTR)淀粉样变性成人患者第1阶段或第2阶段多发性神经病的治疗。然而目前的载体,包括脂质体在内,仍存在毒副作用、免疫原性或非特异性吸附等相关的副作用。构建癌症组织靶向递送、能对特定刺激做出响应而释放药物、低毒性的多功能纳米载体,实现病变组织的精准治疗,在癌症的临床应用中具有重要的意义。金纳米粒子的免疫原性比脂质类载体低25倍,具有较高的生物相容性,在药物及载体领域中发挥了积极作用。例如,金纳米颗粒药物在类风湿性关节炎的治疗中应用近60年。近40年,核酸纳米材料及其组装技术得到了迅速发展,DNA作为一种新型的生物材料得到了广泛关注。由于碱基互补配对特性,DNA纳米材料具有高度的可编程性,结合功能核酸探针,具有高选择性、高亲和力、高生物相容性、易合成等优势,在生化分析、生物成像、靶向给药等生物医药领域具有极高的应用前景。
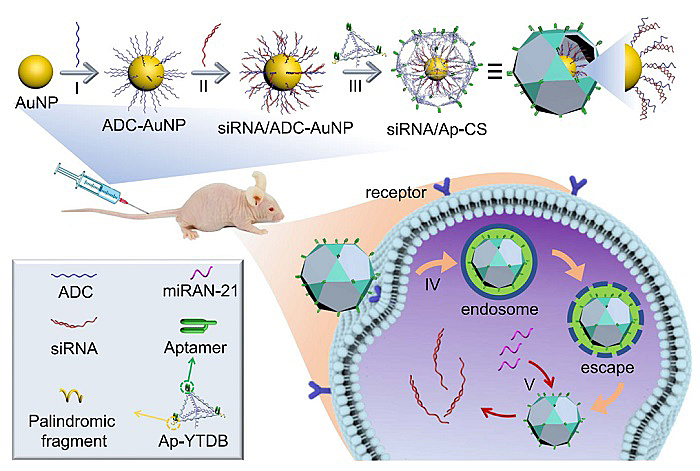
利用金纳米颗粒为核、中层自组装DNA为骨架负载siRNA、外层刚性DNA三角形为抗降解保护壳、核酸适体为靶向分子,福州大学吴再生教授团队构建了siRNA/Ap-CS核壳型纳米结构药物载体。具体来说,以35 nm的金纳米颗粒 (AuNP) 为核,在纳米金表面修饰DNA单链 (ADC),形成AuNP-ADC;通过与ADC靠近金表面的片段杂交,装载siRNA,而ADC外侧片段用于抗降解保护外壳的安装。外壳保护层的基本结构单元是刚性的DNA三角形,三个顶点含有相同的核酸回文片段,使基本结构单元互相交联,在外表面形成一层DNA外壳。同时,在刚性三角形的中心安装核酸适体,用于对肿瘤细胞的特异性识别,构建成纳米金内核、DNA-diRNA中层和三角形-适体外层的核壳型结构siRNA/Ap-CS。
通过适体介导的特异性识别与细胞内化过程,siRNA/Ap-CS进入肿瘤细胞内部,细胞内的特征分子microRNA能够与ADC优先杂交,释放siRNA,以此形成刺激-响应药物释放过程。通过PCR、蛋白质印记、细胞活性测试等技术手段,验证了siRNA/Ap-CS能够对靶标mRNA、蛋白质具有高效的沉默作用,产生肿瘤杀伤效果。同时,在细胞水平以及活体水平对siRNA/Ap-CS的治疗效果做了验证。研究表明,所构建的siRNA/Ap-CS具有良好的生物相容性以及理想的抗血清降解能力,能够在活体水平运载siRNA药物,并发挥基因调控作用。该课题的研究为生物医药纳米材料的研发、肿瘤的靶向治疗提供了重要的技术支撑和设计思路。

该课题研究得到国家自然科学基金委员会项目(21775024)、福建省自然科学基金项目(2019J02005)等基金项目的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Programmably tiling rigidified DNA brick on gold nanoparticle as multi-functional shell for cancer-targeted delivery of siRNAs
Chang Xue, Shuyao Hu, Zhi-Hua Gao, Lei Wang, Meng-Xue Luo, Xin Yu, Bi-Fei Li, Zhifa Shen & Zai-Sheng Wu
Nat. Commun., 2021, 12, 2928, DOI: 10.1038/s41467-021-23250-5
吴再生教授简介

分析化学博士,福州大学教授、博导,国家级青年人才,福建省高层次创业创新人才(百人计划),福建省闽江学者奖励计划特聘教授;能源与环境光催化国家重点实验室青年骨干,生物药光动力治疗技术国家地方联合工程研究中心与福建省肿瘤转移药物干预重点实验室骨干成员,福州大学肿瘤转移预警与预防研究所所长。原985高校湖南大学研究生导师、化学生物传感与计量学国家重点实验室固定成员、加拿大麦克马斯特大学国际人才专项特聘博士后研究员、全国优秀博士学位论文提名作者。在功能核酸探针、核酸纳米器件及细胞和活体成像等领域发表SCI论文100多篇;其中,在Nat Commun、J Am Chem Soc、Angew Chem Int Ed与Nucleic Acids Res 等中科院JCR一区期刊SCI论文有90多篇。曾获福建省青年科技奖与湖南省化学化工会青年化学化工奖等奖项。入选过河南省高等学校特聘教授,担任过南非国家基金委员会基金评审专家与多种国际高质量期刊常年审稿专家、特邀撰稿人,是获得加拿大麦克马斯特大学Michael G. DeGroote国际人才重点专项基金的第一位中国学者(年度头条新闻与常年滚动新闻特访)。主持海外项目、国家级或其它级别项目10多项;是重大研究计划与重点项目等5项国家自科子课题负责人或骨干成员;实质性参与973计划及重大科学研究计划项目3项; 培养或联合培养硕博研究生80多名。
https://www.x-mol.com/university/faculty/9534
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:如上所述,在siRNA药物的应用中,载体的构建是关键。在这个研究领域,有很多研究者已经提出了诸多新颖的纳米材料用于siRNA运载。但是在应用中,还是会存在很多缺陷,例如毒副作用高,免疫原性强等缺陷。为了降低毒副作用及免疫原性我们构建了纳米金-刚性DNA三角形外壳的多功能核壳结构,希望能够降低了化疗药物的毒副作用和免疫原性,同时提高siRNA的生物稳定性以及药物释放效果,推动siRNA药物的临床应用。
Q:研究过程中遇到哪些挑战?
A:本课题最大的挑战就是针对需要解决的问题,如何设计一个载体系统和智能控制系统相结合的平台,能够在siRNA运载中,既能满足高效运载siRNA、提高siRNA稳定型,靶向肿瘤细胞,又能促进siRNA在细胞内的有效释放。
Q:该研究成果可能有哪些重要的应用?哪些领域的企业或研究机构可能从该成果中获得帮助?
A:我们构建的纳米金-刚性DNA三角形外壳的多功能核壳结构具有良好的生物相容性和优良的抗血清降解能力,在复杂的生物环境中能够精准的将siRNA输送至病变组织并发挥基因调控作用,实现基因调节与治疗。为siRNA的载体构建、药物研发等提供了很好的借鉴思路。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号