Adv. Mater.┃NIR辐照诱导的温热疗法用于克服肿瘤铂类药物的级联耐药
化疗耐药是癌症治疗中一个长期存在的问题。该问题的机制涉及细胞膜转运、药物抑制、药物解毒、DNA修复等,往往是一个多步骤的级联过程。以临床上常见的铂类药物为例,其耐药机制为一级联过程,包括细胞对药物的摄取减少、细胞内谷胱甘肽对药物的解毒增强、细胞核中Pt-DNA加合物的形成被抑制等,这种多步骤的级联过程造成的耐药被称为“级联耐药”。虽然学术界已开展了一些工作,提出了抑制肿瘤铂类耐药的可行性策略,但其中的大多数方法仅仅针对一两个导致耐药的特定过程,而忽略了整体的级联过程,进而无法达到最佳的抗癌效果。因此,如何在治疗过程中系统性地针对肿瘤铂类耐药机制中涉及的所有关键步骤来设计新型载药体系目前仍较具挑战。
为了解决上述问题,中国科学院化学研究所张德清研究员(点击查看介绍)与肖海华研究员(点击查看介绍)课题组进行合作,设计合成了一种含有2,5-二氮杂并环戊二烯单元的新型光热聚合物DAP-F,并利用一种含二硫键的生物可降解性两亲聚合物P1制备出具有光热效应的纳米粒子F-NPs,协同四价铂小分子C16-CisPt(IV)-Suc制备的Pt-NPs构建最终的混合纳米体系F-Pt-NPs。该纳米体系在近红外光(808 nm)照射下产生的温热(43 ℃),可以增强肿瘤细胞细胞膜的通透性,进而促进肿瘤对药物的摄取,同时通过加速谷胱甘肽的消耗抑制顺铂失活,并通过增加Pt-DNA加合物的形成和抑制DNA的修复,最终促进肿瘤细胞的凋亡(图1)。
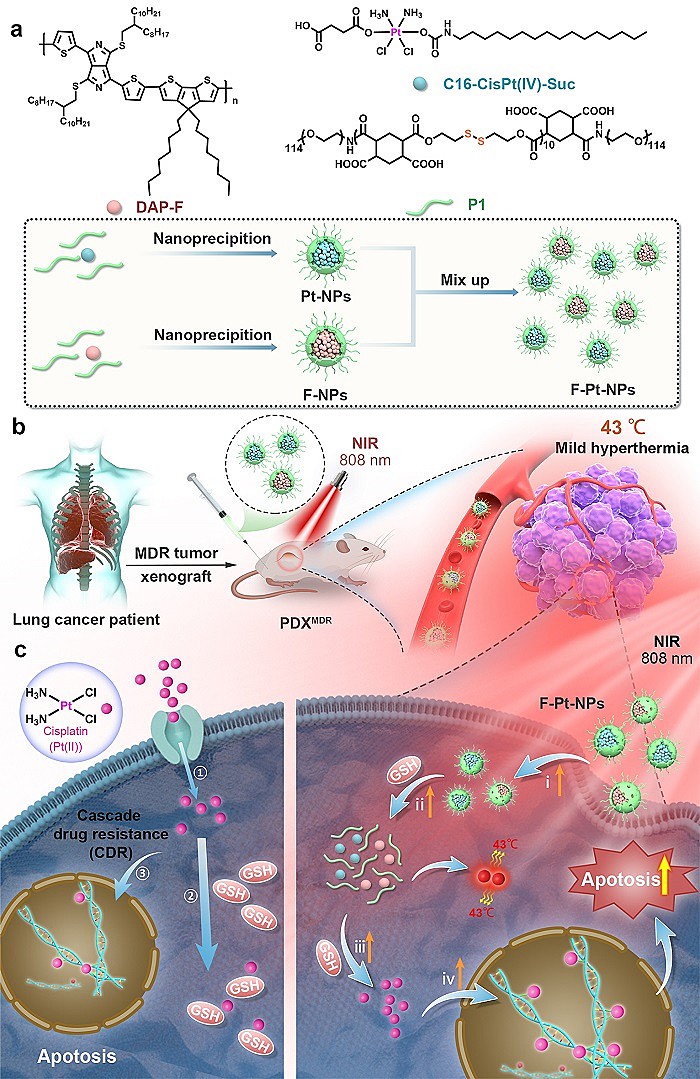
图1. 纳米体系F-Pt-NPs的制备及其在近红外光照射下逆转肿瘤铂类药物级联耐药。
相关研究表明在NIR辐射诱导的温热环境下,纳米体系F-Pt-NPs对耐铂药肿瘤细胞(A549DDP)和人源化的肺癌多药耐药模型(PDX模型)的肿瘤杀伤效果有显著提高。通过进一步研究,证明温热可以增强耐铂药肿瘤细胞对F-Pt-NPs的内吞作用,加速细胞谷胱甘肽的消耗,并促进Pt-DNA加合物的形成。
综上所述,通过将光热聚合物DAP-F形成的F-NPs与四价铂小分子形成的Pt-NPs混合所构建的纳米体系F-Pt-NPs,既具有光热效应,又具有铂药的杀伤性。在NIR诱导下产生的温热可以从多个过程系统性地抑制肿瘤铂类级联耐药,表现出显著的协同抑制作用。因此,利用近红外光触发的温热辅助解决级联耐药可作为一种普适性的联合治疗策略,对临床转化具有潜在意义。
相关论文发表在Advanced Materials 上,中国科学院化学研究所博士研究生王玲娜为文章的第一作者,肖海华研究员、张德清研究员为共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Systematic Strategy of Combinational Blow for Overcoming Cascade Drug Resistance via NIR‐Light‐Triggered Hyperthermia
Lingna Wang, Yingjie Yu, Dengshuai Wei, Lingpu Zhang, Xiaoyan Zhang, Guanxin Zhang, Dan Ding, Haihua Xiao, Deqing Zhang
Adv. Mater., 2021, DOI: 10.1002/adma.202100599
导师介绍
张德清
https://www.x-mol.com/university/faculty/148544
肖海华
https://www.x-mol.com/university/faculty/178031
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号