荧光探针细微结构变化导致细胞内不同荧光行为:以香豆素-喹唑啉酮共轭化合物为例揭示与G4相互作用对荧光探针设计的重要意义
荧光有机材料因其独特的性能而备受关注。大多数荧光材料在有机和细胞环境中的不同光学行为阻碍了它们的应用,尤其是在生物成像中的应用。例如,许多染料在水溶液中聚集,导致聚集诱导荧光淬灭(Aggregation Caused Quenching, ACQ);但是在有机溶剂或者表面活性剂的作用下发生解聚诱导荧光发射(Disaggregation Induced Emission, DIE)。过去几年的研究发现,一些生物小分子,例如蛋白质和DNA也可以在水相中诱导染料解聚以开启荧光。
G-四链体DNA(G4)是由富含碱基G的核酸序列折叠而成的特殊核酸二级结构。G4因其在细胞中的特殊调控作用而备受关注。除了细胞核,在线粒体基因组中也存在G4结构。尽管在过去十几年中,科学家设计了多种荧光探针用于G4结构检测,但其中大多数探针靶向细胞核,能够特异性靶向线粒体G4的探针相对较少,尤其是具有双光子荧光和超分辨率成像功能的线粒体G4探针尚不成熟。
近日,湖南大学黄静教授课题组与江西师范大学宋智彬副教授合作,报道了两种香豆素-喹唑啉酮共轭化合物CQ和MeCQ,两者在结构上仅有一个甲基取代基的区别。高度的结构相似性使其具有类似的物理和光学性质,但CQ和MeCQ在活细胞中的荧光性能却截然不同。CQ和MeCQ在水相中都有聚集诱导荧光淬灭效应(ACQ)。CQ因其分子内氢键形成大共轭平面,能与G-四链体DNA特异性结合,完成从聚集到解聚的转换而恢复荧光。MeCQ则由于与G-四链体的相互作用较弱而保持聚集形式没有明显的荧光增强现象。CQ具有线粒体定位功能,在活细胞中CQ与G-四链体结合,因此可以作为靶向线粒体G-四链体探针。其光闪烁性能还可用于活细胞中线粒体网络结构的超分辨率成像(图1)。
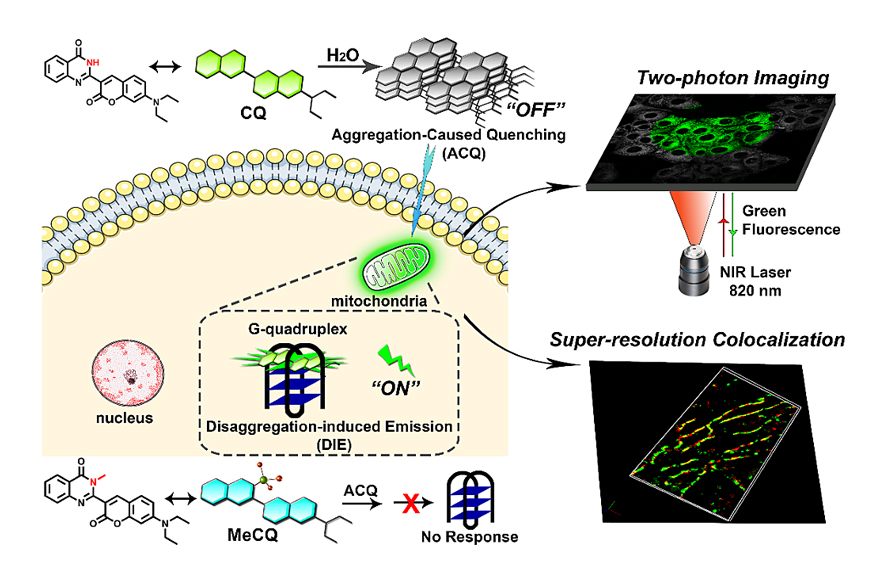
图1. CQ和MeCQ在活细胞中的不同光学行为示意图
研究人员使用荧光滴定法研究了CQ/MeCQ与不同DNA序列的相互作用。如图2所示,平行和混合G4s显著增强了CQ的荧光。相比之下,MeCQ则不具有这样的性质。这一结果证明了G4结构诱导CQ分子解聚而使其荧光增强,而MeCQ与G4结构的相互作用较弱。
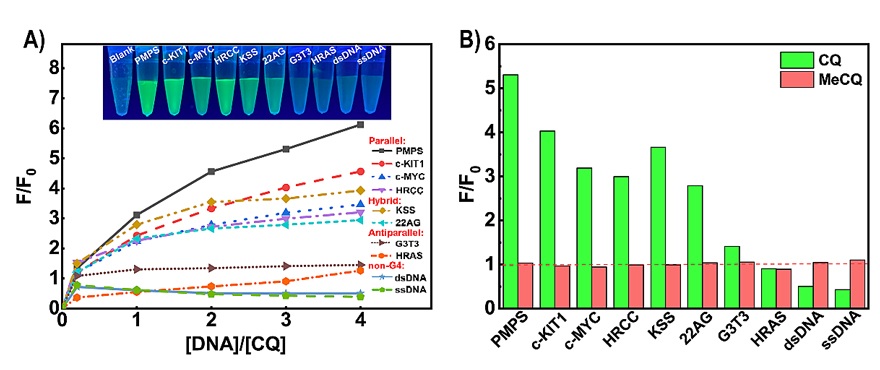
图2. CQ和MeCQ在不同DNA序列中的荧光强度变化
CQ具有双光子荧光性质,且表现出良好的光闪烁特征,可在活细胞线粒体聚集。研究人员利用随机光学重建显微技术 (STORM) 对CQ进行超分辨成像。相对于常规宽场成像,可以获得信噪比更高的线粒体网络图像。3D STORM图像显示:在活细胞中CQ和MitoTracker®Red CMXRos具有很高的共定位系数(图3所示)。重建的3D超分辨图显示了线粒体网络的深度可视化,证明CQ可以作为线粒体特异性染料用于超分辨率成像。
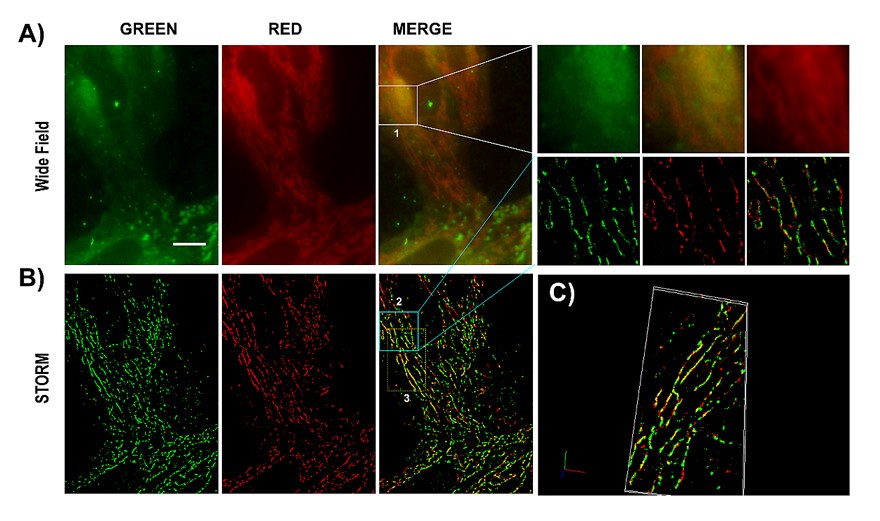
图3.活细胞中CQ和MitoTracker Red的荧光成像与STORM成像
这一成果近期发表在Analytical Chemistry 上,文章的第一作者是湖南大学化学化工学院博士研究生刘松和卜玲莉。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Subtle Structural Changes of Dyes Lead to Distinctly Different Fluorescent Behaviors in Cellular Context: The Role of G-Quadruplex DNA Interaction Using Coumarin-Quinazolinone Conjugates as a Case Study
Song Liu, Lingli Bu, Yuming Zhang, Jiangyu Yan, Ling Li, Guorui Li, Zhibin Song, Jing Huang
Anal. Chem., 2021, 93, 5267–5276, DOI:10.1021/acs.analchem.1c00301
黄静教授简介
黄静,博士生导师,湖南大学化学生物学与纳米医学研究所、湖南大学生物学院,化学生物传感与计量国家重点实验室教授。2010年毕业于武汉大学化学与分子科学学院,获化学生物学博士学位。2010年赴美国国立卫生研究院(NIH/NIA)从事博士后研究。2016年加入湖南大学,2017年入选“湖南省青年百人计划”。主要研究方向包括基于小分子的DNA识别以及损伤修复机理研究、靶向药物的设计筛选及其活性研究等。已在Molecular Cell, Angew. Chem. Int. Ed.,Cell Reports 等国际期刊上发表论文三十余篇。
https://www.x-mol.com/groups/huang_jing

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号