凝集体巨型囊泡作为一种新型人造细胞模型
人造细胞模型是能够实现多种仿生功能的腔室化微囊系统,具有分子腔室化、体外基因表达和初级代谢等特征,在生命起源、合成生物学以及生物医学领域等方面具有潜在的应用前景。传统的人造细胞模型,比如巨型单层囊泡(Giant unilamellar vesicles, GUVs)由于其磷脂双层膜的组成和微米级的尺寸形状,具有生长融合和类似细胞的机械/化学特性,广泛用作人造细胞模型。但是GUVs低的膜渗透性,低的封装效率以及结构不稳定性严重限制了其作为细胞模型的适用性。近日,湖南大学和英国布里斯托大学合作,通过将磷脂膜自组装在预先形成的凝聚体微滴的表面,构建了凝集体巨型囊泡(Giant coacervate vesicles, GCVs)结构,开发了一种具有选择性膜通透性和内部大分子拥挤的新型人造细胞模型。
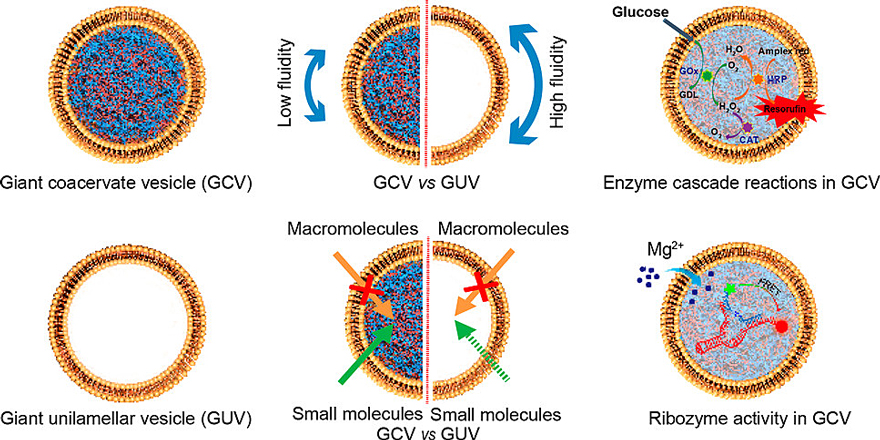
本工作将两性磷脂分子二棕榈酰基卵磷脂 (DPPC) 自组装在DNA/DEAE-dextran液相分离形成的凝集体表面,发展了一种含磷脂双层膜结构的内部大分子拥挤的人造细胞新型模型,凝集体巨型囊泡。该模型内部为具有液液相分离特性的凝集体,提供了大分子密集的腔室环境;该模型外膜为双层磷脂膜,提供了具有尺寸选择性的膜通透性结构,对于分子量低于4 kDa的物质具有膜渗透性。与传统的GUVs相比,GCVs将磷脂膜锚定到凝集体相表面,赋予了GCVs结构稳定性增大,膜流动性降低以及膜通透性增加等特性;同时液液相分离的凝集体为生化反应的进行提供了类似细胞的生物大分子密集腔室环境。葡萄糖介导的葡萄糖氧化酶-辣根过氧化物酶级联反应,以及镁离子介导的锤头状核酶裂解反应证实了膜的尺寸通透性,凝集体为生物酶反应和核酶反应提供了类细胞的生物分子密集的腔室环境。
将磷脂膜介导的腔室结构和液液相分离整合发展的GCVs,在人造细胞模型系统、原始细胞以及微反应器等方面具有潜在的应用优势,在原始生物组织的构建,人造亚细胞器的设计以及智能腔室微反应器等方面也具有广泛的应用前景。
这一成果近期发表在JACS上。湖南大学化学化工学院张艳文博士生为本文第一作者,刘剑波副教授和布里斯托大学Stephen Mann院士为论文通讯作者。本文得到国家自然科学基金等资助,主要依托湖南大学化学生物传感与计量学国家重点实验室、生物纳米与分子工程湖南省重点实验室等完成。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Giant Coacervate Vesicles As an Integrated Approach to Cytomimetic Modeling
Yanwen Zhang, Yufeng Chen, Xiaohai Yang, Xiaoxiao He, Mei Li, Songyang Liu, Kemin Wang, Jianbo Liu*, Stephen Mann*
J. Am. Chem. Soc., 2021, 143, 2866–2874, DOI: 10.1021/jacs.0c12494
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号