基于核酸适配体-CRISPR/CAS12a偶联体系的免疫分析法
CRISPR/Cas系统因其优异的基因编辑能力而广为人知。除此之外,由于CRISPR/Cas系统独特的靶点识别方式、极高的酶活力以及等温反应等特性,在核酸生物传感领域也表现出巨大的应用价值。然而,由于缺乏直接的信号转导策略,目前大多数基于CRISPR/Cas系统的传感策略只能分析核酸类靶标物,而对于非核酸靶标物质的检测则受限于少量的分析靶标、复杂的信号转导模式和较低的灵敏度,限制了其在临床诊断上的应用范围。
近日,合肥工业大学的李超副教授(点击查看介绍)和王峰教授(点击查看介绍)在Analytical Chemistry 杂志上发表内封面论文,开发了一种基于核酸适配体-CRISPR/Cas12a偶联体系的免疫分析方法(Aptamer-linked CRISPR/Cas12a immunoassay, ALCIA)。该方法充分利用了CRISPR/Cas12a体系和核酸适配体本身的特点,无需借助任何复杂的化学修饰或纯化手段,将CRISPR/Cas12a体系与核酸适配体相偶联,赋予CRISPR/Cas12a体系识别靶分子的能力。经测试,该方法普适性极强,能够直接应用于传统的酶联免疫吸附法(ELISA)平台,对多种生物物质,包括蛋白质、有机小分子、细菌、肿瘤细胞以及病毒颗粒等实现灵敏检测,极大地拓宽了CRISPR/Cas系统在生物传感中的应用范围。同时,由于偶联体的优良特性,使得检测方法更为灵活,适用于多种检测平台,进一步拓展了其普适性。
CRISPR/Cas12a在引导RNA(crRNA)与激活DNA序列(acDNA)的同时存在下,其反式酶活性(trans-cleavage)被激活,会疯狂地切割体系内存在的单链DNA分子(图2A)。通过分析三者的结构关系(图2B),它们呈现典型的“钳”式结构,其中Cas12a的酶活区域位于钳子的夹口处,而钳柄处主要是核酸结合区域。因而,研究者假设可以在acDNA的一端加入核酸适配体结构(远离酶活性区域),这样得到的偶联体系既不会影响Cas12a的酶活性,又能够给予Cas12a特异性识别非核酸分子的能力。
利用这一工具,研究者分别设计了ALCIA、Nano-ALCIA、Opti-ALCIA以及E-ALCIA(图3),并相继验证了它们在蛋白质、有机物小分子、肿瘤细胞、细菌以及病毒颗粒等分析物中的检测效果,显示出该方法在相关疾病诊断中具有广阔的应用前景。

图1. 当期封面。
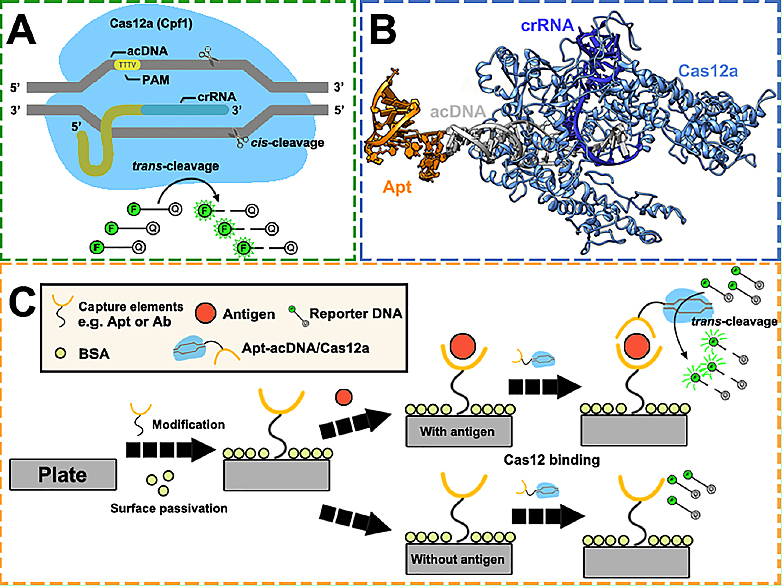
图2. (A)CRISPR/Cas12a体系及酶活性示意图。(B)核酸适配体-CRISPR/Cas12a偶联体的三维结构。(C)基于核酸适配体-CRISPR/Cas12a偶联体系的免疫分析法的工作示意图。
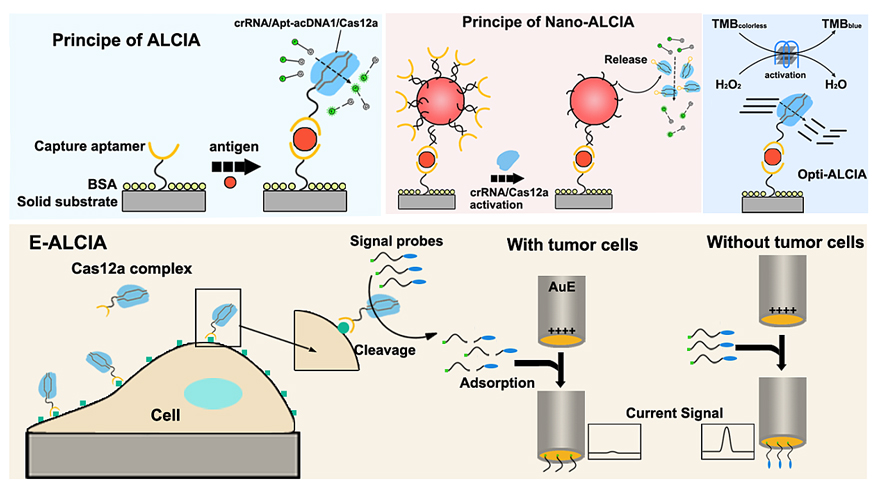
图3. 基于核酸适配体-CRISPR/Cas12a偶联体的多种免疫分析法。
这一成果近期发表在Analytical Chemistry 上,文章通讯作者为合肥工业大学李超副教授与王峰教授,第一作者是合肥工业大学硕士研究生李慧和南京大学博士研究生李梦璐。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Aptamer-Linked CRISPR/Cas12a-Based Immunoassay
Hui Li, Menglu Li, Yucai Yang, Fei Wang, Feng Wang*, and Chao Li*
Anal. Chem., 2021, 93, 3209–3216, DOI: 10.1021/acs.analchem.0c04687
导师介绍
李超
https://www.x-mol.com/university/faculty/115570
王峰
https://www.x-mol.com/university/faculty/115540
课题组介绍
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号