Science:又一力证,生命起源要归功于化学合成
生命到底是怎么来的?这是古往今来无数学者希望弄明白但又可能永远无法弄明白的问题。关于生命起源存在多种假说,比如宇宙生命论、自然发生论以及后来兴起的化学起源说等。这些假说中,目前学界接受程度最广的一种是化学起源说——在原始地球温度逐步下降以后的很长一段时间内,非生命物质通过极其复杂的化学过程,一步一步地演变而成原始生命,大致路线为:无机小分子→有机小分子→有机大分子→多分子体系→原始生命。1953年美国芝加哥大学研究生米勒在其导师的指导下实验发现,在原始地球还原性大气中闪电能促进有机物分子的产生,特别是氨基酸,这证明了化学过程在生命起源中的重要性。但问题依然存在,氨基酸这种有机小分子如何相互连接从而形成肽以及蛋白质这种有机大分子?在现在的生命体系里,大家都知道肽以及蛋白质的合成依靠的是高度进化的酶催化体系,但酶本身就是蛋白质,这其中似乎又缺失了关键的一环。
在自然界构成肽以及蛋白质的20种氨基酸中,带巯基的半胱氨酸算是比较特殊的一种,它具有很高的反应活性,可作为亲核试剂、金属配体,也是很多酶活性位点的重要组成单元。这让一些科学家猜测,半胱氨酸以及含半胱氨酸的肽在前生物化学(prebiotic chemistry)中是否能够催化肽连接(peptide ligation),从而找到那缺失的一环?不过,实验结果很让人泄气,科学家在模拟原始地球条件下进行了大量合成和分离半胱氨酸的尝试,却均未获得成功。比如,传统的Strecker反应可以合成α-氨基腈这类前生物氨基酸前体,但半胱氨腈(Cys-CN)这种半胱氨酸前体并不稳定,这说明Strecker反应在前生物条件下无法合成半胱氨酸类小分子。这让人们广泛认为半胱氨酸并非来源于化学合成,而是来源于后来的生物进化。
果真如此吗?近期,英国伦敦大学学院(UCL)的Matthew Powner教授(点击查看介绍)等人发现,胺的简单酰化即可防止半胱氨腈的降解,并能由乙酰化脱氢丙氨腈和硫化氢合成这种半胱氨酸前体。这应该是首次报道的稳定半胱氨酸衍生物的前生物合成。此外,在其它可组成蛋白质的α-氨基腈分子存在时,所合成的N-酰基半胱氨酸分子可以在中性水中催化肽连接反应。这些结果表明,半胱氨酸在生命起源时很可能作为丝氨腈(Ser-CN)合成的次要产物存在,并且很可能就是前生物合成过程中所需催化活性的基础。相关论文发表于Science 杂志。

Matthew Powner教授。图片来源:UCL
现在生物体内选择性和高效率合成半胱氨酸需要酶的作用。在植物和各种古细菌中,一般半胱氨酸的合成首先是通过酶催化丝氨酸的乙酰化或者磷酸化,接着在磷酸吡哆醛(PLP)作用下进行β消除反应,随后进行硫化氢的β加成反应(下图A)。在整个过程中,丝氨酸的α-氨基与PLP共价结合,以促进脱乙酰,并防止高度不稳定的脱氢丙氨酸(dehydroalanine,Dha)的分解。在前生物合成时期没有酶的存在,此时需要其他物质(如有机催化剂)的存在以促进该过程的进行,尤其是有机小分子,其中由Strecker反应合成的氨基腈在前生物合成氨基酸过程中的作用被大家所认可。另外,作者前期的工作发现α-氨基腈的N-酰化是在水中引发RNA和多肽合成的一个关键元素,它可以防止乙内酰脲、二酮哌嗪和咪唑引起的肽降解,N-酰化也可以稳定修饰腈基之后的Dha(Dha-CN),还可以避免烯胺与亚胺的转化以阻止硫化物与Dha的加成和半胱氨腈(Cys-CN)的分解。由此作者猜测通过丝氨酸的二酰化或许可以实现Dha的前生物合成,并且N,O-二乙酰化丝氨腈(Ac-SerAc-CN)是形成半胱氨酸的重要中间体(下图B)。除了α-腈的吸电子效应,N,O-二乙酰化也使Ac-SerAc-CN上的α-H酸性更强,活化丝氨酸上羟基作为离去基团。基于以上效应,作者猜测Ac-Dha-CN在中性条件下即可制备。
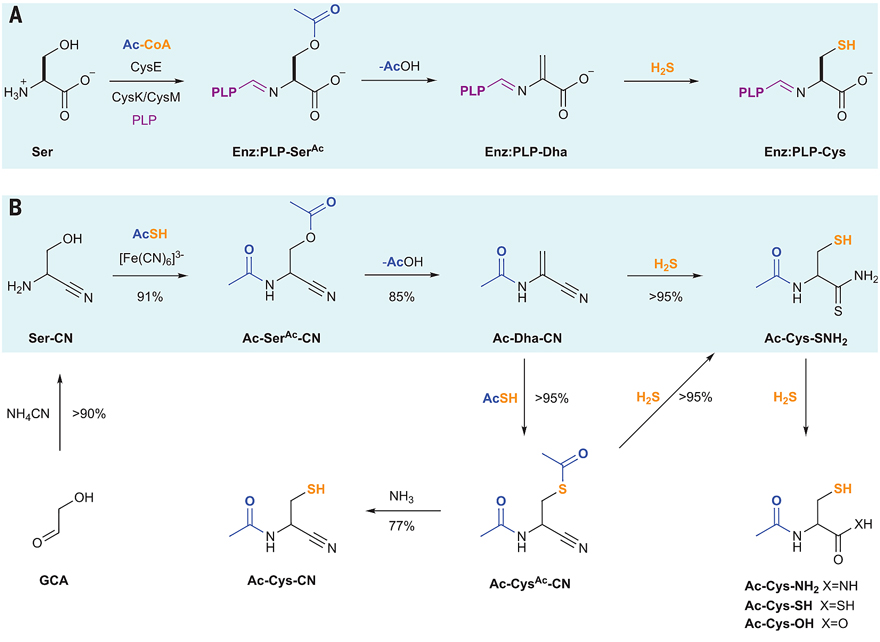
半胱氨酸的前生物合成。图片来源:Science
Ser-CN的二乙酰化,在铁氰化物和硫代乙酸(thioacetic acid,AcSH)存在时室温下反应1 h即可以实现,产率高达91%。在pH = 8的室温条件下Ac-SerAc-CN就可转化为稳定的Ac-Dha-CN,反应4天的转化率为85%(上图B)。通过对比腈基和酰基的作用可得α-腈有利于脱乙酸。Ac-Dha-CN的稳定性较高,即使在pH = 11时也很难与醋酸盐、磷酸盐以及氢氧化物反应,而可与硫化氢选择性反应生成半胱氨酸衍生物Ac-Cys-SNH2(上图B)。这应该是报道中首次实现的稳定半胱氨酸衍生物的前生物合成。Ac-Dha-CN也可以与水溶性更好的前生物环境中的乙酰化试剂AcSH反应生成硫酯Ac-CysAc-CN,随后快速与NH3反应生成Ac-Cys-CN,或者与H2S反应生成Ac-Cys-SNH2(上图B),这都为半胱氨酸的形成提供了条件。

中性水中硫醇催化的肽合成。图片来源:Science
既然证明了半胱氨酸类小分子可以实现前生物合成,那么这些小分子或者肽是否能作为有机催化剂来促进多肽合成呢?作者提出了他们的猜测(上图A ii),并以N-乙酰半胱氨酸(Ac-Cys-OH)为催化剂进行了证明。将Ac-Gly-CN、甘氨酸和Ac-Cys-OH一起在pH = 7的水中反应24 h实现了前两者的肽连接反应,得到Ac-GlyN-Gly-OH(下图C),该过程不需要活化剂的存在,反应条件更加简单。需要强调的是,这种反应的选择性也很不错,多种底物实验表明Ac-Cys-OH催化的肽连接反应会选择性构建α肽键(下图)。此外,这种有机催化的通用性也不错,多种氨基酸都可以发生肽连接反应(表1)。

半胱氨酸衍生物选择性催化构建α肽键。图片来源:Science
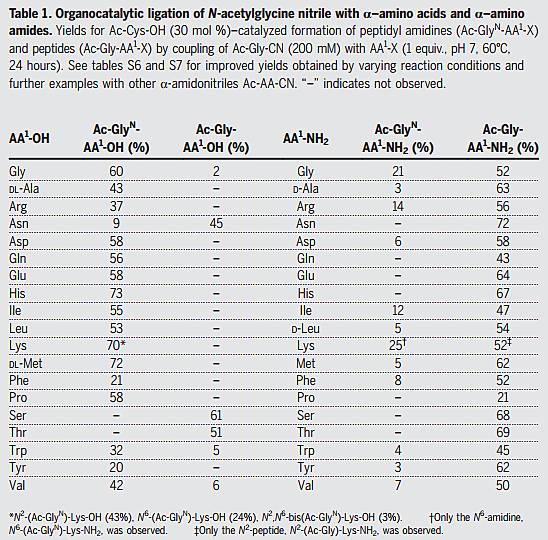
表1. 有机催化N-乙酰甘氨腈与不同α-氨基酸与α-氨基酰胺的反应。图片来源:Science
小结
Powner教授团队受半胱氨酸生物合成的启发,提出了半胱氨酸的前生物合成途径,以及半胱氨酸类分子在中性水中催化多肽合成的可能性,并以实验进行了证明。该工作为生命起源中肽与蛋白质的合成过程提供了一个新的有力证据。但是,该工作也带来了另外一些问题,比如,如果在生命起源形成初期多肽合成使用的是腈类化合物,那为什么随着进化会转向非腈类的物质呢?也许,就像本文一开始所说,生命起源可能是一个学者们希望弄明白但又可能永远无法弄明白的问题。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Prebiotic synthesis of cysteine peptides that catalyze peptide ligation in neutral water
Callum S. Foden, Saidul Islam, Christian Fernández-García, Leonardo Maugeri, Tom D. Sheppard, Matthew W. Powner
Science, 2020, 370, 865-869, DOI: 10.1126/science.abd5680
导师介绍
Matthew Powner
https://www.x-mol.com/university/faculty/4214
(本文由Sunshine供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号