CCS Chemistry | “葫芦”里装药:超分子多肽治疗药物输运新策略
摘要:国家纳米科学中心易宇副研究员、赵宇亮研究员与清华大学王华博士、张希教授合作,设计了葫芦[7]脲(CB[7])与PEG的共聚物作为超分子多肽的新型输运载体,再利用N-端苯丙氨酸与葫芦[7]脲的强主客体相互作用的原理,成功组装成为超分子多肽纳米药物。实验研究表明,该策略不仅提高多肽药物的稳定性并可以同时提高输送治疗效率。
多肽药物以其高活性、特异性以及毒副作用小等优点,在肿瘤和自身免疫性疾病治疗等方面具有重要的临床应用。然而在生理条件下,多肽药物稳定性差、易于被清除降低了其对肿瘤的治疗效果,肿瘤部位富集能力差同样制约了多肽药物的临床发展。为了解决这些问题,国家纳米科学中心易宇副研究员、赵宇亮研究员与清华大学王华博士、张希教授合作,提出了一种简便高效的超分子多肽治疗策略用于肿瘤治疗(图1)。该策略基于多肽N端的苯丙氨酸与CB[7]较强的主客体相互作用(结合常数~106 M-1),在溶液中将PEG与CB[7]的共聚物Poly-CB[7]同N端含苯丙氨酸的多肽简单混合,即可获得极高包封率(>97%)的超分子多肽纳米药物。
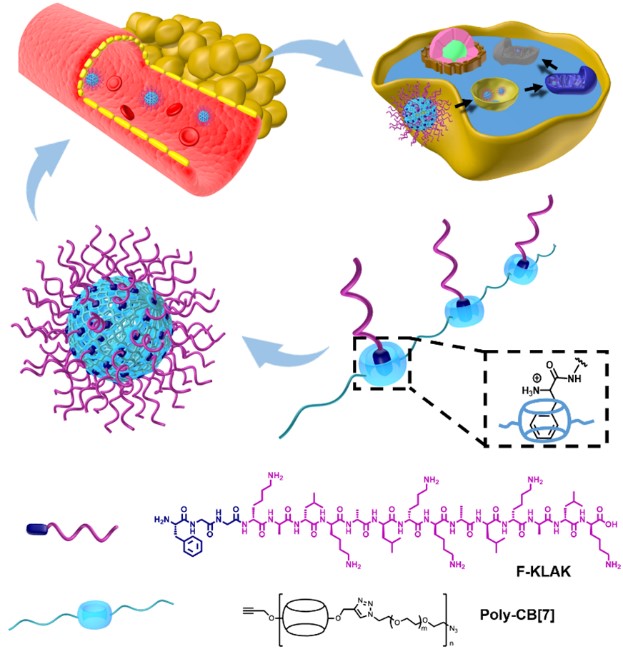
图1 超分子多肽治疗策略示意图
首先,通过多肽固相合成在抗肿瘤多肽(KLAK)的N端引入天然氨基酸苯丙氨酸单元,制备了多肽药物F-KLAK。值得注意的是,N端引入苯丙氨酸后,F-KLAK对HCT116肠癌细胞的细胞毒性明显增加,半抑制浓度值相比KLAK减小了10倍,并且该杀伤效果对肿瘤细胞具有选择性(图2A、2B)。研究表明,苯丙氨酸为KLAK提供了疏水基团,使其更易于与细胞膜结合,增加了多肽药物穿膜和破膜效率。随后,F-KLAK通过主客体相互作用高效地被Poly-CB[7]包载,组装形成超分子多肽纳米药物。超分子多肽纳米药物在细胞水平上维持了多肽药物的抗肿瘤活性及选择性(图2C)。体内实验表明,与单纯多肽药物相比,超分子多肽纳米药物在小鼠血液中循环时间延长,在肿瘤部位的富集量增加至2.8倍,并取得了良好的抑制肿瘤生长的效果(图2D、2E)。此外,超分子多肽纳米药物具有较低的血液毒性、肝毒性以及肾毒性,显示了优异的生物安全性(图2F)。
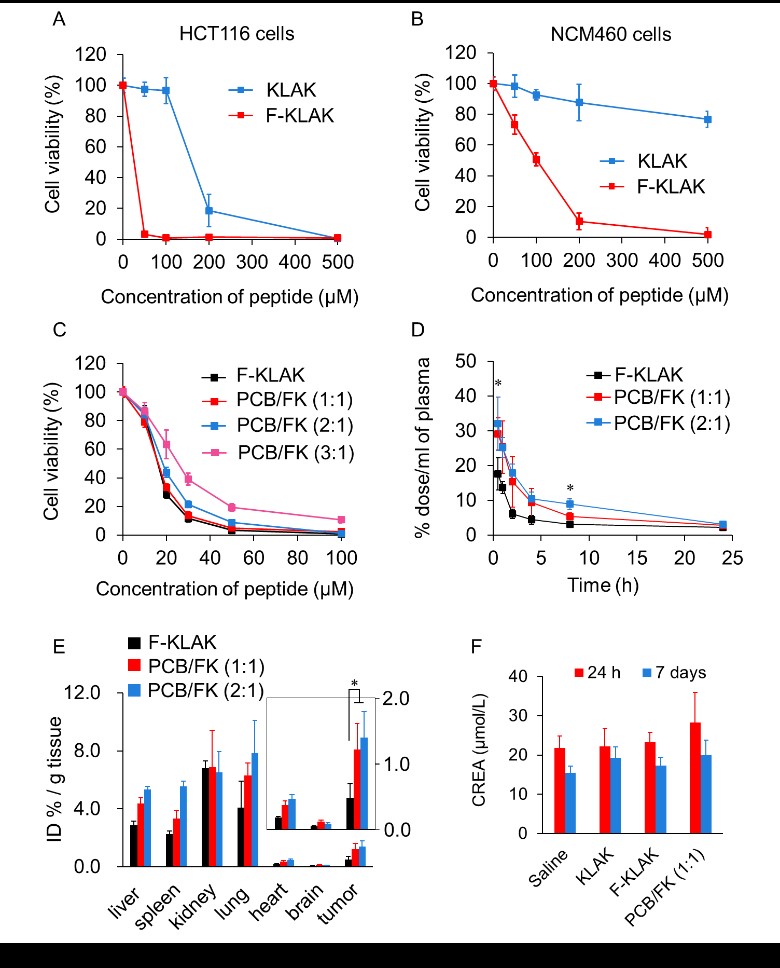
图2 多肽药物对HCT116结肠癌细胞(A)和NCM460肠表皮细胞(B)的细胞毒性;超分子多肽纳米药物对HCT116细胞的抗肿瘤活性(C),在血液中的代谢情况(D),在主要器官中的分布(E),以及肾毒性(F)。
可以预期,该超分子多肽治疗策略不仅适用于本文介绍的在N端引入苯丙氨酸的抗肿瘤多肽,也将可能适用于多种原本在N端就含有苯丙氨酸单元的临床多肽药物,例如人胰岛素、比伐卢定等,以提高它们的体内稳定性和治疗效果。由此可见,超分子多肽治疗策略有望为具有生物活性的多肽和蛋白类药物的药剂制备及其临床转化提供一个通用的、有潜力的方法。此项研究得到了科技部“纳米科技”重点专项以及国家自然科学基金的资助(参见王华等CCS Chemistry,2020,2,739-748)。该工作以Research Article的形式发表在CCS Chemistry,并在官网”Just Published”上线。
 扫描二维码,免费阅读下载原文。
扫描二维码,免费阅读下载原文。
文章详情:
Supramolecular Peptide Therapeutics: Host–Guest Interaction-Assisted Systemic Delivery of Anticancer Peptides
Hua Wang , Ya-Qiong Yan , Yu Yi *, Zi-Yu Wei , Hao Chen , Jiang-Fei Xu , Hao Wang , Yuliang Zhao * & Xi Zhang *
Citation:CCS Chem. 2020, 2, 739–748
文章链接:https://www.chinesechemsoc.org/doi/10.31635/ccschem.020.202000283
关注CCS Chemistry 微信公众号,了解更多文章信息:

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号