Nano Today:新型催化放疗策略用于肿瘤高效治疗
放疗作为临床肿瘤治疗的常规手段,其核心机制是利用高能X射线辐射分解水分子产生强氧化性的羟自由基(•OH),进而损伤肿瘤细胞DNA,最终导致肿瘤细胞死亡。其中,水分子的辐射电离包括两个关键过程:首先,在高能X射线作用下,水分子转变为介稳态的活化水(包括电离态水H2O+和激发态水H2O*);随后,活化水分解转变为•OH,但该过程的转化效率极低,是制约临床放疗疗效的关键因素之一。以往的放疗增敏研究主要是通过向肿瘤区引入含有高原子序数元素的材料,以此增加X射线在瘤区内的能量沉积,称为“元素增敏”放疗策略,然而这类研究策略并不能有效提升活化水到•OH的转化率。近日,复旦大学附属华东医院放射肿瘤科郑向鹏教授与步文博教授的合作团队,在无机功能材料用于放疗增敏长期合作的工作基础上(J. Am. Chem. Soc., 2013, 135, 35, 13041–13048; Nano Lett., 2018, 18, 5768−5774),聚焦于提升活化水到•OH转化率的关键科学问题,重新从化学角度思考,提出了一类新型的肿瘤放疗策略:催化放疗(Catalytic Radiotherapy,CRT)。
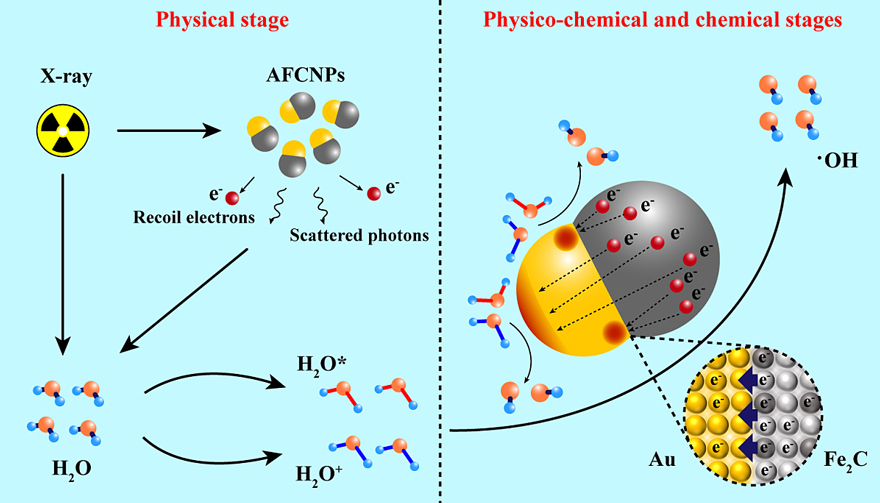
在催化放疗中,催化剂的设计是提升放疗疗效的关键。通过两种异质材料的结构合理设计,可以改变材料表面和界面局域电荷密度,赋予材料产生高催化活性位点的功能。Au是一类常用的放疗增敏材料,为了得到高局域电荷密度的Au表面,从而使其适用于提升活化水到•OH的转化率,该研究选取了Janus结构的Au-Fe2C纳米异质结作为催化剂。首先通过理论模拟计算,表明由于Au和Fe2C功函数和费米能级的差异,导致电子在异质结界面和Au表面的局域富集,这将有可能催化提升活化水分解到•OH反应的转化率,是一种潜在的催化放疗催化剂。基于此,研究人员采用改进的高温热解工艺,合成了单分散的Janus结构的Au-Fe2C纳米异质结。实验结果表明,在放疗X射线照射下,与单一Au相比,在Au-Fe2C异质结的高效催化作用下,•OH的产率提升了5倍之多,进而对肿瘤细胞DNA形成更严重的损伤。值得一提的是,Au-Fe2C还具有影响肿瘤细胞周期的能力,显著提高了对放疗敏感的G2/M期肿瘤细胞的比率。利用单击多靶模型计算放疗增敏比,Au-Fe2C异质结比Au提升了约1.5倍。最后,在荷瘤小鼠动物实验中,Au-Fe2C异质结也表现出了显著的放疗增敏效果。
不同于以往基于高原子序数材料的“元素增敏”策略,该研究提出的催化放疗策略是一个全新的放疗概念,其核心聚焦于X射线辐射水分解的化学过程,借助于合理设计的催化剂,解决活化水到•OH转化率低的瓶颈问题。这类新型的催化放疗策略,不但拓展了纳米催化剂的生物医学应用范围,更重要的是,也为纳米材料用于放疗研究的发展提供了新的思路,值得进一步探索。
相关研究成果已发表于高水平学术期刊Nano Today(影响因子16.907)。论文第一作者为复旦大学博士生吕斌,共同第一作者为华东师范大学博士生张会林;论文通讯作者为复旦大学附属华东医院放射肿瘤科郑向鹏教授和复旦大学材料科学系步文博教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Structure-oriented catalytic radiosensitization for cancer radiotherapy
Bin Lv, Huilin Zhang, Xiangpeng Zheng,* Han Wang, Weiqiang Ge, Yanping Ren, Zi Tan, Meng Zhang, Zhongmin Tang, Yanyan Liu, Libo Zhang, Yelin Wu, Xingwu Jiang, Wenbo Bu*
Nano Today, 2020, 35, 100988, DOI: 10.1016/j.nantod.2020.100988
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号