外泌体靶向药物递送体系——骨关节炎的无细胞疗法
骨关节炎(OA)是老年人关节疼痛和致残的主要原因,是四大致残原因之一。流行病学调查表明,中国60岁以上人群骨关节炎患病率高达50%。随着人口老龄化的增加,骨关节炎发病率逐年升高,严重威胁国人的身体健康和降低其生活质量。骨关节炎是一种由多种因素导致的关节疾病,发病机制复杂。目前,骨关节炎治疗的重点在于缓解症状而不是预防或治疗,临床上开发用于治疗骨关节炎的药物虽然具有一定的疗效,但至今没有一种药物能够阻断骨关节炎的进程。软骨代谢失衡是骨关节炎发生的病理基础。深圳市第二人民医院骨科基础研究团队于2016年就报道了miRNA-140参与关节软骨基质的代谢调控,是治疗骨关节炎明星因子(Arthritis Research & Therapy, 2016, 18, 105)。
靶向递送至特定的病灶细胞或组织是核酸药物临床成功应用的关键,特别将microRNA-140(miR-140)穿过致密无血管的软骨基质递送到软骨细胞中仍然是一个重大挑战。近日香港中文大学夏江教授团队和深圳市第二人民医院骨科基础研究团队设计构建靶向软骨细胞的体系,特异性递送miR-140到软骨细胞,抑制软骨基质降解,用于骨关节炎的治疗。利用携带软骨细胞的亲合肽(CAP)融合表达展示于外泌体膜蛋白(lamp2b)上表面作为靶向的基因工程化外泌体可实现靶向软骨细胞(图1)。与无靶向的天然外泌体相比,关节内注射的CAP外泌体在能长时间保留在关节腔中,减少体内扩散。CAP外泌体还通过致密的软骨基质将miR-140传递至深层软骨区域,抑制软骨降解蛋白酶,并抑制大鼠模型中的骨关节炎恶化,从而为骨关节炎的治疗提供了一种潜在的基于细胞器的无细胞疗法。

图1. 研究方案,CAP靶向性外泌体递送体系将miR-140靶向递送至软骨细胞进行OA治疗。
研究表明CAP改造的外泌体能更特异的递送Cy3荧光标记miRNA进入软骨细胞并抑制MMP-13基因及蛋白水平的表达,动物活体成像也展现CAP外泌体携带miR-140较长时间保留在关节腔里,并特异性靶向进入软骨层的软骨细胞(图2)。且CAP外泌体携带miR-140可明显抑制MMP-13和adamts5,说明表达CAP-lamp2b蛋白的外泌体能高效果携载miR-140,能更有效地抑制MMP-13 ,起到对抗骨关节炎的作用。

图2. CAP靶向性外泌体关节腔注射后靶向递送miRNA至软骨层细胞,并抑制软骨基质的降解。
组织切片及免疫组化结果表明基因工程改造靶向性外泌体递送miRNA-140能治疗骨性关节炎(图3)。该结果揭示CAP-exosome 能用于软骨靶向性核酸药物治疗,为临床的应用提供可能。
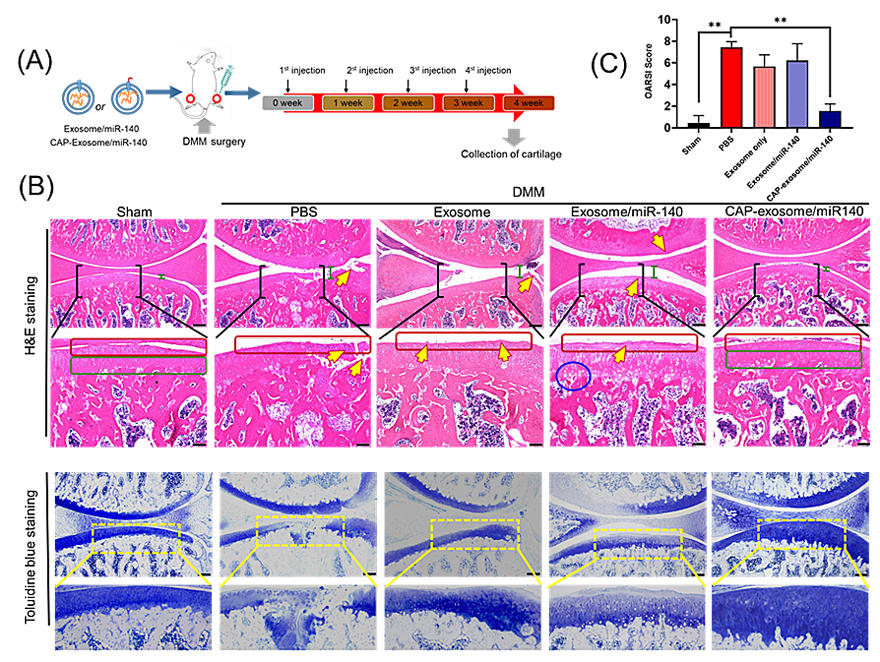
图3. OA动物模型表明CAP外泌体携带miR-140抑制骨关节炎。
近年来,骨关节炎的发病率逐渐增加。传统的手术关节置换及干细胞治疗价格高昂,应用外泌体作为药物载体的靶向治疗在提高抗骨关节炎效能的同时,也降低了患者治疗成本。外泌体来源广、免疫原性低,在靶向骨关节炎的治疗性药物递送领域将具有广阔的应用前景。相信随着更为深入的研究,有望为包括骨关节炎治疗,开辟一条高效可行的新途径。
这一成果近期发表在ACS Appl. Mater. Interfaces。共同第一作者为梁宇杰博士和徐晓博士,共同通讯作者为段莉研究员、王大平教授、夏江教授,这项工作得到了国家自然科学基金和深圳市科创委相关基金的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Chondrocyte-Targeted MicroRNA Delivery by Engineered Exosomes toward a Cell-Free Osteoarthritis Therapy
Yujie Liang, Xiao Xu, Xingfu Li, Jianyi Xiong, Biquan Li, Li Duan*, Daping Wang*, Jiang Xia*
ACS Appl. Mater. Interfaces, 2020, 12, 36938–36947, DOI: 10.1021/acsami.0c10458
香港中文大学夏江教授团队:
https://chem.cuhk.edu.hk/people/academic-staff/xj/
https://www.iterm.cuhk.edu.hk/our-people/prof-xia-jiang/
深圳市第二人民医院骨科基础研究团队:
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号