ACS编辑良择 | 大面积高度排列的富勒烯纳米晶体支架增强间充质干细胞的自我更新和多能性

每天,ACS遍布全球的期刊编辑们从ACS的众多期刊中选出一篇新近发表的文章,永久免费开放给所有读者。这些被特别选出的文章所探讨的最新研究成果将因其免费开放而使更广大的科研受众获益。
英文原题:Large-Area Aligned Fullerene Nanocrystal Scaffolds as Culture Substrates for Enhancing Mesenchymal Stem Cell Self-Renewal and Multipotency

通讯作者:贾晓芳,日本国立材料研究所 (National Institute for Materials Science);Katsuhiko Ariga,日本国立材料研究所 (National Institute for Materials Science);东京大学新领域创成科学研究科 (Graduate School of Frontier Sciences, The University of Tokyo)
作者:Jingwen Song (宋静文), Xiaofang Jia (贾晓芳),Kosuke Minami, Jonathan P. Hill, Jun Nakanishi, Lok Kumar Shrestha, Katsuhiko Ariga
人的间充质干细胞(hMSCs)是成年的多能干细胞,能够分化为不同的细胞谱系,包括组成骨骼,脂肪,神经和软骨细胞。由于易于获取和有效的免疫抑制特性,hMSCs正逐渐用于基于细胞的组织再生疗法。但是hMSCs从人源分离的细胞数量十分有限,远远低于在临床实践中需求,并且在体外扩增过程中,hMSC会迅速失去了其多能性和再生能力,分化失控(图1)。因此,在增强基于hMSC的治疗效率,包括在神经性疾病、骨骼组织损伤和器官衰竭等疾病的过程中,找到保持hMSCs干性,同时对其进行体外扩增的新策略是非常重要的。
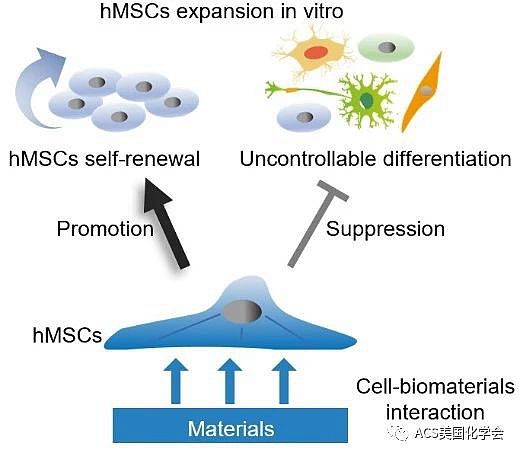
图1. 生物材料的生物物理性质通过细胞-材料相互作用诱导hMSC自我更新,抑制无法控制的分化
除了可溶性生化诱导剂外,基底的生物物理性质显示出可控制短期和长期的细胞行为,包括粘附、迁移和分化。其中精确连续地调整细胞微环境的纳米尺度形貌参数可以用于优化控制干细胞自我更新。然而,目前提供可微调的纳米尺度形貌特征的策略不能用于大面积的制备,而且制备过程复杂,因此限制了临床实践的应用。在本文中,一方面,Langmuir-Blodgett(LB)方法只需调整两个组装单元的形态、尺寸和比例即可实现纳米尺度形貌特征连续可调性的变化。为制造大面积用户定义的纳米结构提供了策略。另一方面,富勒烯可以通过液体-液体界面沉淀的方法得到一维、二维和三维的从纳米到微观的结构,为我们提供了创建适合于形成不同纳米图案的各种组装单元。我们混合不同含量的长径比不同的富勒烯纳米晶体(FNWs),使用LB方法来制备具有连续可调大面积排列的纳米结构表面,作为hMSCs的体外扩增的细胞培养基底(图2)。我们已经发现,高度排列的FNWs纳米结构表面能够促进由适当的细胞收缩力和Yes相关蛋白(YAP)的核定位介导的hMSCs的增殖和长期多能性保持。
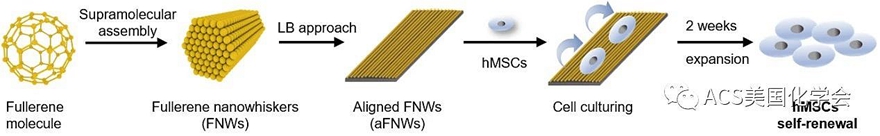
图2. 通过使用LB方法获得大面积FNWs纳米结构的支架用于在体外保持hMSCs的自我更新
通过使用FNWs作为细胞培养支架,我们成功实现了hMSCs体外扩展并保留其多能性。我们阐明了干细胞多能性保留在FNWs纳米结构支架的表面上与细胞中的粘着斑的形成和YAP转录共激活子易位的关系。首先,在诸如玻璃的平坦基底上,hMSCs表现出较大的粘着面积和高的细胞骨架张力。这会将干细胞从缓慢的生长状态转变为高活性状态,从而导致hMSCs的分化不受控制并失去干性。所以在hMSCs扩增过程中要保持多能性,需要引入小的细胞骨架张力。排列整齐的FNWs支架的疏水纳米形貌表面提供有限的细胞-材料接触面积,从而导致hMSCs的细胞伸展和黏着区域降低,细胞的骨架张力也随之降低。因此,与玻璃基底相比,hMSCs的干性在FNWs纳米支架上得以保留。
其次,排列整齐的FNWs的纳米支架与富勒烯对蛋白质吸附特性共同形成的细胞外基质的蛋白质纹路可以用于调节细胞行为(图3)。高度排列的FNWs支架促进平行于FNWs的长轴的细胞粘着斑的延长,并防止垂直于FNWs的长轴的细胞粘着斑的生长。因此,细胞沿FNWs的长轴定向伸展。相比之下,排列程度低的FNWs支架可用于ECM蛋白质吸附的表面积较小,虽然没有限制细胞粘着斑的方向,但阻止了其成熟。相应地,在排列程度低的FNWs基底上,hMSCs的伸展面积更小并且没有聚合的F-肌动蛋白。因此,与排列程度低和中的FNWs支架相比,高度排列的FNWs支架提供了更加一致的生物物理性质,并且均匀地激活了hMSCs的机械转导过程。高度排列的FNWs支架控制hMSCs的均匀伸长和方向,从而影响细胞核中组蛋白的乙酰化和甲基化,启动hMSC自我更新模式。
另外,Yes相关蛋白(YAP)的核定位被认为是对干细胞中大量的多能性基因表达进行正向调控的启动子。同时YAP在机械转导中的作用是作为一种由基底的生物物理性质控制的传感器和介质。细胞中成熟的粘着斑粘附和F-肌动蛋白聚合帮助YAP从细胞质募集到细胞核,然后促进多能性基因的表达。因此,高度排列的FNWs基底促进YAP的的核转移从而促进了hMSCs干性调节因子OCT4,NANOG和SOX2的表达。综上所述,高度排列的FNWs作为细胞培养支架提供了一种中间条件,可以有效减少但不消除粘着斑,通过适当的细胞收缩力和YAP的核定位介导hMSCs长期的多能保持扩增。

图3. FNWs纳米的支架通过机械转导控制hMSC自我更新过程。从细胞与ECM相互作用到激活细胞核干性调节因子的机械转导过程模型。
本研究的相关结果已发表于ACS Applied Nano Materials,并入选ACS Editors'Choice。本项目得到了日本学术振兴会 (Japan Society for the Promotion of Science (JSPS) KAKENHI Grant No. JP16H06518)和日本科学技术振兴机构(the Core Research for Evolutional Science and Technology (CREST) program of Japan Science and Technology Agency (JST) Grant No. JPMJCR1665)的支持。
扫描二维码阅读英文原文,或点此查看原文:

ACS Appl. Nano Mater. 2020, 3, 7, 6497–6506
Publication Date: July 4, 2020
https://doi.org/10.1021/acsanm.0c00973
Copyright © 2020 American Chemical Society
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号