动态界面揭示细胞粘附新途径
生物体内细胞微环境是一个高度动态的复杂体系,细胞与细胞外基质(ECM)和相邻细胞之间,无时无刻不在发生着动态相互作用。这些相互作用被细胞膜表面受体蛋白感应,激活其特异性信号通路,同时给予细胞力学刺激,是影响细胞生物功能的重要因素。然而,由于其体系的复杂性,动态相互作用调控细胞行为与功能的机制尚不明确。
四川大学魏强研究员(点击查看介绍)及其合作者,首先利用材料化学手段,设计了细胞粘附配体能够在细胞粘附界面动态扩散的模型,从最小的分子基元模拟细胞微环境中配体的动态行为(图1)。该模型采用两亲性嵌段共聚物的自组装单分子层,疏水锚点基团为二苯基甲酮,亲水链段为聚甘油(polyglycerol),具有抵抗ECM蛋白非特异性吸附能力,并在顶端修饰细胞粘附配体RGD多肽。调控基底材料疏水性,便可通过疏水相互作用控制嵌段共聚物分子以及粘附配体在基底表面的流动性,制得配体高流动性与低流动性界面。利用紫外光诱发二苯基甲酮夺氢反应,可将嵌段共聚物共价接枝在基底表面,从而完全限制配体的流动性,制得静态界面。同时,细胞接触界面的粘附配体密度、形貌与亲水性可保持一致。
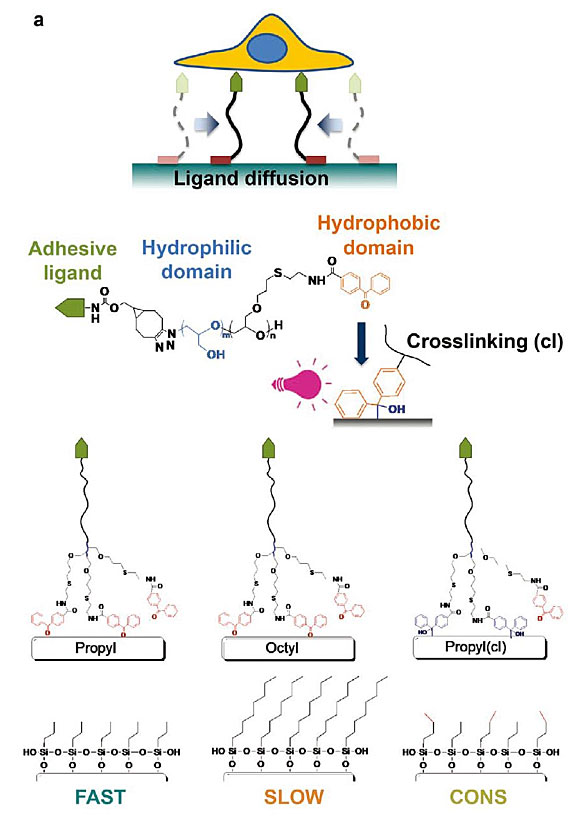
图1. 粘附配体动态扩散模型
基于该模型体系,研究人员发现,细胞在配体低流动性界面铺展速率慢,而在高流动性界面与静态界面铺展速率快。然而,相比于静态界面,高流动性界面并不能诱导间充质干细胞成骨分化。有趣的是,以往经验表明,有利于细胞铺展的界面,能够给与细胞更强的力学刺激,从而诱导干细胞成骨分化。而动态界面的研究发现与以往经验不符。细胞在高流动性界面的粘附可能基于非典型方式。
II型肌球蛋白抑制实验与核纤层蛋白A/C的免疫荧光染色显示,细胞在高流动性界面的铺展并不完全依赖于通常促进细胞铺展的肌动球蛋白收缩作用力。通过配体荧光标记与整合素抑制实验(图2),发现细胞能够通过整合素α5β1特异性地“拢聚”高流动性配体,从而促进细胞铺展。而在低流动界面,配体活动受限,“拢聚”行为很弱。在静态界面,“拢聚”行为被抑制,共价接枝却赋予细胞较强的粘附作用力,同时激活整合素α5β1与整合素αvβ3。
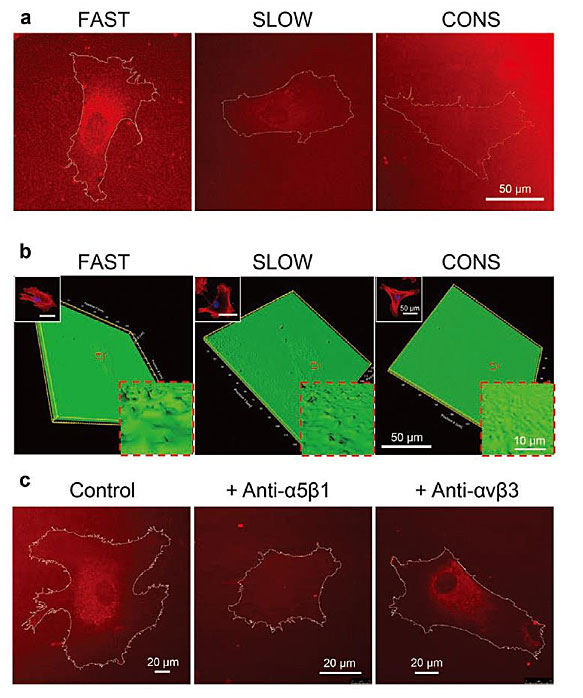
图2. 细胞通过整合素α5β1特异性地“拢聚”高流动性配体
转录组测序技术系统性考察了与细胞粘附铺展关系紧密的Rho GTPase相关信号通路。结果显示,高流动性界面有助于激活RhoA,但ROCK活性却被大幅抑制,以至II型肌球蛋白表达被抑制,令细胞缺乏内部作用力。与此同时,高流动性界面通过PI3K通路激活Rac信号。RhoA与Rac共同促进了肌动蛋白聚合,让细胞呈现出片状伪足式铺展(图3a)。静态界面则激活典型的RhoA/ROCK/myosin II力学信号转导通路,产生肌动球蛋白收缩作用力,刺激细胞铺展(图3b)。
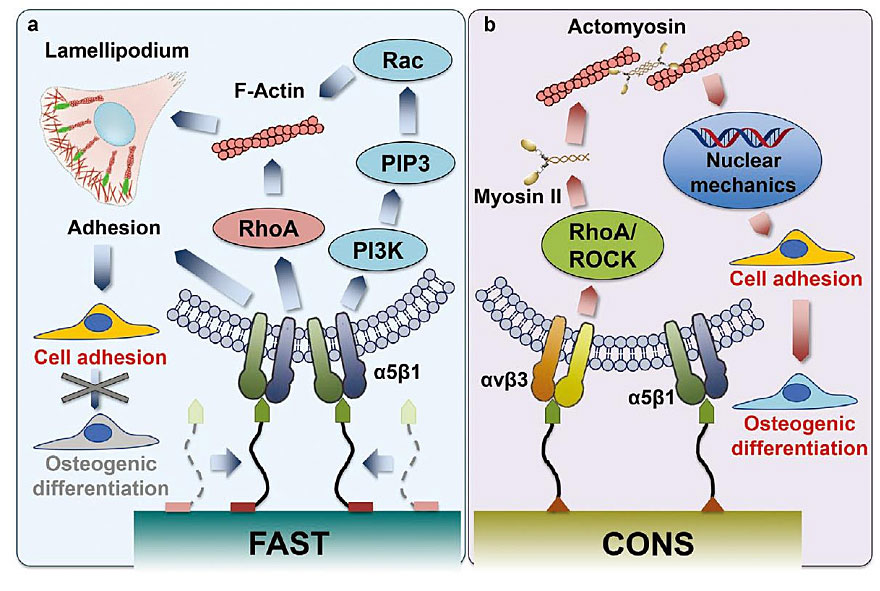
图3. 粘附配体流动性通过整合素α5β1激活Rac与RhoA信号通路促进不基于细胞内作用力的细胞铺展。
该工作构建了研究细胞与微环境动态相互作用的简化模型,发现了异于典型的肌动球蛋白驱动的细胞粘附机制,深入研究了不同类型的整合素与Rho GTPase在细胞响应微环境动态刺激过程中的角色,对从分子水平上理解细胞行为具有深远的指导意义。此工作是该团队继生物界面粘附位点分布与界面拓扑结构对细胞行为影响研究之后(ACS Nano, 2017, 11, 8282; Adv. Healthcare Mater., 2019, 8, 1801384; Small, 2020, 16, 1905422; Nano Lett., 2019, 20, 748),在细胞与材料界面相互作用领域的又一重要成果,对理解生物界面细胞行为机制,以及设计可调控细胞功能的新型界面材料提供了值得借鉴的思路。
该工作发表于Advanced Materials。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Ligand diffusion enables force-independent cell adhesion via activating α5β1 integrin and initiating Rac and RhoA signaling
Leixiao Yu#, Yong Hou#, Wenyan Xie, Jose Luis Cuellar Camacho, Chong Cheng, Andrew Holle, Jennifer Young, Britta Trappmann, Weifeng Zhao, Matthias F. Melzig, Elisabetta A. Cavalcanti-Adam, Changsheng Zhao, Joachim P. Spatz, Qiang Wei*, Rainer Haag
Adv. Mater., 2020, DOI: 10.1002/adma.202002566
导师介绍
魏强
https://www.x-mol.com/groups/wei
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号