蛋白类药物复杂糖修饰鉴定与定量新技术
异质性分析是治疗性蛋白药物质量控制的关键,其中电荷异质性和糖基化异质性是两个主要的质量控制参数。拥有多个糖修饰位点的蛋白类药物,其等电点异质体分离和糖基化修饰的定量表征缺乏有效的解决方案。康柏西普是一种抗血管内皮生长因子的Fc-融合蛋白,用于治疗眼部湿性黄斑病变。该融合蛋白分子中含有14个N-糖基化修饰位点(单体中含有7个),糖基化修饰比例占整个分子质量数的 ~30 %,因此,在整体蛋白水平实现其电荷异构体高效分离和异构体糖基化修饰的表征十分困难,基于传统的FLR-UPLC、HPAEC-PAD等技术方法不能进行位点特异性N-糖基化修饰的量化分析。
近日,国家蛋白质科学中心(北京)应万涛课题组、北京工业大学董俊兴教授和成都康弘药业合作,建立了基于二维电泳(2-DE)高分辨分离并制备电荷异构体的方法,并且建立了“串联质谱特征碎片离子辅助的位点特异性糖肽定量策略”,从而实现对康柏西普14个电荷异构体高效分离,以及每个异构体7个位点上各自N-糖基化修饰的类型及丰度变化分析。这一技术应用于康柏西普的电荷异构体和糖修饰的批间一致性分析,实现了N-糖动态变化与电荷异构体的酸碱性相关性分析,发现关键位点唾液酸修饰占比与等电点分布显著相关。该方法为分离高度糖基化蛋白类药物的电荷异构体、分析位点特异性N-糖基化修饰动态变化及批间一致性提供了新的参考方案。
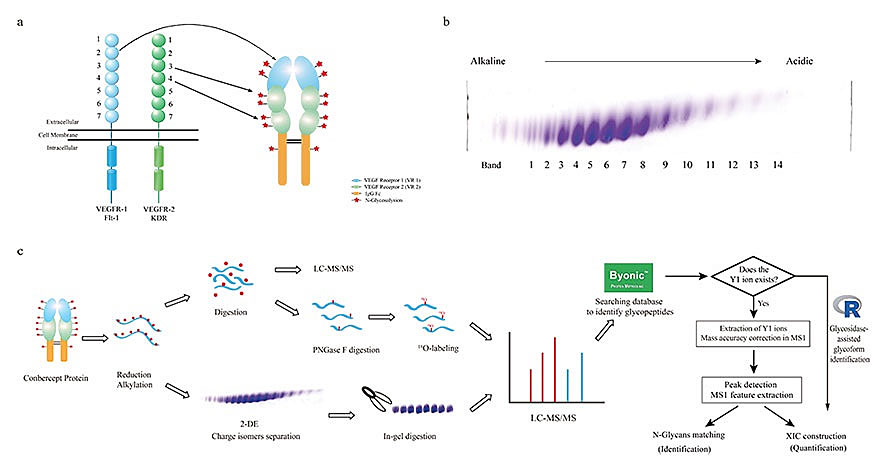
Figure 1. Schematic representation of the analysis workflow
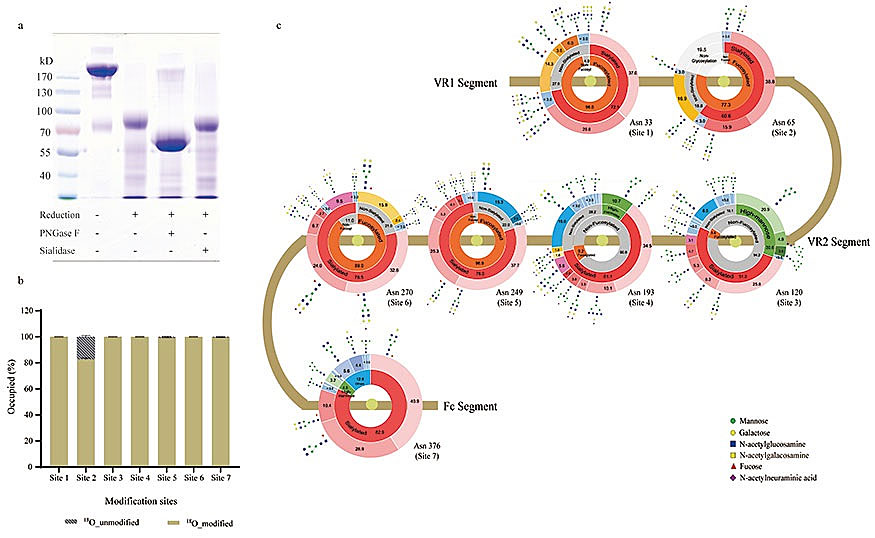
Figure 2. Glycan content and site-specific glycoforms
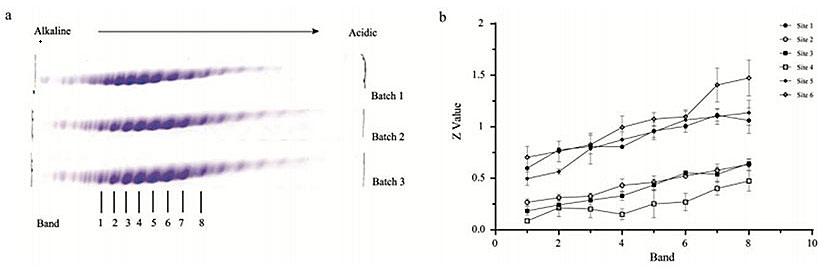
Figure 3. Relative content of sialic acid in different gel spots
这一成果近期发表在Analytical Chemistry 上,文章的第一作者是北京工业大学博士研究生李晓宇和成都康弘药业的贺庆博士。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Site-Specific and Quantitative N-Glycan Heterogeneity Analysis of the Charge Isomers of an Anti-VEGF Recombinant Fusion Protein by High-Resolution Two-Dimensional Gel Electrophoresis and Mass Spectrometry
Anal. Chem., 2020, 92, 5695-5700, DOI: 10.1021/acs.analchem.0c00592
应万涛博士简介

国家蛋白质科学中心-北京、北京蛋白质组研究中心研究员,生物质谱与糖蛋白质组学课题组PI,北京市科技新星。研究方向为蛋白质糖基化修饰分析的新技术与新方法、定量蛋白质组学与修饰研究的新技术与方法及精准肿瘤蛋白质组应用。在Nature,PNAS,Mol Cell Proteomics,Anal Chem等发表SCI论文60余篇。课题组随时欢迎博士后合作研究及硕博士考生。
Email:yingwantao@ncpsb.org.cn
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号