肿瘤微环境响应的自组装纳米反应器用于级联式催化联合化疗
肿瘤微环境(tumor microenvironment, TME)介导的纳米催化治疗主要是利用无毒或低毒的纳米材料,通过选择性地催化、触发TME内部的特定化学反应,在局部产生数量可观的特定反应产物如活性氧物种(reactive oxygen species, ROS)的肿瘤治疗策略,从而实现一系列的生物学和病理学响应,并降低对正常组织的副作用,是一种肿瘤特异性的治疗方式。但是,TME介导的纳米催化治疗效率一般会受肿瘤内H2O2水平和酸度不足的限制。因此,能否通过调节TME而增强肿瘤催化治疗效果成为当前研究的热点之一。
虽然已有为数不多的研究报道了纳米级联催化疗法并显示出通过自供给H2O2和H+而增强产生ROS的潜能,但是,这一过程中肿瘤乏氧的加重可能导致肿瘤的增殖和转移,也很难精准地将H2O2递送到肿瘤部位。特别需要注意的是,肿瘤细胞需要大量的营养物质才能快速增殖,这使得肿瘤细胞中的葡萄糖浓度高于正常细胞。鉴于此,葡萄糖氧化酶(GOx)作为一种天然的蛋白酶,被用来有效催化葡萄糖并在肿瘤区域生成H2O2和葡萄糖酸。然而,游离的GOx不但不稳定而且缺乏肿瘤的特异性,其在苛刻的TME中的催化活性和稳定性都大大降低,也会很快从肿瘤中渗出并到达正常组织,从而降低了级联催化治疗的疗效且容易造成对正常组织的损伤。
近日,中国科学院高能物理研究所纳米生物效应与安全性重点实验室的研究人员设计了一种TME中葡萄糖响应的级联纳米催化反应器(cascaded nanocatalytic reactor, NCR)用于级联式催化联合化疗,有效地解决了上述问题。该纳米反应器主要是利用MoS2纳米酶(MoS2@CGTC NCR,C代表壳聚糖,G代表GOx,T代表乏氧激活型抗肿瘤药物替拉扎明TPZ)设计而成。在酸性TME中,MoS2@CGTC反应器上的壳聚糖逐渐降解并使得GOx的催化特性显现,该级联纳米催化反应器克服了GOx单独使用时易从肿瘤内渗出到正常组织的局限性。GOx催化TME中高表达的葡萄糖并生成H2O2的同时产生更多的H+和消耗了更多的O2,从而加剧了瘤内的酸度和乏氧。从NCR上释放出来的TPZ被加剧的乏氧TME激活并产生更多的自由基,而NCR中的基体MoS2具有拟过氧化物酶的功能,可以催化GOx催化葡萄糖分解过程产生的H2O2为羟基自由基的同时还可将肿瘤内高表达的抗氧化剂GSH催化氧化为GSSG,打破了细胞内抗氧化剂的保护平衡,从而实现TME响应的“自增强”催化治疗/化疗的联合治疗。与同等剂量的游离TPZ抗肿瘤疗效相比,MoS2@CGTC NCR可以产生更多的自由基,从而使得抗肿瘤疗效更为显著并抑制了肿瘤转移。此外,MoS2@CGTC的载体MoS2参与级联式催化疗法联合化疗后,在TME中逐渐尺寸缩减并降解后以低毒的钼酸盐的形式排出体外,从而减少了治疗过程对正常组织的损伤。
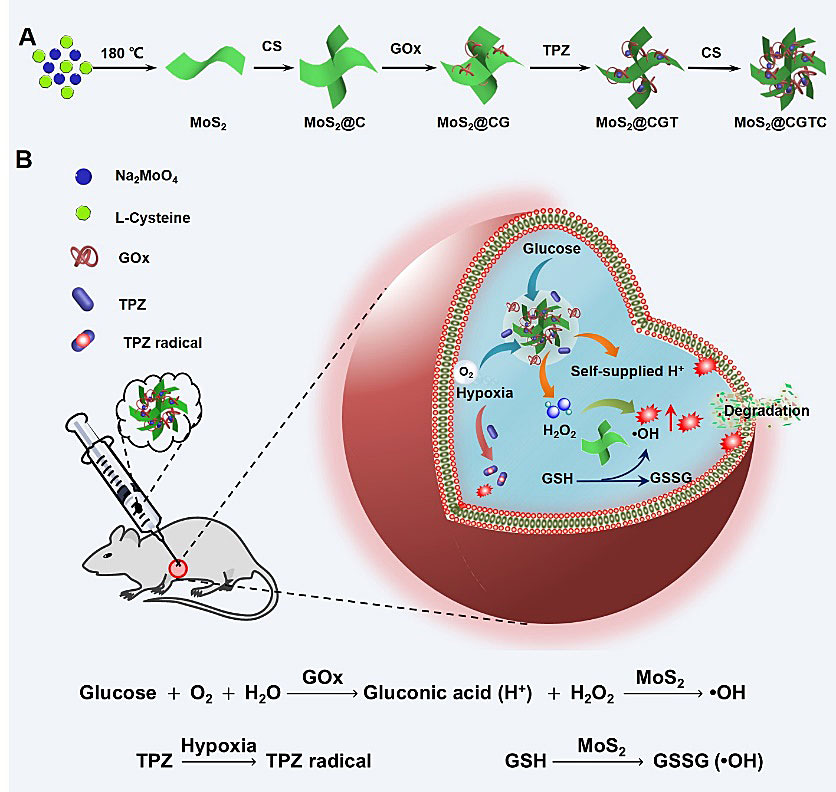
图1.(A)自组装MoS2@CGTC NCR的设计原理图;(B)MoS2@CGTC NCR实现葡萄糖响应的自调节TME增强级联式催化联合放疗的思路。
这一成果近期发表在Materials Horizons 上,文章的第一作者是中国科学院高能物理研究所的博士研究生梅林强。中科院高能物理研究所的谷战军研究员和尹文艳副研究员为该文章的共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Glucose-responsive cascaded nanocatalytic reactor with self-modulation of the tumor microenvironment for enhanced chemo-catalytic therapy
Linqiang Mei, Dongqing Ma, Qin Gao, Xiao Zhang, Wenhui Fu, Xinghua Dong, Gengmei Xing, Wenyan Yin, Zhanjun Gu, Yuliang Zhao
Mater. Horiz., 2020, DOI: 10.1039/d0mh00105h
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号