基于金-硒界面的高保真电化学生物检测平台
金电极具有优良的电化学性质,已被广泛地用于构建电化学生物检测平台。金电极与生物分子之间的电极-分子界面对生物检测平台的稳定性和效率至关重要。传统的金电极-分子界面主要由电极和巯基化合物构建,所形成的Au-S界面在生物体系的应用中易受谷胱甘肽(GSH)和其它生物硫醇破坏,导致检测结果失真。此外,Au-S界面中从电极到分子的电荷注入能量势垒较高,并非电化学检测中理想的电极-分子界面。
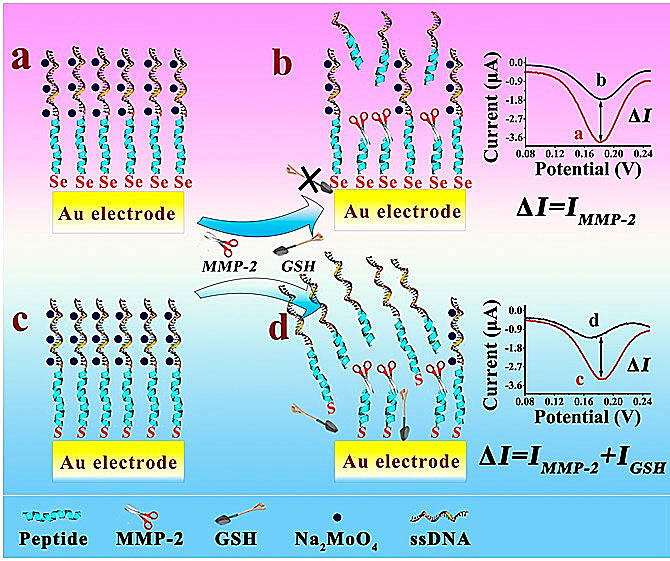
图1. 基于金-硒界面的电化学生物检测平台用于MMP-2高保真检测
针对以上问题,山东师范大学唐波教授(点击查看介绍)研究团队利用Au-Se键形成的电极-分子界面构建了一种高保真电化学生物检测平台用以避免巯基化合物的干扰,并有效的提高电化学检测效率(图1)。在该平台中,Se修饰的MMP-2特异性识别的肽链(P1)可通过Au-Se键组装至Au电极表面。含有12个胞嘧啶碱基的单链DNA(ssDNA)通过酰胺键连接到P1肽链的另一端。在Na2Mo2O3存在时,ssDNA含有的磷酸基团可以与钼酸盐在合适的电位下发生氧化还原发生,产生电流。其电流信号的变化对2.0 pmol/L ~5.0 nmol/L MMP-2呈现了良好的线性关系,可实现MMP-2的定量检测。
相较于Au-S界面,Au-Se界面展示了优良的电化学检测性能(图2)。在高浓度GSH和其它多种巯基化合物存在下,由Au-Se界面构建的电化学检测平台具有良好的稳定性和对MMP-2响应的特异性,检测灵敏度低至1.3 pmol/L。基于键能理论计算和循环伏安法对金表面吸附的硫醇或硒醇的单电子还原反应(RS-Au+ e- → RS- + Au, RSe-Au + e- → RSe- + Au)电位的测定,研究人员推断相较于Au-S键,Au-Se 键具有更高的键能,从而有利于其构建的电化学检测平台在生物体系中实现高保真检测。此外,研究人员通过化学阻抗测试(EIS)与表面增强拉曼散射(SERS)确认了Au-Se界面具有更高的电子转移率。最终,所构建的基于Au-Se界面的电化学检测平台被成功的应用于炎症环境下HepG2细胞MMP-2分泌过程的高保真实时监测。
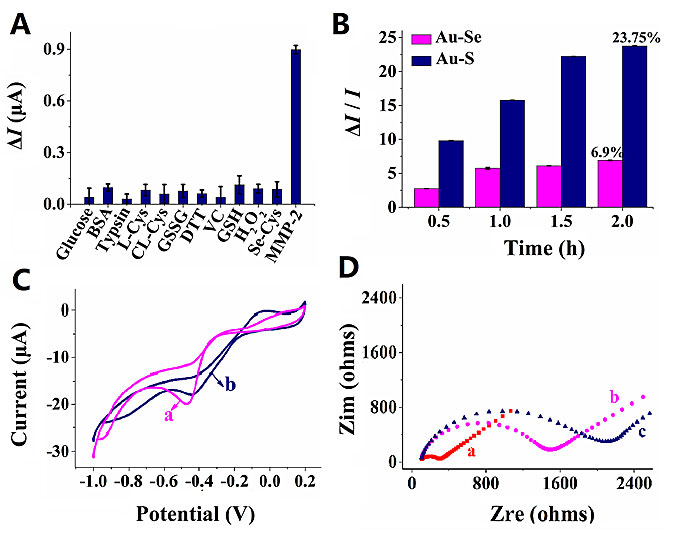
图2. 基于Au-Se界面的电化学生物检测平台性能分析。A. 对MMP-2特异性响应评估。B. 在5.0 mmol/L GSH存在时,基于Au-Se界面的电化学生物检测平台与基于Au-S界面的电化学生物检测平台的稳定性评估。C. 循环伏安法测试 P1修饰的金电极(a)和P2修饰的金电极(b)的还原解吸过程。D. 化学阻抗测试裸金电极(a)、P1修饰的金电极(b)和P2修饰的金电极(c)电子转移率。
此项工作所构建的基于Au-Se界面的电化学生物检测平台有效解决了GSH等生物硫醇对传统电化学生物检测的干扰,降低了电极-分子界面电荷注入能量势垒,提高了电化学检测效率,实现了生物分子的高保真、高效电化学检测,为电化学生物检测平台的设计及其在生物传感和临床检测的应用方面提供了一种新途径。
相关研究成果近期发表在Analytical Chemistry 上,文章的第一作者是山东师范大学博士研究生陈衍政,通讯作者为李璐教授和唐波教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A High-Fidelity Electrochemical Platform Based on Au-Se Interface for Biological Detection
Yanzheng Chen, Xiaoting Song, Lu Li*, Bo Tang*
Anal. Chem., 2020, 92, 5855-5861, DOI: 10.1021/acs.analchem.9b05509
导师介绍
唐波
https://www.x-mol.com/university/faculty/12175
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号