基于超分子手性的立体选择性控制策略:β环糊精二聚体调控的蒽酸光二聚反应
通过催化、酶促和光氧化还原反应诱导基态分子的手性是现代化学研究的热点之一,所得到的汇总结果和观点极大地方便了直观阐明相关反应中起作用的控制因素和立体区分机制,也为设计合理的合成路线和选择合适的催化剂、底物和条件以获得最佳立体化学结果提供了通用的、强有力的工具。近日,四川大学的杨成(点击查看介绍)课题组利用一系列的桥联β-环糊精(β-CD)为手性源,得到了光激发态二聚反应中最高的化学和立体选择(图1)。

图1. β-CD二聚体调控的2-蒽酸光二聚反应示意图。
经过持续多年对2-蒽甲酸 (AC, X = CO2-,图2) 光环二聚反应的研究,该反应已成为评价手性主体介导超分子手性光反应的能力或性能的一个基准反应。迄今为止,最成功的激发态反应立体化学控制的例子是用犬血清白蛋白疏水性结合空腔中AC的光环二聚反应,其对映体syn-9,10:9',10'-HT(2)的对映体过量(ee)为97%,产率为77%。然而,66 kDa的犬血清白蛋具有高度复杂的三维结构,虽然显示出了优异的光致手性催化性能,但其及不易获得也不容易清楚地阐明其中的具体反应机理。而人工或半合成的手性主体在调控激发态反应时通常表现出低的立体选择性水平,这使得设计出具有同等或更高立体控制水平的简单手性主体成为了一个巨大的挑战。
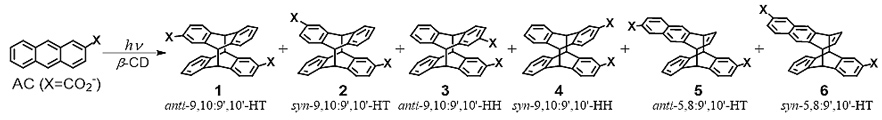
图2. β-CD调控的2-蒽酸光二聚反应。
杨成课题组曾经发现γ-CD衍生物可以和AC形成1:2主客体复合物,进而有效的提高光反应的活性和选择性(J. Am. Chem. Soc., 2014, 136, 6916)。γ-CD中引入敏化剂可以实现催化的AC光二聚反应(Org. Lett., 2018, 20, 1680)。而两个天然β-CD形成的胶囊状结构可以和AC形成2:2主客体复合物,并产生反常光二聚产物5和6(J. Am. Chem. Soc., 2018, 140, 3959)。该课题组设想通过桥联方式将两个β-CD连接起来能进一步限制两个空腔的相对位置,提高β-CD胶囊空腔的限制作用,从而提高该光化学反应的立体选择性。为了实现这个猜想,他们合成了一系列β-CD二聚体(图3),通过这些二聚体调控AC的光二聚反应,来深入研究连接β-CD桥的位置、角度、结构以及长度对该光二聚立体化学结果的影响。
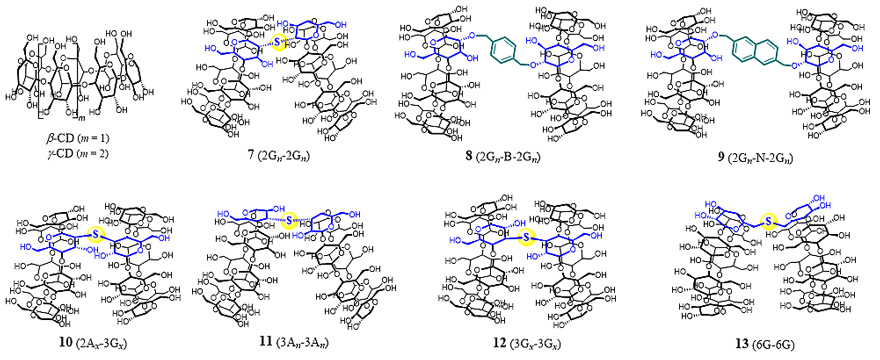
图3. 天然环糊精及环糊精二聚体的化学结构
该工作系统的研究揭示了超分子手性光反应发生的作用因素和机制,证明了主体化合物的结构以及反应的途径是提高光化学反应立体选择性的关键。通过化合物的结构和反应条件的筛选,最终化合物12在低pH或低温的反应条件下,实现了对AC光二聚反应的极限立体控制,使其中产物2的相对产率达到了98%,ee值高达100%(图4)。该工作也进一步建立了可能适用于更广泛的超分子手性光反应的指导原则。
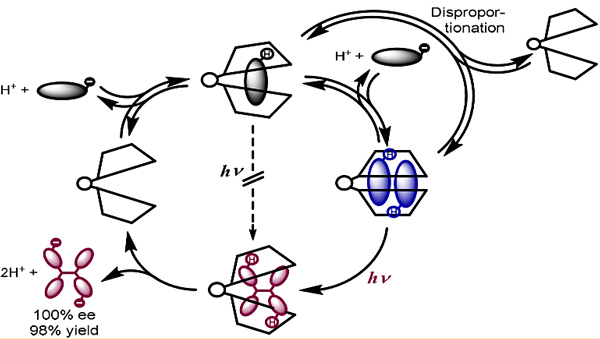
图4. 桥联环糊精催化蒽酸光二聚反应的机理图
这一成果近期发表在J. Am. Chem. Soc.上,文章的第一作者是四川大学博士研究生纪杰城。神户学院大学的袁德其教授和大阪大学的Yoshihisa Inoue教授为共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

An Ultimate Stereocontrol in Supramolecular Photochirogenesis: Photocyclodimerization of 2-Anthracenecarboxylate Mediated by Sulfur-Linked β-Cyclodextrin Dimers
Jiecheng Ji, Wanhua Wu, Wenting Liang, Guo Cheng, Ryohei Matsushita, Zhiqiang Yan, Xueqin Wei, Ming Rao, De-Qi Yuan,* Gaku Fukuhara, Tadashi Mori, Yoshihisa Inoue,* Cheng Yang*
J. Am. Chem. Soc., 2019, 141, 9225-9238, DOI: 10.1021/jacs.9b01993
导师介绍
杨成
https://www.x-mol.com/university/faculty/12793
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号