Pd催化酮与分子内炔烃的α-位烯丙基化:非对映选择性构建[3.2.1]桥环
酮与炔基的分子内Conia-ene 反应是一种重要的构建桥环或稠环骨架的方法,广泛应用于天然产物的全合成中。以往的研究主要利用π-酸性金属催化剂,在酮α-位与炔烃的近端碳之间形成新的C-C键。美国芝加哥大学董广彬教授(点击查看介绍)课题组设想能否发展新催化策略实现酮α-位碳与炔丙位碳之间的偶联,从而一步构建具有两个连续手性中心的[3.2.1]桥环骨架。
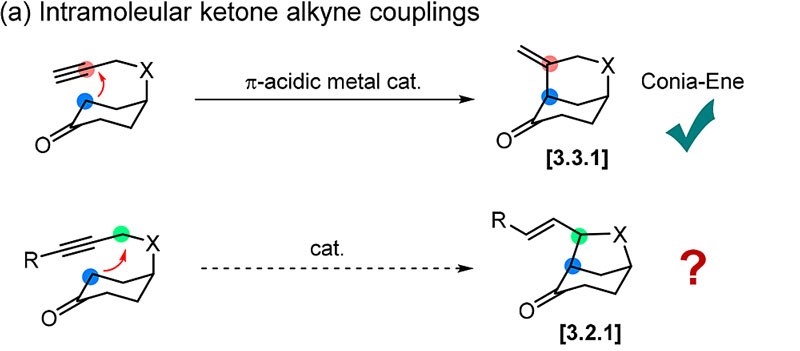
事实上,Yamamoto教授和Trost教授报道炔烃在Pd和酸的催化作用下可以产生亲电性的烯丙基钯物种,与一系列常见的亲核试剂实现烯丙基化。但将合成中常见的非活化的酮作为亲核试剂与炔烃实现烯丙基化,直到2016年,才由Lin课题组通过脯氨酸与Pd协同催化的策略实现。随后,Zhao课题组利用手性配体和手性胺催化剂,报道该反应的不对称版本。但是,酮α-位直接与炔烃的分子内烯丙基化反应目前还未见报道。
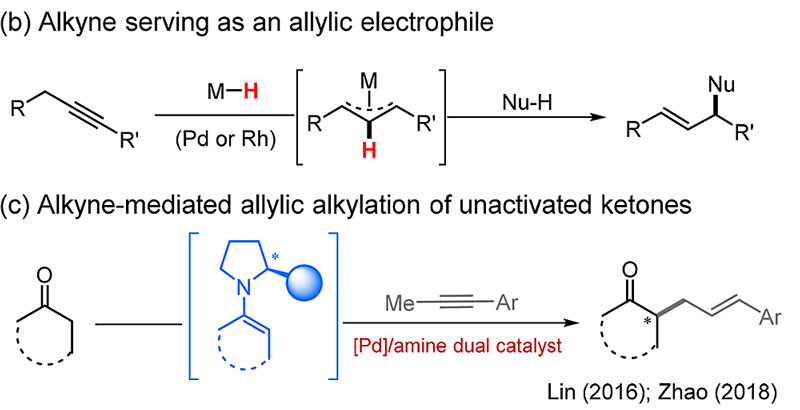
最近,董广彬教授课题组实现了Pd催化酮与分子内炔烃的α-位烯丙基化反应。该反应通过调节配体和添加剂可以快速、非对映选择性的得到endo型和exo型的环己酮[3.2.1]桥环骨架。该反应不需要使用胺作为协同催化剂,原子经济性高。该工作发表在ACS Catalysis 上,第一作者是董广彬教授课题组的联合培养博士生郑鹏飞。
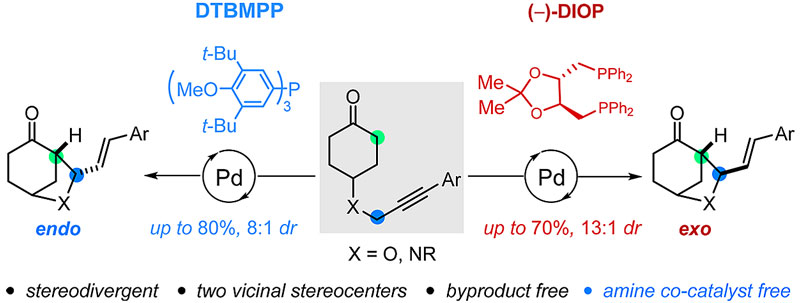
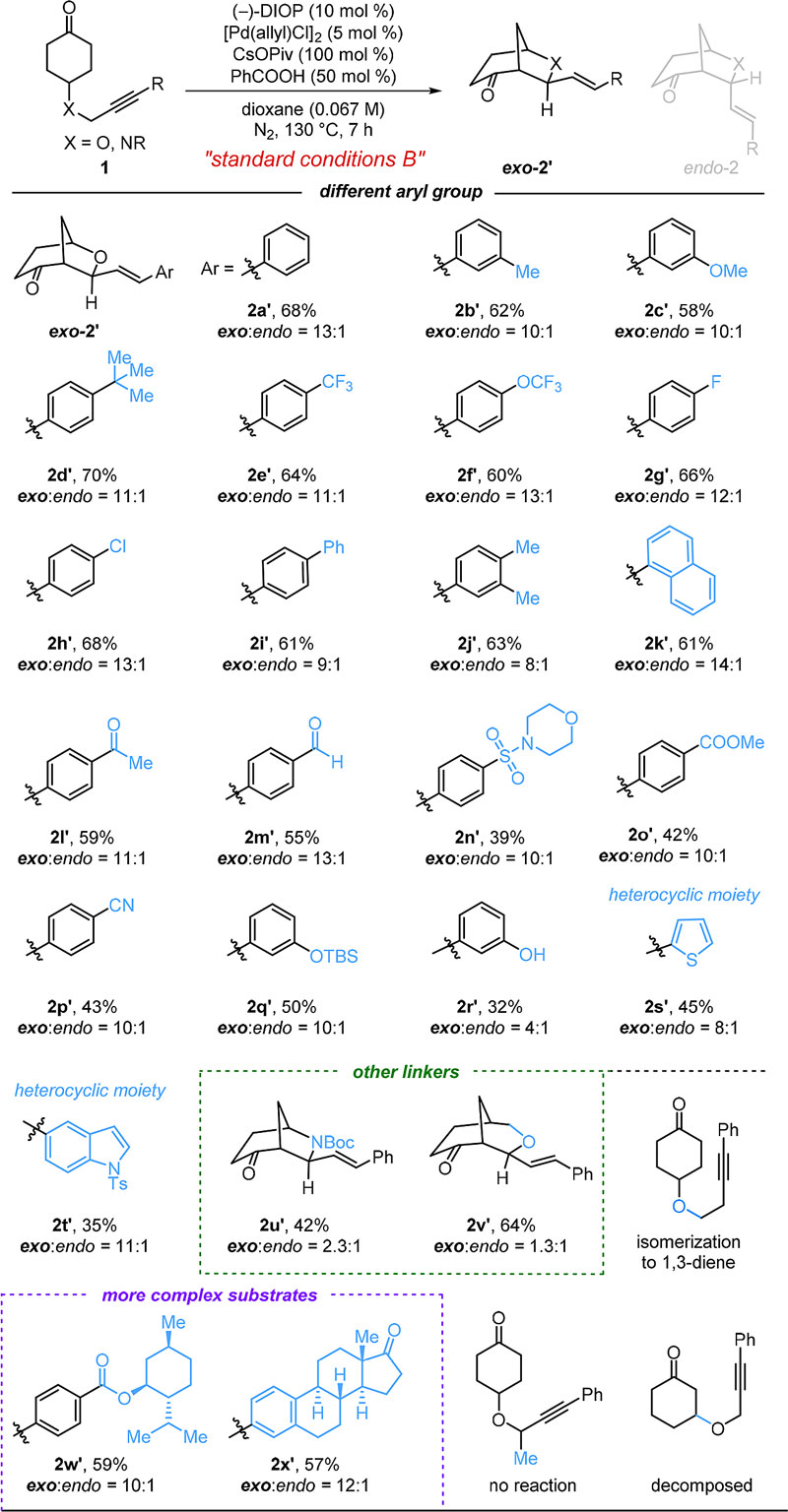
该反应的发现源自于董广彬课题组一直探索的Pd催化酮与炔烃的偶联反应。通过一系列条件优化,当使用 DTBMPP (tris(3,5-di-tert-butyl-4-methoxyphenyl)-phosphine)大位阻单齿配体和HFIP时可以得到endo型非对映选择性产物(yield:80% ,endo:exo=8:1);当使用DIOP 双齿配体和PhCOOH时主要得到exo型非对映选择性产物(yield:68% ,endo:exo=1:13)。同时,通过一系列对照实验发现,配体在非对映选择性调节中起关键作用。
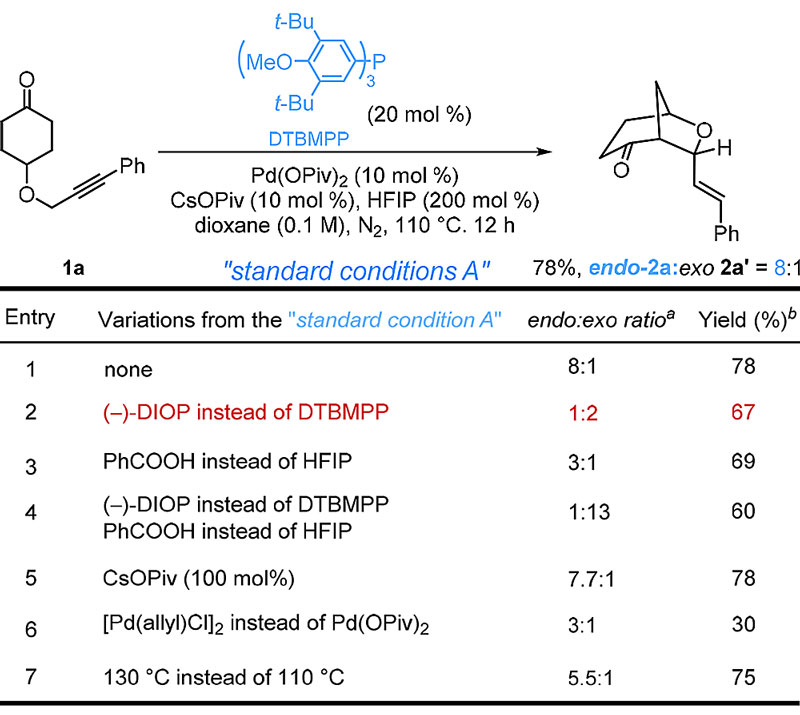
在优化的endo型和exo型反应条件下,该反应具有良好的底物和官能团(醛基、酯基、羟基、氰基等)兼容性,对杂环(吲哚、噻吩等)和氮原子连接的炔烃底物也能很好的兼容。但遗憾的是,延长碳链或改变炔丙基与环己酮的连接位点则不能得到理想的产物。

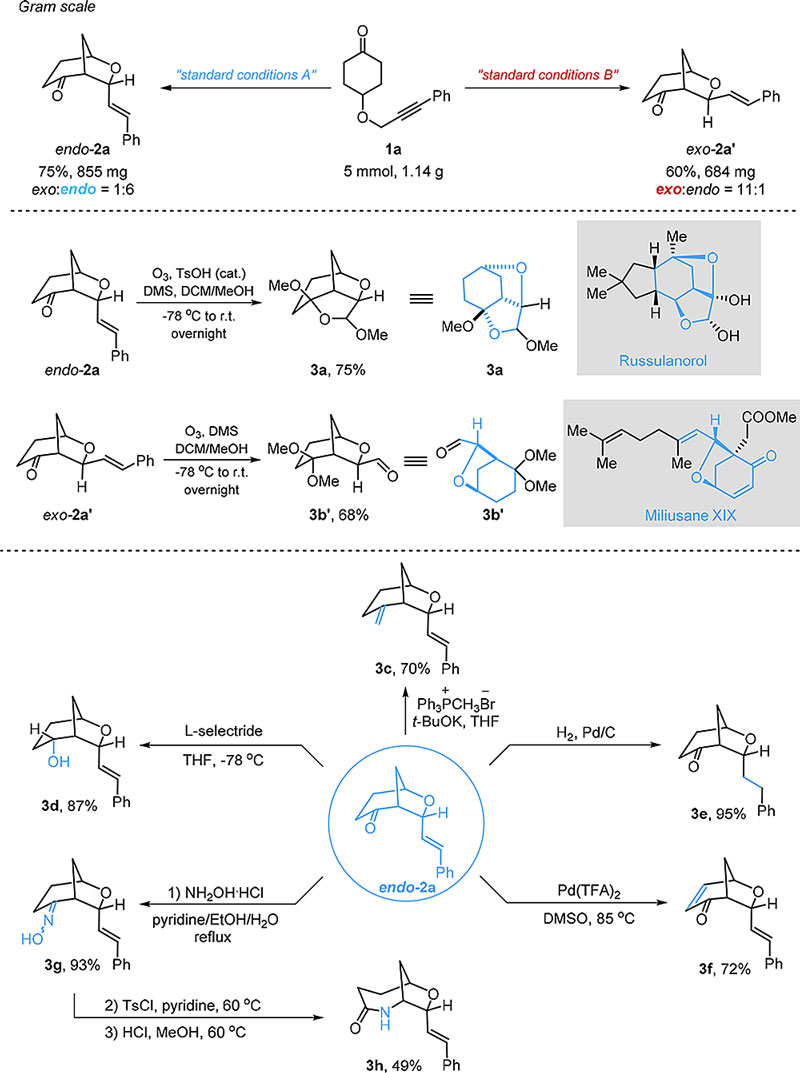
随后,作者对该反应进行了克级水平的尝试,得到良好的结果。值得一提的是,当对endo型产物进行臭氧化转化时,由于反式烯烃在空间上与羰基距离较近,在MeOH作为溶剂时,得到与russulanorol核心骨架类似的三环半笼状的结构;对exo型的产物进行臭氧化转化时,则产生缩酮保护的醛。同时,endo型催化产物可以进一步转化成官能团多样的桥环化合物。
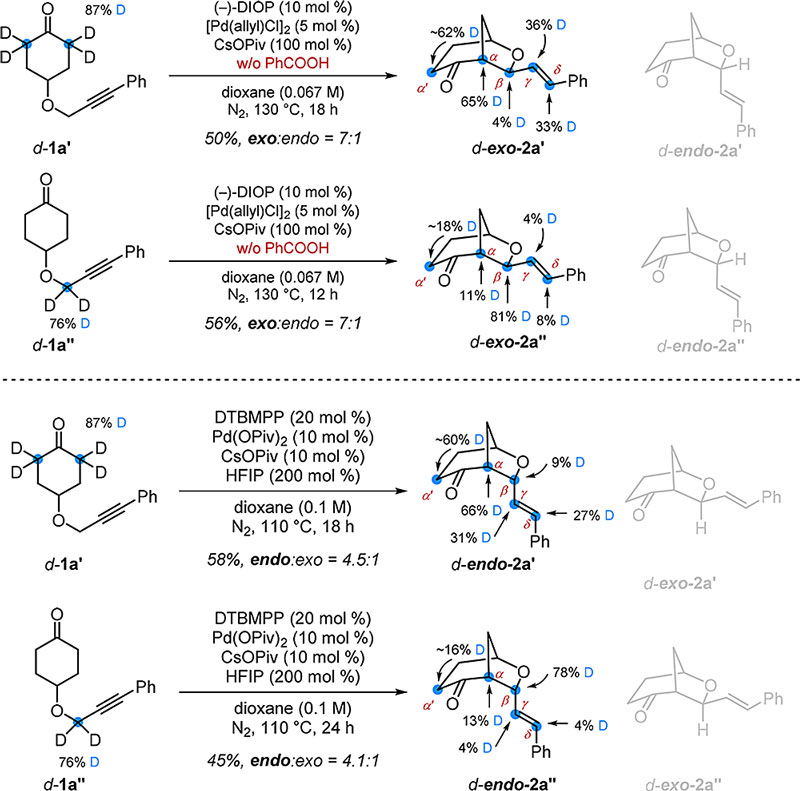
最后,通过氘代实验验证了该反应是通过炔烃/联稀异构化产生烯丙基Pd物种的方式发生的。
总结
董广彬教授课题组发现了Pd催化酮与分子内炔烃的烯丙基化反应。该反应不需要添加胺催化剂,可以通过调节配体和酸性添加剂,选择性的得到endo型和exo型的环己酮桥环骨架。该反应具有良好的底物官能团兼容性,氘代实验证明了该反应是通过炔烃/联稀异构化产生烯丙基Pd物种的方式发生的。后续针对该反应中配体在非对映选择性的作用以及对映选择性反应研究正在进行中。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Pd-Catalyzed Intramolecular α-Allylic Alkylation of Ketones with Alkynes: Rapid and Stereodivergent Construction of [3.2.1] Bicycles
Pengfei Zheng, Chengpeng Wang, Ying-Chun Chen, Guangbin Dong
ACS Catal., 2019, 9, 5515-5521, DOI: 10.1021/acscatal.9b00997
导师介绍
董广彬
https://www.x-mol.com/university/faculty/352
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号