Angew. Chem.:通过主客体策略精确递送光敏剂和前药用于近红外光激活联合治疗
相较于单独给药,联合给药即同时递送两种或多种治疗药物可达到很好的协同治疗效果,已经成为药物递送的研究热点。其中,光动力治疗和化疗协同治疗可有效抑制肿瘤生长。近年来虽然有大量光敏剂和活性氧响应前药联合递送用于肿瘤治疗的报道,但是仍然缺少有效的方法去调节递送两种药物的精确比例,从而限制了此类体系的应用前景。一般而言,对于光敏剂和前药的联合递送体系,以下三种方式最常见:1)共价修饰光敏剂和药物分子;2)将一种药物修饰为载体用来包载另外一种或多种药物;3)用其他有机或者无机载体包载多种药物。共价修饰受限于有限的修饰位点和复杂的合成纯化步骤很难有效调节两种药物的比例。后两种方式则受限于药物结构和物化性质,很难保证包载的精确比例从而面临提前释放的风险,增加了联合给药的不确定性,难以达到最优的治疗效果。
最近,南洋理工大学赵彦利教授(点击查看介绍)课题组和中山大学药学院(深圳)梅林教授(点击查看介绍)课题组合作开发了一种基于主客体作用的超分子纳米载药体系,用于优化光敏剂和活性氧响应的前药比例,从而最大化提高联合给药的治疗效果(图1)。该体系在近红外光照射下能够有效实现光动力治疗以及连锁的前药激活带来的化学治疗。
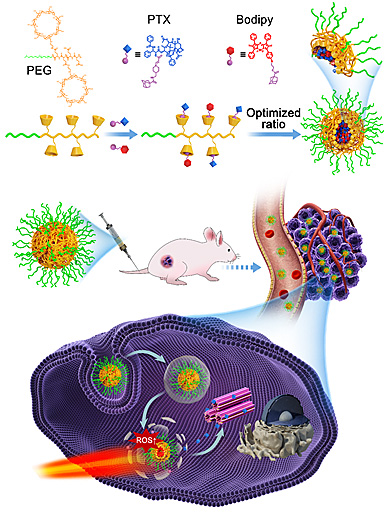
图1:β环糊精修饰的聚乙二醇聚谷氨酸共聚物、金刚烷修饰的BODIPY光敏剂和金刚烷氨基丙烯酸酯修饰的紫杉醇前药通过超分子自聚集形成纳米载药体系用于肿瘤的联合治疗。
他们合成了β环糊精修饰的聚乙二醇聚谷氨酸共聚物作为主体化合物,金刚烷修饰的BODIPY作为光敏剂,金刚烷氨基丙烯酸酯修饰的紫杉醇作为前药。基于β环糊精与金刚烷之间有效的主客体键合作用,光敏剂和前药分子与主体高分子之间的作用方式是相同并且确定的。将不同比例的光敏剂和前药分子溶解在DMSO中,超声下将其加入主体溶液得到确定比例的纳米粒子。在近红外光照射下,当光敏剂和前药分子的比例为2:3的时候,相应的纳米体系达到最好的协同治疗效果。动物实验结果显示,此类纳米药物具有更长的体内循环时间,可有效富集在肿瘤部位。基于最优化的光动力治疗和化疗的协同作用,展现出高效的抑制肿瘤生长的效果。该方法有望用于优化各种联合给药体系并提升肿瘤诊疗的效果,为联合给药体系提供有意义的探索和新的研究思路。
相关工作发表在Angewandte Chemie International Edition 上。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

NIR-Light-Activated Combination Therapy with Precisely Integrated Photosensitizer and Prodrug by a Host‐Guest Strategy
Hongzhong Chen, Xiaowei Zeng, Huijun Phoebe Tham, Soo Zeng Fiona Phua, Wei Cheng, Wenfeng Zeng, Haoran Shi, Lin Mei, Yanli Zhao
Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201900886
导师介绍
赵彦利
https://www.x-mol.com/university/faculty/4465
梅林
https://www.x-mol.com/university/faculty/50085
(本稿件来自Wiley)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号