亲和纯化新方法——多肽特异共价固定诱导蛋白
在蛋白组学的研究中,一个基础且重要的研究方法是将目标蛋白从众多的蛋白中利用亲和纯化的方法分离出来。这就像钓鱼一样,用一个好鱼钩将想要钓的一类鱼从众多的海洋生物中钓出来。纪晓岚的《钓鱼绝句》中吟诵到:“一篙一橹一渔翁,一个渔翁一钓钩。一拍一呼又一笑,一人独占一江秋。”就像绝句中写到的那样,“钓钩”之于“渔翁”非常重要。科研上的“姜太公”们也在不断探索如何设计鱼钩将所需要的一类目标蛋白更好地分离出来。能将目标蛋白“钓出来”的一类蛋白叫引诱蛋白(bait protein),设计引诱蛋白的固定方式是构建“鱼钩”的重要环节。
传统的研究中,通常利用非共价作用,例如亲疏水性、极性或者离子键等作用,将蛋白固定在基质上。但是非共价固定的缺点是相互作用太弱,在后续实验处理过程中会损失一部分引诱蛋白和目标蛋白。非共价固定方法还包括将引诱蛋白加上一个标签(tag),例如His、Flag、GST等,但是蛋白仍然是通过非共价方式固定,而且仍然不能保证固定的效率和特异性。在已知的共价固定方法中,能够形成共价键的两个生物共价反应基团的反应活性和特异性都有所欠缺,比如NHS树脂能与蛋白中所有赖氨酸侧链的氨基形成共价键,导致蛋白在树脂表面杂乱无章得排列,就导致一些位点被阻碍,不能够充分和其他蛋白相互作用,因此杂乱无章得共价作用会损失一些目标蛋白。
为了优化蛋白的固定方式,加拿大西安大略大学的Shawn Li教授团队、香港中文大学夏江教授团队以及香港城市大学的张亮教授合作提出了一种特异性共价固定诱导蛋白的方法,并将此方法应用于研究赖氨酸甲基化。
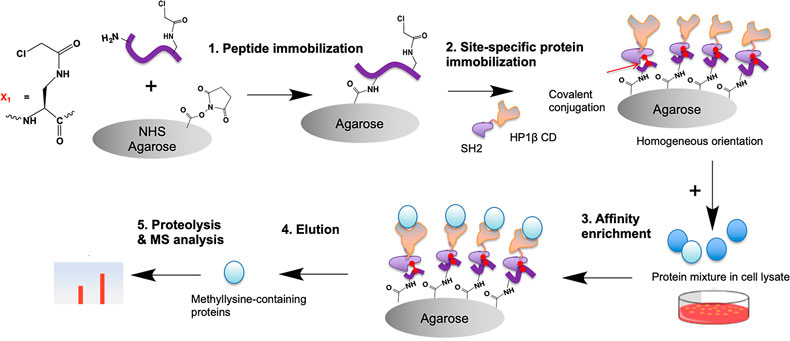
HP1β 蛋白的CD结构域是能够“钓”目标蛋白赖氨酸甲基化蛋白的一个诱导“鱼钩”。研究团队首先构建了HP1β 蛋白的CD结构域和另外一个SH2结构域结合的融合蛋白,并通过能与SH2结构域共价特异反应的反应活性多肽(利用半胱氨酸和氯乙酰氯的特异性生物共价反应),将HP1β 蛋白的CD结构域通过SH2结构域共价固定在基质上,使HP1β 蛋白的CD结构域能充分与其他蛋白作用,从而聚集目标蛋白,便于纯化赖氨酸甲基化的蛋白。

在利用HP1β 蛋白的CD结构域亲和纯化赖氨酸甲基化蛋白质组的应用中体现了特异性共价固定诱导蛋白的优势,并且从与HP1β 蛋白的CD结构域结合的332个蛋白中纯化出了184个甲基化蛋白,发现了275个甲基化位点,发现了30个新的甲基化蛋白。说明利用共价特异反应的反应活性多肽固定蛋白可以应用于蛋白组学中的亲和纯化。
这一成果近期发表在Analytical Chemistry 上,文章的第一作者是王蕊博士和加拿大的Mei Huang博士。
该论文作者为:Rui Wang, Mei Huang, Linting Li,Tomonori Kaneko, Courtney Voss,Liang Zhang,* Jiang Xia,* and Shawn S. C. Li*
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Affinity Purification of Methyllysine Proteome by Site-Specific Covalent Conjugation
Anal. Chem., 2018, 90, 13876–13881, DOI: 10.1021/acs.analchem.8b02796
香港中文大学夏江教授团队多年来在蛋白质定点反应上有较深入的研究,包括半胱氨酸、酪氨酸和赖氨酸的定点反应。氨基酸定点反应在细胞标记、细胞内的共价抑制、蛋白质定点固定等方面有广泛用途。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号