双重响应黑磷纳米药物肿瘤放疗增敏
基于肿瘤的生化特性进行化学设计,已经成为创造和发现创新药物的重要途径。将纳米化学设计与生物医学应用相融合,利用化学分子及材料的生物响应特性,进行靶向修饰,可实现肿瘤的精准打击,为肿瘤的药物运输供新的策略与思路。暨南大学陈填烽教授(点击查看介绍)课题组一直致力于靶向纳米药物的化学设计及肿瘤诊疗应用研究。最近,该团队与中国科学院深圳先进技术研究院喻学锋教授(点击查看介绍)团队合作,开发了一种具有表面电荷翻转能力和生物响应控制释放的纳米体系用于黑色素瘤的放射治疗。此项研究成果发表在纳米领域重要期刊ACS Nano (IF =13.709)上,博士生陈樑是该文章的第一作者。
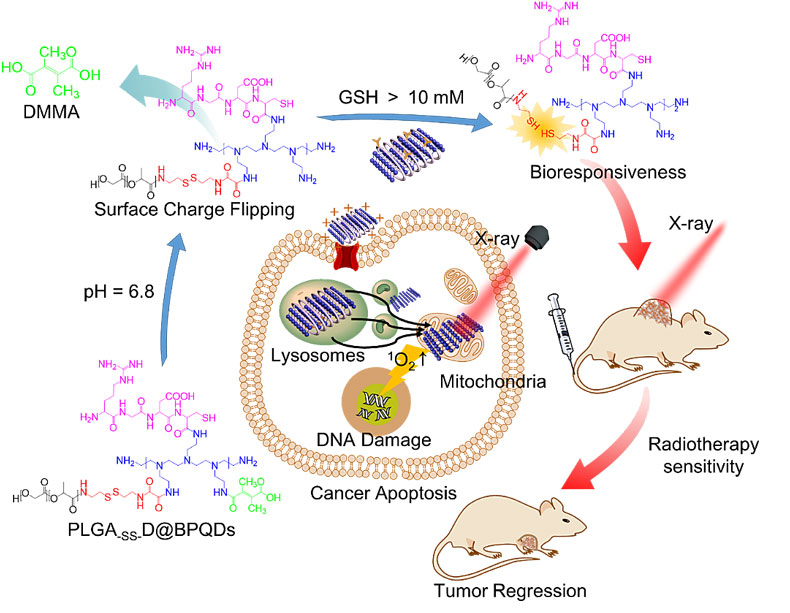
图1. 本研究设计思路:具有酸响应特性纳米体系PLGA-SS-D@BPQDs的设计及其放疗增敏作用机理。
目前,放疗和化疗是临床上肿瘤最常用的治疗方法,但其疗效受到射线辐射剂量和药物毒性的极大限制。因此,开发高效低毒的放化疗增敏剂具有重大意义。近年来,大量的半导体材料被应用于放疗增敏,其机制主要在于与X射线相互作用产生显著的单线态氧,进而增强X射线对肿瘤组织的损伤。其中,黑磷量子点(BPQDs)因其独特的光电效应和生物降解性等使其在生物及医学领域具有广阔应用前景。黑磷是红磷经高温高压后得到的黑色惰性同素异形体。研究团队利用探头超声和水浴超声的液相剥离方法,可控制备横向尺寸约为2.6纳米的黑磷量子点。黑磷是直接带隙半导体带隙,即电子导电能带(导带)底部和非导电能带(价带)顶部在同一位置。这意味着黑磷量子点和光或X射线可以直接耦合。因此黑磷量子点作为高效放疗增敏剂用于肿瘤治疗拥有巨大的潜力。
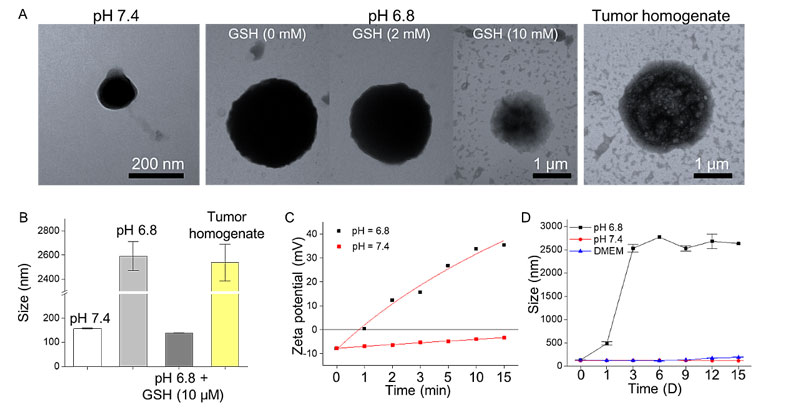
图2. 黑磷纳米药物的生物响应特性。(A)PLGA-SS-D@BPQDs纳米体系在pH 7.4,pH 6.8(GSH浓度为0 mM, 2 mM 和10 mM)和肿瘤微环境的透射电镜形貌变化。(B)纳米体系在pH 7.4,pH 6.8(GSH浓度为0 mM, 2 mM 和10 mM)和肿瘤微环境的粒径变化。(C)纳米体系的在pH 7.4和pH 6.8的PBS溶液中的表面电位翻转能力。(D)纳米体系在pH 6.8,pH 7.4和DMEM溶液中的粒径变化。
本研究选择低毒性且具有良好生物响应性的聚乳酸-羟基乙酸共聚物(PLGA)作为载体,并负载具有放疗增敏作用的BPQDs,修饰上生物相应的二硫键嵌段用于连接阳离子聚合物聚乙烯亚胺(PEI)来提高纳米体系在水中的分散性,及提高肿瘤细胞的吸收,并利用具有酸不稳定的β-羧酸基团可逆地修饰氨基,最终得到一种具有多重生物相应能力的纳米体系,实现肿瘤的放疗增敏。
肿瘤微环境具有弱酸性的化学特点,因此,黑磷纳米体系在修饰了特异性靶向多肽的基础上,再装备上具有酸响应性的基团,利用酸不稳定的β-羧酸基团可逆地修饰氨基,从而形成了具有表面电荷翻转能力的纳米体系。当该体系游离在血液循环中时会保持负电性,而当该纳米系统到达肿瘤部位时,弱酸性的微环境使得酸不稳定的β-羧酸基团脱落,氨基重新暴露于纳米管的表面,整个纳米管体系表面电荷将发生改变,由原来的负电荷翻转为正电荷,让该纳米系统更容易进入肿瘤细胞并累积下来。纳米体系进入肿瘤细胞后,连接PLGA和PEI的二硫键被细胞内高浓度的谷胱甘肽(大于10 mM)还原断裂,纳米粒子迅速降解并释放出BPQDs量子点,从而增强药物放疗的效果,为肿瘤个性化精准治疗提供新的思路。
此项工作为黑磷的放疗增敏应用和纳米载药体系的靶向设计提供了新的策略。
上述研究工作得到了国家万人计划青年拔尖人才项目、国家高技术研究发展计划 (863计划) 项目、国家自然科学基金等项目的资助。
该论文作者为:Leung Chan, Pan Gao, Wenhua Zhou, Chaoming Mei, Yanyu Huang, Xue-Feng Yu, Paul K. Chu, Tianfeng Chen
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Sequentially Triggered Delivery System of Black Phosphorus Quantum Dots with Surface Charge-Switching Ability for Precise Tumor Radiosensitization
ACS Nano, 2018, 12, 12401-12415, DOI: 10.1021/acsnano.8b06483
导师介绍
陈填烽
https://www.x-mol.com/university/faculty/26825
喻学锋
https://www.x-mol.com/university/faculty/47837
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号